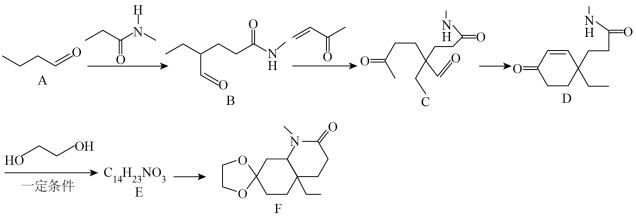
化合物F是一种重要的有机合成中间体,某研究小组按下列路线进行合成:
已知: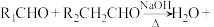
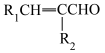
请回答下列问题:
(1)有机物B所含的官能团名称是___________ ,B→C的反应类型为___________ 。
(2)化合物E的结构简式是___________ 。
(3)写出D→E的化学方程式:___________ 。
(4)1分子有机物F分子中含有的手性碳原子数为___________ 。
(5)上述流程涉及的非金属元素中,电负性由大到小的顺序为___________ ,第一电离能最大的为___________ (填元素符号)。
(6)有机物H是D的同分异构体,写出符合下列条件的H的结构简式:___________ (任写一种)。
①IR谱检测表明:分子中含有一个苯环,有 键,无
键,无 、
、 键。
键。
② 谱检测表明:分子中共有5种不同化学环境的氢原子。
谱检测表明:分子中共有5种不同化学环境的氢原子。
③仅含有两种官能团,其中一种为 ,且氨基与苯环直接相连。
,且氨基与苯环直接相连。

已知:
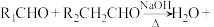
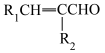
请回答下列问题:
(1)有机物B所含的官能团名称是
(2)化合物E的结构简式是
(3)写出D→E的化学方程式:
(4)1分子有机物F分子中含有的手性碳原子数为
(5)上述流程涉及的非金属元素中,电负性由大到小的顺序为
(6)有机物H是D的同分异构体,写出符合下列条件的H的结构简式:
①IR谱检测表明:分子中含有一个苯环,有
 键,无
键,无 、
、 键。
键。②
 谱检测表明:分子中共有5种不同化学环境的氢原子。
谱检测表明:分子中共有5种不同化学环境的氢原子。③仅含有两种官能团,其中一种为
 ,且氨基与苯环直接相连。
,且氨基与苯环直接相连。
更新时间:2023-09-10 19:54:49
|
相似题推荐
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐1】某研究小组拟合成染料X和医药中间体Y。

已知:① ②
②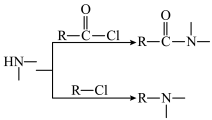 ③
③ ④
④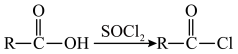 。
。
(1)下列说法正确的是_________ 。
A.化合物A能与能与NaHCO3反应产生气体 B.X的分子式是C15H14Cl2O3N2
C.化合物C能发生取代、还原、加成反应 D.A→B,B→C的反应类型均为取代反应
(2)化合物D的结构简式是_________ 。
(3)写出E+H→F 的化学反应方程式__________________ 。
(4)写出化合物B(C10H10O4)同时符合下列条件的两种同分异构体的结构简式______________ 。
①与NaHCO3溶液反应,0.1mol该同分异构体能产生4.48L(标准状况下)CO2气体;②苯环上的一氯代物只有两种且苯环上的取代基不超过三个;③核磁共振氢谱有五种不同化学环境的氢,且峰面积比为1:2:2:2:3。
(5)设计以乙烯为原料合成制备Y(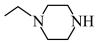 )的合成路线
)的合成路线________________ (用流程图表示,无机试剂任选)。

已知:①
 ②
② ③
③ ④
④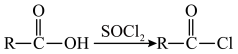 。
。(1)下列说法正确的是
A.化合物A能与能与NaHCO3反应产生气体 B.X的分子式是C15H14Cl2O3N2
C.化合物C能发生取代、还原、加成反应 D.A→B,B→C的反应类型均为取代反应
(2)化合物D的结构简式是
(3)写出E+H→F 的化学反应方程式
(4)写出化合物B(C10H10O4)同时符合下列条件的两种同分异构体的结构简式
①与NaHCO3溶液反应,0.1mol该同分异构体能产生4.48L(标准状况下)CO2气体;②苯环上的一氯代物只有两种且苯环上的取代基不超过三个;③核磁共振氢谱有五种不同化学环境的氢,且峰面积比为1:2:2:2:3。
(5)设计以乙烯为原料合成制备Y(
 )的合成路线
)的合成路线
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
【推荐2】有机物G是合成免疫抑制剂药物霉酚酸的中间体,可由如下路径合成:
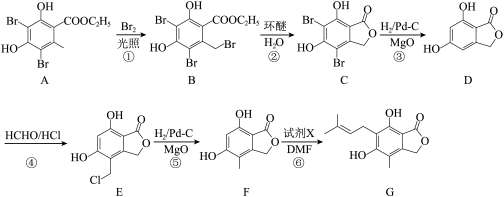
(1)A的实验式为________ ,有机物A→G中均含有的官能团名称为________ 。
(2)反应②的反应类型为________ ,除C外另一种生成物的官能团电子式为________ 。
(3)步骤④可得到副产品有机物J,有机物J和有机物E互为同分异构体,写出有机物J的结构简式________ 。
(4)反应⑥除生成G外还生成HBr,则试剂X的结构简式为________ 。
(5)芳香化合物H是F的同分异构体,符合下列要求的H共有________ 种。
①遇 溶液产生
溶液产生 气体;②1molH与足量银氨溶液反应生成2molAg;
气体;②1molH与足量银氨溶液反应生成2molAg;
③遇氯化铁溶液发生显色反应;④苯环最多三个侧链。
其中含有手性碳原子,且苯环上只有2种不同化学环境的氢原子的结构简式为________ :
(6) 的系统命名为
的系统命名为________ ;已知:直接与苯环相连的卤素原子难与NaOH溶液发生取代反应。参照上述合成路线,设计以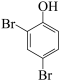 为原料制备
为原料制备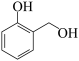 的合成路线(其他试剂任选):
的合成路线(其他试剂任选): ________________ 。

(1)A的实验式为
(2)反应②的反应类型为
(3)步骤④可得到副产品有机物J,有机物J和有机物E互为同分异构体,写出有机物J的结构简式
(4)反应⑥除生成G外还生成HBr,则试剂X的结构简式为
(5)芳香化合物H是F的同分异构体,符合下列要求的H共有
①遇
 溶液产生
溶液产生 气体;②1molH与足量银氨溶液反应生成2molAg;
气体;②1molH与足量银氨溶液反应生成2molAg;③遇氯化铁溶液发生显色反应;④苯环最多三个侧链。
其中含有手性碳原子,且苯环上只有2种不同化学环境的氢原子的结构简式为
(6)
 的系统命名为
的系统命名为 为原料制备
为原料制备 的合成路线(其他试剂任选):
的合成路线(其他试剂任选):
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
解题方法
【推荐3】连花清瘟胶囊中连翘的有效成分连翘酯苷A,具有抗微生物、抗氧化等作用。有研究小组合成了连翘酯苷A的类似物K,进行了相关抗菌研究,合成路线如图:
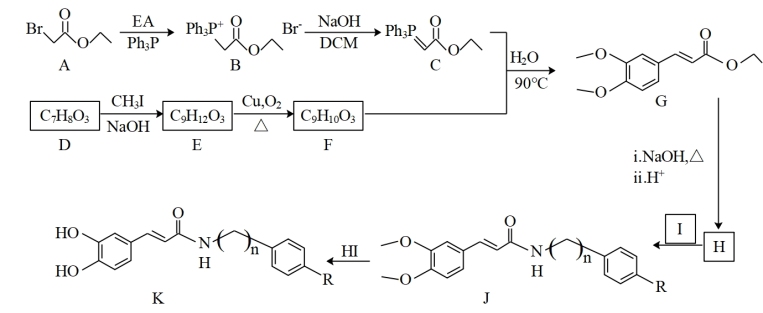
已知:①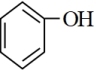
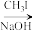

② +CH3CHO
+CH3CHO

请回答下列问题:
(1)G中含氧官能团的名称是_______ ,J→K的反应类型是_______ 。
(2)D→E,E→F两个反应是否可以交换顺序_______ (填“是”或“否”),请说明理由_______ 。
(3)I的结构简式是_______ 。请写出E→F的化学方程式:_______ 。
(4)写出满足下列条件的F的同分异构体的结构简式_______ (任写一种)。
①加入FeCl3溶液显紫色;②能发生水解和银镜反应;③核磁共振氢谱的峰面积之比为6:2:1:1。
(5)请模仿题目信息,以一氯环己烷、乙醛、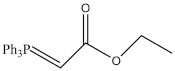 为原料,设计合成
为原料,设计合成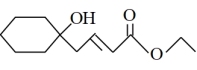 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)_______ 。

已知:①

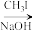

②
 +CH3CHO
+CH3CHO

请回答下列问题:
(1)G中含氧官能团的名称是
(2)D→E,E→F两个反应是否可以交换顺序
(3)I的结构简式是
(4)写出满足下列条件的F的同分异构体的结构简式
①加入FeCl3溶液显紫色;②能发生水解和银镜反应;③核磁共振氢谱的峰面积之比为6:2:1:1。
(5)请模仿题目信息,以一氯环己烷、乙醛、
 为原料,设计合成
为原料,设计合成 的合成路线(无机试剂任选)
的合成路线(无机试剂任选)
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】Ⅰ.魔酸(Magic acid)是最早发现的超强酸,由五氟化锑(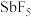 )和氟磺酸(
)和氟磺酸(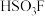 )按体积比
)按体积比 混合制成的混酸,酸性为纯硫酸的1000万倍。
混合制成的混酸,酸性为纯硫酸的1000万倍。
(1)氟磺酸(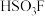 )中元素电负性由大到小的顺序为
)中元素电负性由大到小的顺序为___________ (写汉字名称)。
(2)魔酸根离子中与中心 原子配位的氟磺酸中的原子为
原子配位的氟磺酸中的原子为___________ (填元素符号)。
(3)五氟化锑(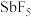 )分子中
)分子中 的杂化类型是下列中的
的杂化类型是下列中的___________ (填字母序号)。
a. b.
b.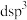 c.
c. d.
d.
Ⅱ.使用超酸可以活化碳氢化合物,如六氟合锑酸( 和
和 的物质的量比
的物质的量比 混合,酸性估计可达无水硫酸的
混合,酸性估计可达无水硫酸的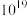 倍)溶液中对甲基环戊烷的羰基化反应。对
倍)溶液中对甲基环戊烷的羰基化反应。对 键的质子化导致失去一个氢气而生成一个碳正离子(其可能发生的重排-碳正离子可能的正电位置并未给出),加入的
键的质子化导致失去一个氢气而生成一个碳正离子(其可能发生的重排-碳正离子可能的正电位置并未给出),加入的 捕获这些碳正离子即生成稳定的酰基碳正离子,它与后处理过程中加入的乙醇发生反应生成相应的乙酯化合物如图所示(超酸中的氢离子用“
捕获这些碳正离子即生成稳定的酰基碳正离子,它与后处理过程中加入的乙醇发生反应生成相应的乙酯化合物如图所示(超酸中的氢离子用“ ”表示)。
”表示)。
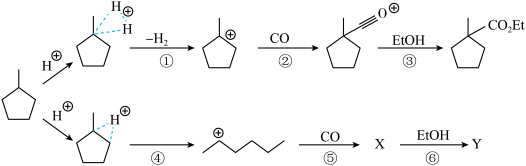
(4)“步骤①”生成的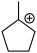 可能发生的碳正离子转移重排,写出“重排”后所得产物“乙酯化合物”的结构简式
可能发生的碳正离子转移重排,写出“重排”后所得产物“乙酯化合物”的结构简式___________ (除题给产物外任写1种)。
(5)步骤③的反应方程式为___________ 。
(6)满足下列条件的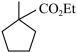 的同分异构体种类有
的同分异构体种类有___________ 种(不考虑立体异构)。
a.存在六元环状结构、且环上只有1~2个侧链
b.能发生银镜反应
c.热氢氧化钠溶液中能水解
(7)Y的系统名称为___________ 。
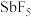 )和氟磺酸(
)和氟磺酸(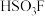 )按体积比
)按体积比 混合制成的混酸,酸性为纯硫酸的1000万倍。
混合制成的混酸,酸性为纯硫酸的1000万倍。(1)氟磺酸(
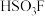 )中元素电负性由大到小的顺序为
)中元素电负性由大到小的顺序为(2)魔酸根离子中与中心
 原子配位的氟磺酸中的原子为
原子配位的氟磺酸中的原子为(3)五氟化锑(
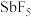 )分子中
)分子中 的杂化类型是下列中的
的杂化类型是下列中的a.
 b.
b.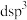 c.
c. d.
d.
Ⅱ.使用超酸可以活化碳氢化合物,如六氟合锑酸(
 和
和 的物质的量比
的物质的量比 混合,酸性估计可达无水硫酸的
混合,酸性估计可达无水硫酸的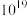 倍)溶液中对甲基环戊烷的羰基化反应。对
倍)溶液中对甲基环戊烷的羰基化反应。对 键的质子化导致失去一个氢气而生成一个碳正离子(其可能发生的重排-碳正离子可能的正电位置并未给出),加入的
键的质子化导致失去一个氢气而生成一个碳正离子(其可能发生的重排-碳正离子可能的正电位置并未给出),加入的 捕获这些碳正离子即生成稳定的酰基碳正离子,它与后处理过程中加入的乙醇发生反应生成相应的乙酯化合物如图所示(超酸中的氢离子用“
捕获这些碳正离子即生成稳定的酰基碳正离子,它与后处理过程中加入的乙醇发生反应生成相应的乙酯化合物如图所示(超酸中的氢离子用“ ”表示)。
”表示)。
(4)“步骤①”生成的
 可能发生的碳正离子转移重排,写出“重排”后所得产物“乙酯化合物”的结构简式
可能发生的碳正离子转移重排,写出“重排”后所得产物“乙酯化合物”的结构简式(5)步骤③的反应方程式为
(6)满足下列条件的
 的同分异构体种类有
的同分异构体种类有a.存在六元环状结构、且环上只有1~2个侧链
b.能发生银镜反应
c.热氢氧化钠溶液中能水解
(7)Y的系统名称为
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
【推荐2】非诺洛芬是一种治疗类风湿性关节炎的药物,通过以下方法合成:

请回答下列问题:
(1)非诺洛芬中的含氧官能团为_____ (填名称)。
(2)反应①中加入的试剂X的分子式为C8H8O2,X的结构简式为_____ ,K2CO3的作用是_____ 。
(3)下列说法不正确的是_____。
(4)若反应⑤所需试剂为E和盐酸,则产物为非诺洛芬和_____ 。
(5)B的一种同分异构体满足下列条件:
Ⅰ.能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应。
Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环。
写出该同分异构体的结构简式:_____ 。
(6)根据已有知识并结合相关信息,写出以 为原料制备
为原料制备 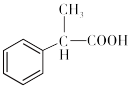 的合成路线流程图(无机试剂任用)
的合成路线流程图(无机试剂任用)_____ 。合成路线流程图示例如下: 。
。

请回答下列问题:
(1)非诺洛芬中的含氧官能团为
(2)反应①中加入的试剂X的分子式为C8H8O2,X的结构简式为
(3)下列说法不正确的是_____。
| A.化合物A可以发生加成反应、取代反应和消去反应 |
| B.反应②中NaBH4作还原剂 |
| C.如果将反应④中NaCN换成HCN,转化率会低很多 |
| D.1mol化合物E最多与6molH2加成 |
(4)若反应⑤所需试剂为E和盐酸,则产物为非诺洛芬和
(5)B的一种同分异构体满足下列条件:
Ⅰ.能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应。
Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环。
写出该同分异构体的结构简式:
(6)根据已有知识并结合相关信息,写出以
 为原料制备
为原料制备  的合成路线流程图(无机试剂任用)
的合成路线流程图(无机试剂任用) 。
。
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
【推荐3】以 和芳香烃
和芳香烃 为原料制备除草剂茚草酮中间体(I)的合成路线如下:
为原料制备除草剂茚草酮中间体(I)的合成路线如下:
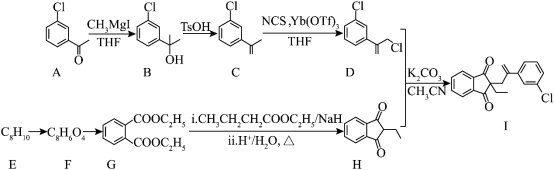
回答下列问题:
(1)A中所含官能团的名称为___________ ,物质 的名称
的名称___________ 。
(2) 的反应类型为
的反应类型为___________ , 中碳原子的杂化类型为
中碳原子的杂化类型为___________ 。
(3)B与C在水中溶解度较大的是___________ ,理由___________ ;
(4)写出 的化学方程式
的化学方程式___________ 。
(5)B的同分异构体中,满足下列条件的结构有___________ 种;其中,核磁共振氢谱有四组峰,且峰面积之比为 的结构简式为
的结构简式为___________ 。
条件:①含有苯环;②与 溶液发生显色反应;③含有2个甲基,且连在同一个碳原子上。
溶液发生显色反应;③含有2个甲基,且连在同一个碳原子上。
 和芳香烃
和芳香烃 为原料制备除草剂茚草酮中间体(I)的合成路线如下:
为原料制备除草剂茚草酮中间体(I)的合成路线如下:
回答下列问题:
(1)A中所含官能团的名称为
 的名称
的名称(2)
 的反应类型为
的反应类型为 中碳原子的杂化类型为
中碳原子的杂化类型为(3)B与C在水中溶解度较大的是
(4)写出
 的化学方程式
的化学方程式(5)B的同分异构体中,满足下列条件的结构有
 的结构简式为
的结构简式为条件:①含有苯环;②与
 溶液发生显色反应;③含有2个甲基,且连在同一个碳原子上。
溶液发生显色反应;③含有2个甲基,且连在同一个碳原子上。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。回答下列问题:
(1)基态Fe3+的电子排布式为___________ ;实验室用KSCN溶液、苯酚(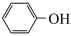 )检验Fe3+,N、O、S的第一电离能由大到小的顺序为
)检验Fe3+,N、O、S的第一电离能由大到小的顺序为___________ (用元素符号表示)。
(2)基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等,1mol Fe(CO)5分子中含σ键数目为___________ ,与CO互为等电子体的离子是___________ (填化学式,写一种)
(3)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为___________ 。

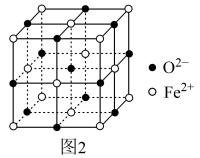
(4)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为___________ ;Fe2+与O2-的最短间距为___________ pm。
(1)基态Fe3+的电子排布式为
 )检验Fe3+,N、O、S的第一电离能由大到小的顺序为
)检验Fe3+,N、O、S的第一电离能由大到小的顺序为(2)基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等,1mol Fe(CO)5分子中含σ键数目为
(3)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为

(4)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】碳元素在无机物和有机物中均充当了重要的角色,请回答下列问题:
(1)基态碳原子的价层电子排布图(轨道表达式)为__ ,其电子占据的能量最高的原子轨道的形状为__ ;C、N、O三种元素第一电离能最大的是__ 。
(2)有机物 中碳原子的轨道杂化类型为
中碳原子的轨道杂化类型为__ ,分子中两种碳碳单键长的大小关系为①__ ②(填“>”、“<”或“=”)。
(3) 和
和 均可以形成氢键,则沸点较高的是
均可以形成氢键,则沸点较高的是__ ,原因是__ 。
(4)石墨的结构及晶胞如图一所示,则石墨的密度为__ g·cm-3(用含a、d、NA的表达式表示)。A的原子坐标为( 、
、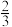 、0),则B的原子坐标为
、0),则B的原子坐标为__ 。

(5)石墨能与熔融的金属K作用,形成一种青铜色的化合物CxK,如图二所示,则x=__ 。
(1)基态碳原子的价层电子排布图(轨道表达式)为
(2)有机物
 中碳原子的轨道杂化类型为
中碳原子的轨道杂化类型为(3)
 和
和 均可以形成氢键,则沸点较高的是
均可以形成氢键,则沸点较高的是(4)石墨的结构及晶胞如图一所示,则石墨的密度为
 、
、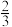 、0),则B的原子坐标为
、0),则B的原子坐标为
(5)石墨能与熔融的金属K作用,形成一种青铜色的化合物CxK,如图二所示,则x=
您最近一年使用:0次
【推荐3】2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH2=CH2)与四氯乙烯(CF2=CF2)的共聚物(ETFE)制成。回答下列问题:
(1)F原子最外层轨道表示式为_______ 。
(2)图a、b、c分别表示C、N、O和F的气态原子逐级失去电子所需能量(纵坐标的标度不同)。失去最外层的一个电子所需能量的变化图是_______ (填标号),判断的根据是_______ ,失去三个电子的变化图是_______ (填标号)。

(3)上图四种元素中,原子核外s亚层电子数与p亚层电子数相同的元素在周期表中的位置是_______ ,其形成的氢化物的沸点_______ H2S的沸点(填>、<或=),理由是_______ 。
(4)聚四氯乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
(5)FTFE_______ (填“有”、“没有”)固定熔沸点,其结构简式为:_______ 。
(1)F原子最外层轨道表示式为
(2)图a、b、c分别表示C、N、O和F的气态原子逐级失去电子所需能量(纵坐标的标度不同)。失去最外层的一个电子所需能量的变化图是

(3)上图四种元素中,原子核外s亚层电子数与p亚层电子数相同的元素在周期表中的位置是
(4)聚四氯乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因
(5)FTFE
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】氮化物应用广泛,如叠氮化钠(NaN3)是典型的高能量密度含能材料,氮化硼是特殊的耐磨和切削材料,氮化铬、氮化钼等过渡金属氮化物常用作高强度材料。回答下列问题:
(1)Na、N、B中,电负性由大到小的顺序是__ 。
(2)基态N原子的价电子排布式为___ 。基态铬原子核外未成对电子数为______ 。
(3)NaN3中阴离子N 是直线型离子。4.2gN
是直线型离子。4.2gN 中的σ键数目为
中的σ键数目为__ 。分子或离子中的大π键可用符号Π 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π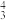 ),则N
),则N 中的大π键应表示为
中的大π键应表示为__ 。
(4)石墨型(BN)x转变为金刚石型(BN)x时,B原子的杂化轨道类型由_____ 变为__ 。推测金刚石型(BN)x的硬度比金刚石的硬度__ (填“大”或“小”)。
(5)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示。
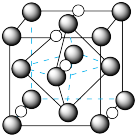
氮化钼的化学式为_____ ,如果让Li+填入氮化钼晶体的八面体空隙,一个晶胞最多可以填入_____ 个Li+。氮化钼晶胞边长为anm,晶体的密度ρ=___ g·cm-3(列出计算式,设NA为阿伏加德罗常数的值)。
(1)Na、N、B中,电负性由大到小的顺序是
(2)基态N原子的价电子排布式为
(3)NaN3中阴离子N
 是直线型离子。4.2gN
是直线型离子。4.2gN 中的σ键数目为
中的σ键数目为 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如CO2分子中存在两个大π键Π ),则N
),则N 中的大π键应表示为
中的大π键应表示为(4)石墨型(BN)x转变为金刚石型(BN)x时,B原子的杂化轨道类型由
(5)氮化钼作为锂离子电池负极材料具有很好的发展前景。它属于填隙式氮化物,N原子部分填充在Mo原子立方晶格的八面体空隙中,晶胞结构如图所示。

氮化钼的化学式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】黄铜矿是主要的炼铜原料,CuFeS2是其中铜的主要存在形式。回答下列问题:
(1)CuFeS2中存在的化学键类型是_______ 。其组成的三种元素中电负性较强的是 _______ 。
(2)下列基态原子或离子的价层电子排布图正确的______ 。

(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是____ ,中心原子杂化类型为____ ,属于_______ (填“极性”或“非极性”)分子。
②X的沸点比水低的主要原因是___________ 。
(4)CuFeS2与氧气反应生成SO2,其结构式为 ,则SO2中共价键类型有
,则SO2中共价键类型有_________ 。
(5)四方晶系CuFeS2晶胞结构如图所示。

①Cu+的配位数为__________ ,
②已知:a=b=0.524 nm,c=1.032 nm,NA为阿伏加 德罗常数的值,CuFeS2晶体的密度是________ g•cm3(列出计算式)。
(1)CuFeS2中存在的化学键类型是
(2)下列基态原子或离子的价层电子排布图正确的

(3)在较低温度下CuFeS2与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的立体构型是
②X的沸点比水低的主要原因是
(4)CuFeS2与氧气反应生成SO2,其结构式为
 ,则SO2中共价键类型有
,则SO2中共价键类型有(5)四方晶系CuFeS2晶胞结构如图所示。

①Cu+的配位数为
②已知:a=b=0.524 nm,c=1.032 nm,NA为阿伏加 德罗常数的值,CuFeS2晶体的密度是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】Ⅰ.SiC、BN、GaAs 等是人工合成半导体的材料,具有高频、大功率和抗辐射等优点。请回答:
(1)Ga的第一电离能失去的是___________ 能级的电子。
(2)B、C、N的电负性由大到小排列为___________ 。
Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(3)拟卤素(CN)2、(SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足8 电子结构。(SCN)2对应的酸有两种,测得硫氰酸(H—S—C≡N )的沸点低于异硫氰酸(H-N=C=S),其原因是___________ 。
(4)卤化物 RbICl2 在加热时会分解为晶格能相对较大的卤化物 A 和卤素互化物或卤素单质,A 的化学式为___________ ;I 属于多卤素阳离子,其空间构型为
属于多卤素阳离子,其空间构型为___________ 。
(5)卤素互化物如IBr、ICl等与卤素单质结构和性质相似。Cl2、IBr、ICl沸点由高到低的顺序为___________ 。
(6)请推测①HClO4、②HIO4、③H5IO6[可写成(HO)5IO]三种物质的酸性由强到弱的顺序为___________ (填序号)。
III.金属铁是生活中最常见的金属,其晶胞为体心立方堆积。
(7)其晶胞的俯视图为____ (填字母序号)。
(8)若铁的密度为a g/cm3,则铁晶胞中最近的两个铁原子的核间距离是____ pm(列表达式即可)。
(1)Ga的第一电离能失去的是
(2)B、C、N的电负性由大到小排列为
Ⅱ.卤素化学丰富多彩,能形成卤化物、卤素互化物、多卤化物等多种类型的化合物。
(3)拟卤素(CN)2、(SCN)2与卤素单质结构相似、性质相近,分子中所有原子都满足8 电子结构。(SCN)2对应的酸有两种,测得硫氰酸(H—S—C≡N )的沸点低于异硫氰酸(H-N=C=S),其原因是
(4)卤化物 RbICl2 在加热时会分解为晶格能相对较大的卤化物 A 和卤素互化物或卤素单质,A 的化学式为
 属于多卤素阳离子,其空间构型为
属于多卤素阳离子,其空间构型为(5)卤素互化物如IBr、ICl等与卤素单质结构和性质相似。Cl2、IBr、ICl沸点由高到低的顺序为
(6)请推测①HClO4、②HIO4、③H5IO6[可写成(HO)5IO]三种物质的酸性由强到弱的顺序为
III.金属铁是生活中最常见的金属,其晶胞为体心立方堆积。
(7)其晶胞的俯视图为____ (填字母序号)。
A. | B. | C.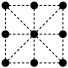 | D. |
您最近一年使用:0次



