下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将 气体通入 气体通入 溶液,出现黑色沉淀 溶液,出现黑色沉淀 |  不溶于稀硫酸 不溶于稀硫酸 |
| B | 取 乙醇,加入 乙醇,加入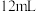 浓硫酸及少量沸石,迅速升温至 浓硫酸及少量沸石,迅速升温至 ,将产生的气体通过溴水,溴水褪色 ,将产生的气体通过溴水,溴水褪色 | 产物中有乙烯 |
| C | 向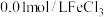 溶液中加入少量 溶液中加入少量 固体,溶液颜色加深 固体,溶液颜色加深 |  水解程度增大 水解程度增大 |
| D | 向硫酸铜溶液中逐滴滴加浓氨水,先产生蓝色沉淀,而后沉淀逐渐溶解 |  是两性氢氧化物 是两性氢氧化物 |
| A.A | B.B | C.C | D.D |
更新时间:2023-09-10 13:04:23
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列实验中,对应的现象以及结论都正确且两者具有因果关系的是
选项 | 实验 | 现象 | 结论 |
A | 将FeCl3溶液加入Mg(OH)2悬浊液中 | 观察到沉淀由白色变为红褐色 | Fe(OH)3的溶解度大于Mg(OH)2 |
B | 向某溶液中滴加BaCl2溶液,随后加稀硝酸酸化 | 溶液中产生白色沉淀,加稀硝酸不溶解 | 原溶液中一定含有SO42- |
C | 将稀硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中 | 溶液变黄色 | 氧化性:H2O2比Fe3+强 |
D | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体 | 溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温时,下列关于 溶液的说法正确的是
溶液的说法正确的是
 溶液的说法正确的是
溶液的说法正确的是A.溶液中存在电离平衡:  ⇌NH ⇌NH +Cl- +Cl- |
| B.加水稀释,溶液中所有离子的浓度均减小 |
C.通入少量 气体, 气体, 与 与 均增大 均增大 |
D.通入少量 气体, 气体,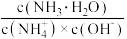 增大 增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列实验方案中,能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 检验CH3CH2Br与NaOH溶液是否发生反应 | 将CH3CH2Br与NaOH溶液共热,冷却,取上层溶液,加AgNO3溶液,观察是否产生淡黄色沉淀 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变成红色 |
| C | 验证氧化性:Fe3+>I2 | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置,观察下层液体是否变成紫色 |
| D | 检验乙醇与浓硫酸共热是否产生乙烯 | 将乙醇与浓硫酸共热至170 ℃,所得气体通入酸性高锰酸钾溶液中,观察溶液是否褪色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验方案﹑实验现象和结论都正确的是
| 选项 | 实验方案 | 实验现象 | 结论 |
| A | 无水乙醇与浓硫酸共热至170℃,将产生的气体直接通入酸性高锰酸钾溶液中 | 酸性高锰酸钾溶液褪色 | 乙烯可被酸性高锰酸钾溶液氧化 |
| B | 向0.1  溶液中加入 溶液中加入 | 产生淡黄色沉淀 |  可将 可将 氧化为S 氧化为S |
| C | 向浓度均为0.1 的 的 、 、 混合溶液中逐滴加入氨水 混合溶液中逐滴加入氨水 | 先出现蓝色沉淀 | 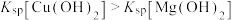 |
| D | 向蔗糖溶液中滴加稀硫酸,水浴加热后直接加入几滴新制 ,继续水浴加热 ,继续水浴加热 | 无砖红色沉淀产生 | 蔗糖未发生水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列图示的实验操作,不能实现相应实验目的的是
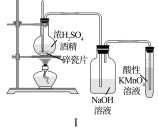




| A.图I:制备乙烯并验证乙烯的还原性 |
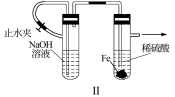
| B.图II:制备少量的Fe(OH)2 |
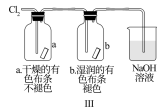
| C.图III:探究氯气是否具有漂白性 |
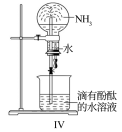
| D.图IV:探究氨气在水的溶解性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】实验:①将少量白色 固体溶于水,得到蓝色溶液;将少量
固体溶于水,得到蓝色溶液;将少量 固体溶于水,得到无色溶液;
固体溶于水,得到无色溶液;
②向蓝色溶液滴加氨水,首先形成难溶物,继续添加氨水并振荡试管,难溶物溶解,得到深蓝色透明溶液;
③向深蓝色透明溶液加入乙醇,析出深蓝色晶体。
下列分析不正确 的是
 固体溶于水,得到蓝色溶液;将少量
固体溶于水,得到蓝色溶液;将少量 固体溶于水,得到无色溶液;
固体溶于水,得到无色溶液;②向蓝色溶液滴加氨水,首先形成难溶物,继续添加氨水并振荡试管,难溶物溶解,得到深蓝色透明溶液;
③向深蓝色透明溶液加入乙醇,析出深蓝色晶体。
下列分析
A.①中蓝色溶液中呈蓝色的物质是 离子 离子 |
B.②中形成难溶物的反应为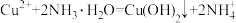 |
C.②中难溶物溶解的反应为 |
D.③中加入乙醇后析出的深蓝色晶体是 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】近年来,光催化剂的研究是材料领域的热点方向。一种Ru配合物(如图所示)复合光催化剂可将CO2转化为HCOOH下列说法错误 的是
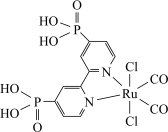

| A.合成Ru配合物的原料H3PO4中中心原子P的价层电子对为4 |
B.吡啶(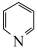 )中C、N原子的杂化方式分别为sp2、sp3 )中C、N原子的杂化方式分别为sp2、sp3 |
| C.该配合物中Ru的配位数是6 |
| D.HCOOH的沸点比CH3CHO高,主要原因是HCOOH分子间存在范德华力和氢键,而CH3CHO分子间只有范德华力 |
您最近一年使用:0次

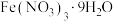 晶体进行如下实验:
晶体进行如下实验: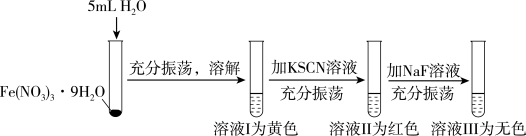
 为浅紫色,
为浅紫色, 为红色,
为红色, 为无色。
为无色。 所致
所致 中碳元素的化合价为
中碳元素的化合价为 价
价 强于
强于

