辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2)。一种以辉铜矿石为原料制备硝酸铜的工艺流程如图所示:

(1)“回收S”过程中温度控制在50~60 ℃之间,不宜过高或过低的原因是_______ 。
(2)“保温除铁”过程中,加入CuO的目的是_______ ;“蒸发浓缩、冷却结晶”过程中,要用HNO3溶液调节溶液的pH,其理由是_______ 。

(1)“回收S”过程中温度控制在50~60 ℃之间,不宜过高或过低的原因是
(2)“保温除铁”过程中,加入CuO的目的是
2023高三·全国·专题练习 查看更多[1]
(已下线)微专题 无机化工流程题的解题策略
更新时间:2023-11-03 09:42:36
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】我国某地粉煤灰中主要含有Al2O3,除此之外还含有Ga2O3及少量Fe2O3、CaO、MgO和SiO2等物质。已知从粉煤灰中回收铝并提取镓的工艺流程如下所示:
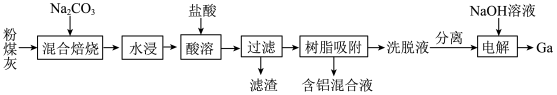
回答下列问题:
(1)焙烧前,应将粉煤灰与纯碱粉末充分混合,其原因是____ ;混合焙烧时,Al2O3、Ga2O3均发生类似于SiO2的反应,试写出Ga2O3在此过程中发生反应的化学方程式:____ 。
(2)滤渣的成分是____ ;含铝混合液中除了大量A13+之外,还有Fe3+和少量Mg2+,由混合液制取纯净Al(OH)3的实验方案是_____ 。
(3)洗脱液中往往还有少量Fe3+,需要进一步分离。若使Fe3+恰好完全沉淀[c(Fe3+)= l×l0-5mol·L-l]时,Ga3+浓度至少为_____ mol·L-l才会开始沉淀。(已知: 。)
。)
(4)电解过程中,Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电,则电解方程式为____ ;电解过程中需要保持溶液为pH=11以上的原因是 ___ 。

回答下列问题:
(1)焙烧前,应将粉煤灰与纯碱粉末充分混合,其原因是
(2)滤渣的成分是
(3)洗脱液中往往还有少量Fe3+,需要进一步分离。若使Fe3+恰好完全沉淀[c(Fe3+)= l×l0-5mol·L-l]时,Ga3+浓度至少为
 。)
。)(4)电解过程中,Ga3+与NaOH溶液反应生成GaO2-,GaO2-在阴极放电,则电解方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】含锌废渣及粉尘是危险废物,碱浸电解法处理可得锌粉。但若其中存在氯,则锌质量就严重下降,对电极板也有严重腐蚀作用。工业上模拟碱浸电解法处理含锌质量分数为16%的废料(主要成分为ZnO、Zn(OH)2、ZnSO4及PbCO3、Fe2O3、Cu杂质)工艺如图:

ⅰ.浸出液中含有[Zn(OH)4]2-和[Pb(OH)4]2-等离子
ⅱ.滤渣Ⅱ的主要成分为:Na2Pb(OH)xS
(1)从物质分类的角度看,ZnO属于__ ,其与NaOH溶液发生反应的离子方程式为__ 。
(2)“滤渣Ⅰ”的主要成分为___ 。
(3)下表是“预处理”的2种除氯方案中粉尘氯的去除率和锌损失率分析表格可知,首选的“除氯剂”为___ ,原因是____ 。
(4)“电解”过程中阴极的电极反应式为____ 。
(5)锌的总回收率为____ 。

ⅰ.浸出液中含有[Zn(OH)4]2-和[Pb(OH)4]2-等离子
ⅱ.滤渣Ⅱ的主要成分为:Na2Pb(OH)xS

(1)从物质分类的角度看,ZnO属于
(2)“滤渣Ⅰ”的主要成分为
(3)下表是“预处理”的2种除氯方案中粉尘氯的去除率和锌损失率分析表格可知,首选的“除氯剂”为
| 除氯剂 | 碱(NaOH) | 碳酸钠 |
| 氯去除率/% | 78.75 | 83.69 |
| 锌损失率/% | 0.26 | 0.28 |
| 价格/t | 7200元 | 3600元 |
(4)“电解”过程中阴极的电极反应式为
(5)锌的总回收率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上用磷铁渣(主要含FeP、Fe2P,以及少量Fe2O3、SiO2等杂质)制备FePO4(磷酸铁)。

已知:FePO4难溶于水,能溶于无机强酸。
(1)“浸取”时磷铁渣粉碎并搅拌目的是_______ ;加入硫酸的目的是_______ 。
(2)“浸取”时Fe2P发生反应的离子方程式为_______ 。
(3)滤渣的主要成分是_______ ,制备操作中需要适当加热,但温度不宜过高的原因是_______ 。
(4)“制备”过程中溶液的pH对磷酸铁产品中铁和磷的含量及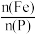 比值的影响如图所示[考虑到微量金属杂质,在pH=1时,
比值的影响如图所示[考虑到微量金属杂质,在pH=1时,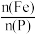 为0.973最接近理论值。]
为0.973最接近理论值。]

在pH范围为1~1.5时,随pH增大,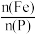 明显增大,其原因是
明显增大,其原因是_______ 。
(5)工业上也可以用电解磷铁渣的方法制备FePO4。

①FeP在阳极放电的电极反应式为_______ 。
②常温电解一段时间,测得溶液中Fe3+浓度约为0.32mol•L-1,为了避免生成Fe(OH)3沉淀,应控制溶液的pH不大于_______ (已知:Ksp[Fe(OH)3]=4×10-38,lg2=0.3)。

已知:FePO4难溶于水,能溶于无机强酸。
(1)“浸取”时磷铁渣粉碎并搅拌目的是
(2)“浸取”时Fe2P发生反应的离子方程式为
(3)滤渣的主要成分是
(4)“制备”过程中溶液的pH对磷酸铁产品中铁和磷的含量及
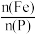 比值的影响如图所示[考虑到微量金属杂质,在pH=1时,
比值的影响如图所示[考虑到微量金属杂质,在pH=1时,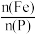 为0.973最接近理论值。]
为0.973最接近理论值。]
在pH范围为1~1.5时,随pH增大,
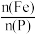 明显增大,其原因是
明显增大,其原因是(5)工业上也可以用电解磷铁渣的方法制备FePO4。

①FeP在阳极放电的电极反应式为
②常温电解一段时间,测得溶液中Fe3+浓度约为0.32mol•L-1,为了避免生成Fe(OH)3沉淀,应控制溶液的pH不大于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】为除去粗盐中的Ca2+、Mg2+、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:(用于沉淀的试剂稍过量)
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:(用于沉淀的试剂稍过量)

(1)第①步中,操作A是________ ,第⑤步中,操作B是________ 。
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)_____________ 。
(3)该方案一共用到了____ 次玻璃棒,在第①步中玻璃棒的作用是__________ 。
(4)判断BaCl2已过量的方法是___________ 。
(5)在第③步操作中,选择除杂试剂不能用KOH代替NaOH,理由是_________ 。
(6)在第⑤步操作B中,得到的沉淀成分有泥沙、BaSO4、Mg(OH)2、___________ 。
(7)该实验方案用到的器材有铁架台(带铁圈)、坩埚钳、石棉网、火柴、________ 。
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:(用于沉淀的试剂稍过量)
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:(用于沉淀的试剂稍过量)
(1)第①步中,操作A是
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
(3)该方案一共用到了
(4)判断BaCl2已过量的方法是
(5)在第③步操作中,选择除杂试剂不能用KOH代替NaOH,理由是
(6)在第⑤步操作B中,得到的沉淀成分有泥沙、BaSO4、Mg(OH)2、
(7)该实验方案用到的器材有铁架台(带铁圈)、坩埚钳、石棉网、火柴、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】闪锌矿主要成分为ZnS,含少量FeS、CuS、CdS杂质。软锰矿的主要成分为 MnO2;含少量A12O3和SiO2。现以闪锌矿和软猛矿为原料制备Zn和MnO2,其简化流程如下(中间产物的固体部分已经略去)。
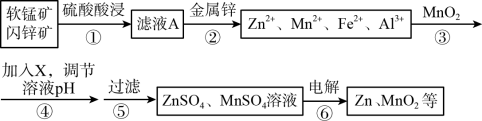
已知:I.矿石中所有金属元素在滤液中均以离子形式存在。
Ⅱ.各种金属离子完全沉淀的pH如下表:
回答下列问题:
(1)步骤①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式________________________________ 。
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是_______________ 。
(3)步骤③与MnO2发生氧化还原反应的离子方程式_________________ ,物质X可以是__________ (用字母表示。
A.Cu2(OH)2CO3 B.MnCO3 C. MgO D.Zn(OH)2
(4)流程中可以循环利用的物质是____________ (填化学式)。
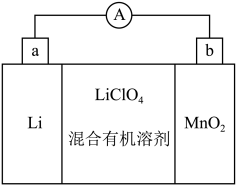
(5)MnO2与Li构成LiMnO2,该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。回答下列问题:
①外电路中的电子移动方向是由______ 极流向______ 极(填字母)。
②写出该锂离子电池的正极电极反应式_____________________________ 。
(6)已知:25℃时,HCN的电离常数K=4.9×10-10, H2S的电离常数K1=1.3×10-7,K2=7.0 ×10 -15,向NaCN溶液中通入少量的H2S气体,该反应的化学方程式为______________________ 。

已知:I.矿石中所有金属元素在滤液中均以离子形式存在。
Ⅱ.各种金属离子完全沉淀的pH如下表:
Zn2+ | Mn2+ | Fe2+ | Fe,3+ | Al3+ | |
pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
回答下列问题:
(1)步骤①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是
(3)步骤③与MnO2发生氧化还原反应的离子方程式
A.Cu2(OH)2CO3 B.MnCO3 C. MgO D.Zn(OH)2
(4)流程中可以循环利用的物质是
(5)MnO2与Li构成LiMnO2,该电池反应原理如图所示,其中电解质LiClO4,溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。回答下列问题:
①外电路中的电子移动方向是由
②写出该锂离子电池的正极电极反应式
(6)已知:25℃时,HCN的电离常数K=4.9×10-10, H2S的电离常数K1=1.3×10-7,K2=7.0 ×10 -15,向NaCN溶液中通入少量的H2S气体,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】 (钴酸锂)是锂离子电池的正极材料。以某海水(含浓度较大的LiCl,含少量
(钴酸锂)是锂离子电池的正极材料。以某海水(含浓度较大的LiCl,含少量 、
、 、
、 等)为原料制备钴酸锂的一种流程如下:
等)为原料制备钴酸锂的一种流程如下:

已知:①碳酸锂的溶解度随温度升高而降低
②常温下,几种难溶物质的溶度积数据如下:
回答下列问题:
(1)滤渣1主要成分有 、
、 和
和___________ (填化学式)。
(2)调 的目的是
的目的是___________ 。
(3)“除杂2”中调 时
时
___________  。
。
(4)“洗涤” 时最好选用
时最好选用___________ (填“冷水”或“热水”)。
(5)写出高温时“合成”反应的化学方程式:___________ 。
(6)流程中可以循环利用的物质有___________ (填化学式)。
 (钴酸锂)是锂离子电池的正极材料。以某海水(含浓度较大的LiCl,含少量
(钴酸锂)是锂离子电池的正极材料。以某海水(含浓度较大的LiCl,含少量 、
、 、
、 等)为原料制备钴酸锂的一种流程如下:
等)为原料制备钴酸锂的一种流程如下:
已知:①碳酸锂的溶解度随温度升高而降低
②常温下,几种难溶物质的溶度积数据如下:
| 物质 |  |  |  |  |  |
 | 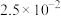 | 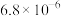 | 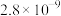 | 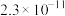 |  |
回答下列问题:
(1)滤渣1主要成分有
 、
、 和
和(2)调
 的目的是
的目的是(3)“除杂2”中调
 时
时
 。
。(4)“洗涤”
 时最好选用
时最好选用(5)写出高温时“合成”反应的化学方程式:
(6)流程中可以循环利用的物质有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氯化钠是生活必需品,也是重要的化工原料。提纯含少量泥沙的粗盐,一般经过如图操作流程:
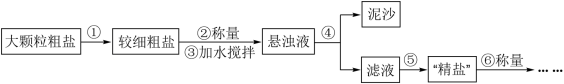
(1)操作①中必须用到的一种仪器是_______ (填字母)。
A.研钵 B.量筒 C.烧杯 D.试管
(2)操作⑤中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到的仪器是_______ 。
(3)粗盐提纯后的精盐含有氯化钙、氯化镁、硫酸钠等可溶性杂质,常通过加入化学试剂使其转化为沉淀而除去。
a.除去氯化镁加入的试剂是_______ ,反应的化学方程式是_______ 。
b.除去硫酸钠加入的试剂是_______ ,反应的化学方程式是_______ 。
c.在滤液中加盐酸的作用是_______ 、_______ (用离子方程式表示)。

(1)操作①中必须用到的一种仪器是
A.研钵 B.量筒 C.烧杯 D.试管
(2)操作⑤中除用到铁架台(带铁圈)、酒精灯、玻璃棒、坩埚钳外,还需要用到的仪器是
(3)粗盐提纯后的精盐含有氯化钙、氯化镁、硫酸钠等可溶性杂质,常通过加入化学试剂使其转化为沉淀而除去。
a.除去氯化镁加入的试剂是
b.除去硫酸钠加入的试剂是
c.在滤液中加盐酸的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】粗盐中常含有少量的泥沙及氯化钙、氯化镁、硫酸盐等一些可溶性的杂质。粗盐的提纯实验操作步骤如图所示:

(1)请写出图中各步实验操作的名称②_____ ,③______ 。
(2)实验操作②的主要目的是______ 。
(3)实验操作①②③中都使用的仪器是_____ ,它在③中其作用是_____ 。
(4)通过上述实验操作,得到的精盐中可能含有的杂质是____ 。

(1)请写出图中各步实验操作的名称②
(2)实验操作②的主要目的是
(3)实验操作①②③中都使用的仪器是
(4)通过上述实验操作,得到的精盐中可能含有的杂质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】钛有强度高和质地轻的优点,广泛应用于飞机制造业等。工业上利用钛铁矿,其主要成分为钛酸亚铁(FeTiO3)制备钛金属,工业流程如下:(已知: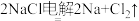 )
)

(1)请写出FeTiO3与稀盐酸反应的离子方程式:________________ 。
(2)请写出“熔融氧化”的化学方程式:_______________________ 。
(3)补充写出实现上述方框内过程A所需的实验操作:___________ 、__________ 过滤、洗涤、在干燥的HCl气流中加热→FeCl2固体
(4)热还原法中能否改用钠代替镁作还原剂:_____________ (填“能”或“不能”);
(5)上流程中可循环利用的物质为:____________________ (填化学式)。
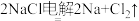 )
)
(1)请写出FeTiO3与稀盐酸反应的离子方程式:
(2)请写出“熔融氧化”的化学方程式:
(3)补充写出实现上述方框内过程A所需的实验操作:
(4)热还原法中能否改用钠代替镁作还原剂:
(5)上流程中可循环利用的物质为:
您最近一年使用:0次



