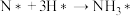某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
下列说法正确的是
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/L KMnO4溶液 | 3 mol/L 某酸a溶液 | ||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | b | 1.0 | 2.0 | 6.4 |
A.反应原理用离子方程式可表示为:2MnO +5C2O +5C2O +16H+=2Mn2++10CO2↑+8H2O +16H+=2Mn2++10CO2↑+8H2O |
| B.酸a可以是硫酸也可以是盐酸或者硝酸 |
| C.b=4.0 |
| D.利用实验1可以计算得到v(H2C2O4)=0.125mol/(L·min) |
更新时间:2023-10-26 08:50:10
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】铬元素(Cr)的化合物存在下列转化关系:
Cr2O3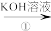 KCrO2(绿色)
KCrO2(绿色)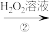 K2CrO4(黄色)
K2CrO4(黄色)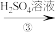 K2Cr2O7(橙红色)
K2Cr2O7(橙红色)
下列判断错误的是
Cr2O3
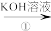 KCrO2(绿色)
KCrO2(绿色)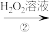 K2CrO4(黄色)
K2CrO4(黄色)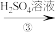 K2Cr2O7(橙红色)
K2Cr2O7(橙红色) 下列判断错误的是
| A.反应①表明Cr2O3具有酸性氧化物的性质 |
| B.反应②H2O2被氧化成O2 |
| C.反应③发生的反应为2K2CrO4+H2SO4=K2Cr2O7+K2SO4+H2O |
| D.反应①②③中只有②是氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】通常利用反应:KClO3+HCl(浓)→KCl+Cl2+H2O(未配平),关于该反应的下列说法中,不正确的是
A.ClO  被还原 被还原 |
| B.每消耗 1molKClO₃, 转移 6mole⁻ |
| C.KClO₃和 HCl 的物质的量之比为1∶6 |
| D.在该反应的条件下,氧化性:KClO3>Cl2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用如下方法回收废旧CPU中的单质Au(金)、Ag和Cu
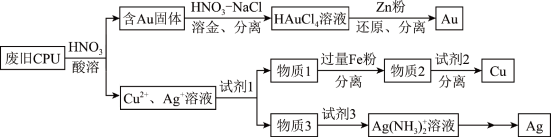
已知:浓硝酸不能单独将Au溶解,通常采用王水[V(浓硝酸):V(浓盐酸)=1∶3]溶解Au。
下列说法不正确 的是

已知:浓硝酸不能单独将Au溶解,通常采用王水[V(浓硝酸):V(浓盐酸)=1∶3]溶解Au。
下列说法
A.浓、稀 均可作酸溶试剂,溶解等量的Cu,选择稀硝酸可节约原料 均可作酸溶试剂,溶解等量的Cu,选择稀硝酸可节约原料 |
B.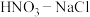 与王水溶金原理相同,反应原理可以表示为: 与王水溶金原理相同,反应原理可以表示为: |
C.用王水溶金时,利用了 的氧化性,浓盐酸的主要作用是增强溶液的酸性 的氧化性,浓盐酸的主要作用是增强溶液的酸性 |
| D.用适当浓度的盐酸、氯化钠溶液、氨水和铁粉可从酸溶后的溶液中回收Cu和Ag,试剂1应选择NaCl溶液 |
您最近一年使用:0次
单选题
|
适中
(0.64)
【推荐1】下列说法不正确的是
| A.任何化学反应都伴随着能量变化 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.离子化合物中一定含有离子键,可能含有共价键 |
| D.强电解质与弱电解质的区别就是电解质在水溶液中是否完全电离 |
您最近一年使用:0次
单选题
|
适中
(0.65)
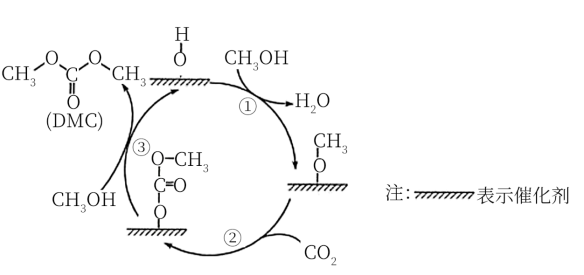
【推荐2】科研人员提出120℃下 催化合成
催化合成 (碳酸二甲酯)需经历三步反应,示意图如图。下列说法正确的是
(碳酸二甲酯)需经历三步反应,示意图如图。下列说法正确的是
 催化合成
催化合成 (碳酸二甲酯)需经历三步反应,示意图如图。下列说法正确的是
(碳酸二甲酯)需经历三步反应,示意图如图。下列说法正确的是
A. 与过量稀 与过量稀 溶液完全反应生成 溶液完全反应生成 和甲醇 和甲醇 |
B.改用更高效的催化剂,可提高 的平衡产率 的平衡产率 |
| C.反应历程①②③中,活化能越高,反应速率越慢 |
| D.向反应体系中加入少量水蒸气,反应物的平衡转化率升高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】把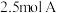 和
和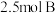 混合盛入容积为
混合盛入容积为 的密闭容器里,发生如下反应
的密闭容器里,发生如下反应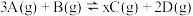 ,经
,经 反应达平衡,在此
反应达平衡,在此 内C的平均反应速率为
内C的平均反应速率为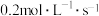 ,同时生成
,同时生成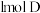 ,下列叙述中
,下列叙述中不正确 的是
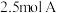 和
和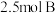 混合盛入容积为
混合盛入容积为 的密闭容器里,发生如下反应
的密闭容器里,发生如下反应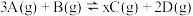 ,经
,经 反应达平衡,在此
反应达平衡,在此 内C的平均反应速率为
内C的平均反应速率为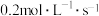 ,同时生成
,同时生成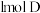 ,下列叙述中
,下列叙述中A. |
B. 内B的反应速率 内B的反应速率 |
| C.当混合气体的平均相对分子质量不再改变时,该反应已达到平衡状态 |
D.当 时,标志着该反应达到平衡状态 时,标志着该反应达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】为验证次氯酸光照分解的产物,某同学采用三种传感器分别测得氯水光照过程中pH、 浓度、
浓度、 体积分数的变化,实验数据如图所示。
体积分数的变化,实验数据如图所示。

已知:①
②用 来表示的化学反应速率
来表示的化学反应速率 。
。
下列叙述错误的是
 浓度、
浓度、 体积分数的变化,实验数据如图所示。
体积分数的变化,实验数据如图所示。
已知:①

②用
 来表示的化学反应速率
来表示的化学反应速率 。
。下列叙述错误的是
| A.从0s到150s,溶液pH降低的原因是HClO的电离程度增大 |
B.从0s到150s,溶液的 增加到起始浓度的 增加到起始浓度的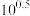 倍 倍 |
C.从50s到150s, 的平均生成速率约为 的平均生成速率约为 |
D.光照后, 会分解为 会分解为 和 和 ,且溶液的导电能力会增强 ,且溶液的导电能力会增强 |
您最近一年使用:0次

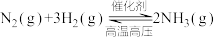 。该反应的能量变化及微观历程的示意图如下所示(*表示物质吸附在催化剂表面的形态)。下列说法不正确的是
。该反应的能量变化及微观历程的示意图如下所示(*表示物质吸附在催化剂表面的形态)。下列说法不正确的是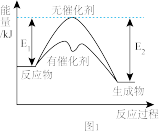
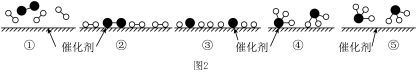
 的断裂,不存在
的断裂,不存在