 是一种常见的氧化剂,广泛用于生活中作消毒剂。某小组设计实验探究
是一种常见的氧化剂,广泛用于生活中作消毒剂。某小组设计实验探究 的氧化能力与介质pH的关系(已知
的氧化能力与介质pH的关系(已知 溶液呈绿色,酸性条件下发生歧化反应生成
溶液呈绿色,酸性条件下发生歧化反应生成 和
和 )。
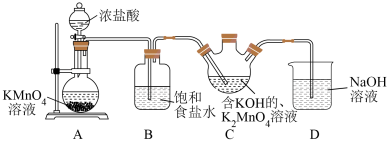
)。
请回答下列问题:
(1)装置A中盛放
 溶液的仪器名称为
溶液的仪器名称为(2)装置A中浓盐酸在反应中表现出来的性质是
(3)由实验推知,A中氧化性:

 ;若装置C中绿色溶液变为紫红色,
;若装置C中绿色溶液变为紫红色, 的氧化性强于
的氧化性强于 。
。(4)有关高锰酸钾的实验及现象如表所示。
| 实验 | 装置 | 试剂R(5 mL含0.1 mol·L  的溶液) 的溶液) | 现象(通入乙烯的体积相等) |
| Ⅰ | 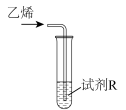 |  溶液 溶液 | 较快产生黑色沉淀 |
| Ⅱ | KOH和 溶液 溶液 | 紫红色溶液较慢变为绿色溶液 | |
| Ⅲ | 稀硫酸和 溶液 溶液 | 紫红色溶液很快变为无色溶液 |
 ,则实验Ⅰ中发生反应的离子方程式为
,则实验Ⅰ中发生反应的离子方程式为②实验结论:其他条件相同,介质pH越低,
 氧化性越
氧化性越
更新时间:2023-10-27 19:30:02
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。
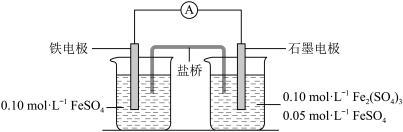
回答下列问题:
(1)由FeSO4·7H2O固体配制0.10 mol/LFeSO4溶液,需要的仪器有药匙、玻璃棒、_______ (填序号)。
A. B.
B.  C.
C. 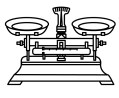 D.
D. 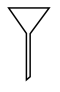 E.
E.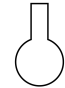
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择___________ (物质化学式)作为电解质。
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入___________ 电极溶液中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+ )增加了0.02 mol/L。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=___________ 。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为___________ ,铁电极的电极反应式为___________ 。因此,验证了Fe2+氧化性小于___________ ,还原性小于___________ 。
(6)实验前需要对铁电极表面活化。在FeSO4 溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是___________ 。

回答下列问题:
(1)由FeSO4·7H2O固体配制0.10 mol/LFeSO4溶液,需要的仪器有药匙、玻璃棒、
A.
 B.
B.  C.
C.  D.
D.  E.
E.
(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择
| 阳离子 | u∞×108/(m2·s-1·v-1) | 阴离子 | u∞×108/(m2·s-1·v-1) |
| Li+ | 4.07. |  | 4.61 |
| Na+ | 5.19 |  | 7.40 |
| Ca2+ | 6.59 | Cl- | 7.91 |
| K+ | 7.62 |  | 8.27 |
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+ )增加了0.02 mol/L。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为
(6)实验前需要对铁电极表面活化。在FeSO4 溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用如图装置(部分装置省略)制备KClO3和NaClO,探究其氧化还原性质。

回答下列问题:
(1)该实验装置制取氯气的化学方程式为______ 。
(2)a中盛放的试剂为______ 。
(3)d中可选用试剂______ (填标号)。
(4)取少量KClO3和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变;2号试管溶液变为棕色,加入CCl4振荡,静置后CCl4层显紫红色。可知该条件下KClO3的氧化能力______ (填“大于”或“小于”)NaClO。
(5)一定条件下,在一定量的NaOH溶液中通入一定量的氯气,二者恰好完全反应。生成物中含有三种含氯元素的离子,其中ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。

参加反应的NaOH的物质的量为______ mol。

回答下列问题:
(1)该实验装置制取氯气的化学方程式为
(2)a中盛放的试剂为
(3)d中可选用试剂
| A.Na2S溶液 | B.NaCl溶液 | C.NaOH溶液 | D.H2SO4溶液 |
(5)一定条件下,在一定量的NaOH溶液中通入一定量的氯气,二者恰好完全反应。生成物中含有三种含氯元素的离子,其中ClO-、ClO
 两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
参加反应的NaOH的物质的量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】物质的类别和核心元素的化合价是研究物质性质的两个角度。请根据图所示回答下列问题:

(1)X与Y反应可生成淡黄色固体,反应的化学方程式____________________ 。
(2)欲制备Na2S2O3,从氧化还原角度分析,下列选项中合理的反应物是______ (填序号)。
a.Na2SO3与S b.Na2S与S
c.SO2与Na2SO4 d.Na2SO3与Na2SO4
(3)7.7g锌镁合金与一定量浓硫酸恰好完全反应,生成SO2与H2的混合气体3.36L(标准状况),反应中转移的电子的物质的量为___________ 。
(4)处理SO2废气的一种工艺如图所示:
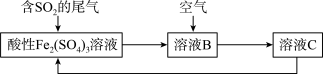
①SO2和酸性Fe2(SO4)3溶液反应的离子方程式是________________________ 。
②溶液B与空气发生反应生成溶液C,其中氧化剂是______________ 。
③推断Fe3+、O2和SO42-的氧化性由强到弱的顺序是______________ 。

(1)X与Y反应可生成淡黄色固体,反应的化学方程式
(2)欲制备Na2S2O3,从氧化还原角度分析,下列选项中合理的反应物是
a.Na2SO3与S b.Na2S与S
c.SO2与Na2SO4 d.Na2SO3与Na2SO4
(3)7.7g锌镁合金与一定量浓硫酸恰好完全反应,生成SO2与H2的混合气体3.36L(标准状况),反应中转移的电子的物质的量为
(4)处理SO2废气的一种工艺如图所示:

①SO2和酸性Fe2(SO4)3溶液反应的离子方程式是
②溶液B与空气发生反应生成溶液C,其中氧化剂是
③推断Fe3+、O2和SO42-的氧化性由强到弱的顺序是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】溴及溴化物在医药、农药、染料和阻燃剂等的生产中有广泛应用。以海水为原料提取溴单质的流程如下:

请回答下列问题:
(1)“吹出塔”中通入热空气吹出溴蒸气,说明溴单质最具有的性质可能是___________(填标号)。
(2)“吸收塔”中发生反应的离子方程式 为___________ 。
(3)粗液溴含少量Cl2,提纯溴单质的方法是加入X,蒸馏、冷凝。X可能是___________(填标号)。
(4)实验室保存液溴的试剂瓶中加一层水,其目的是___________ 。
(5)工业上也可用纯碱溶液吸收Br2,反应生成了NaBrO3、NaBr、CO2,则该反应的化学方程式 为___________ 。

请回答下列问题:
(1)“吹出塔”中通入热空气吹出溴蒸气,说明溴单质最具有的性质可能是___________(填标号)。
| A.氧化性 | B.还原性 | C.易挥发性 | D.活泼性 |
(3)粗液溴含少量Cl2,提纯溴单质的方法是加入X,蒸馏、冷凝。X可能是___________(填标号)。
| A.NaI | B.NaBr | C.NaOH | D.NaCl |
(5)工业上也可用纯碱溶液吸收Br2,反应生成了NaBrO3、NaBr、CO2,则该反应的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】Fe@Fe2O3纳米线是一种新型铁基材料,在催化、生物医药、环境科学等领域具有广阔应用前景。某研究小组以赤泥(铝土矿提取氧化铝过程中产生的固体废弃物,含SiO2、Fe2O3、Al2O3)为原料,设计下列流程制备Fe@Fe2O3纳米线并探究其在水处理中的应用。
(1)“浸出”实验中,盐酸起始浓度对铁、铝浸出率的影响如图所示:___________ 。
②盐酸起始浓度为2 mol·L-1时,铁的浸出率很低,原因是___________ 。
(2)铁的晶胞如图所示,若该晶体的密度是a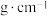 ,则两个最近的Fe原子间的距离为
,则两个最近的Fe原子间的距离为___________ cm(设NA为阿伏加德罗常数的值)。 AlO
AlO + H+ + H2O K=4×10-13。若浸出液c(Al3+) = 0.04 mol·L-1,“调节pH”时,pH最小应为
+ H+ + H2O K=4×10-13。若浸出液c(Al3+) = 0.04 mol·L-1,“调节pH”时,pH最小应为___________ (设调节pH过程中溶液体积不变)。
(4)Fe@Fe2O3纳米线为壳层结构(核是Fe、壳是Fe2O3),壳是由中心铁核在合成过程中被氧化而形成。
①“合成”时滴加NaBH4溶液过程中伴有气泡产生,滤液II中含B(OH)3,合成铁核的离子方程式为___________ 。
②“合成”后,经过滤、___________ 、___________ 获得Fe@Fe2O3纳米线。
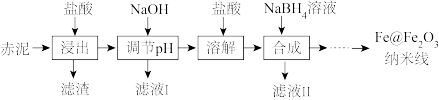
(1)“浸出”实验中,盐酸起始浓度对铁、铝浸出率的影响如图所示:
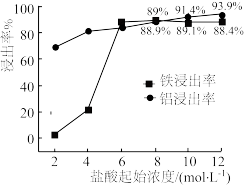
②盐酸起始浓度为2 mol·L-1时,铁的浸出率很低,原因是
(2)铁的晶胞如图所示,若该晶体的密度是a
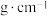 ,则两个最近的Fe原子间的距离为
,则两个最近的Fe原子间的距离为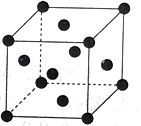
 AlO
AlO + H+ + H2O K=4×10-13。若浸出液c(Al3+) = 0.04 mol·L-1,“调节pH”时,pH最小应为
+ H+ + H2O K=4×10-13。若浸出液c(Al3+) = 0.04 mol·L-1,“调节pH”时,pH最小应为(4)Fe@Fe2O3纳米线为壳层结构(核是Fe、壳是Fe2O3),壳是由中心铁核在合成过程中被氧化而形成。
①“合成”时滴加NaBH4溶液过程中伴有气泡产生,滤液II中含B(OH)3,合成铁核的离子方程式为
②“合成”后,经过滤、
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】镁能在二氧化碳中燃烧: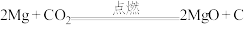 ,钠比镁更活泼,那么钠能在二氧化碳中燃烧吗?某研究性学习小组设计了如图装置进行探究。
,钠比镁更活泼,那么钠能在二氧化碳中燃烧吗?某研究性学习小组设计了如图装置进行探究。
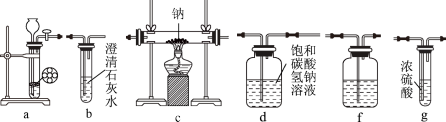
请回答下列问题:
(1)写出装置a中发生反应的离子方程式___________ 。
(2)按照气流的方向从左至右连接装置:a接___________ 、___________ 、___________ 、___________ 、___________ 。
(3)装置f中应盛放的试剂是___________ ,装置b的作用是___________ 。
(4)实验过程中,在点燃装置c中的酒精灯前,必须经过必要的操作,方可进行后续的实验,该必要操作的目的是___________ 。
(5)实验发现钠在充满二氧化碳气体的玻璃管里剧烈地燃烧,产生大量的白烟并伴有黑色物质生成。取一部分生成物于试管中,往试管中加水,白色物质溶解,黑色物质不溶。过滤,得到澄清的滤液。将滤纸上的黑色物质移人小试管中,加少量浓硫酸,加热,有刺激性气味的气体生成。则该黑色物质与浓硫酸共热的化学反应方程式为___________ 。
(6)往(5)所得滤液中加澄清石灰水,溶液变浑浊。再滴入稀盐酸,溶液中有气泡出现。试写出钠与二氧化碳反应的化学方程式:___________ 。
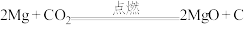 ,钠比镁更活泼,那么钠能在二氧化碳中燃烧吗?某研究性学习小组设计了如图装置进行探究。
,钠比镁更活泼,那么钠能在二氧化碳中燃烧吗?某研究性学习小组设计了如图装置进行探究。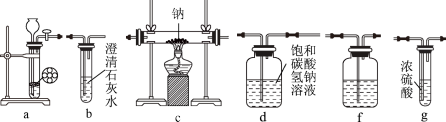
请回答下列问题:
(1)写出装置a中发生反应的离子方程式
(2)按照气流的方向从左至右连接装置:a接
(3)装置f中应盛放的试剂是
(4)实验过程中,在点燃装置c中的酒精灯前,必须经过必要的操作,方可进行后续的实验,该必要操作的目的是
(5)实验发现钠在充满二氧化碳气体的玻璃管里剧烈地燃烧,产生大量的白烟并伴有黑色物质生成。取一部分生成物于试管中,往试管中加水,白色物质溶解,黑色物质不溶。过滤,得到澄清的滤液。将滤纸上的黑色物质移人小试管中,加少量浓硫酸,加热,有刺激性气味的气体生成。则该黑色物质与浓硫酸共热的化学反应方程式为
(6)往(5)所得滤液中加澄清石灰水,溶液变浑浊。再滴入稀盐酸,溶液中有气泡出现。试写出钠与二氧化碳反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】三氯乙醛(CCl3CHO)是生产农药、医药的重要中间体,实验室制备三氯乙醛的反应装置示意图(加热装置未画出)和有关数据如图:
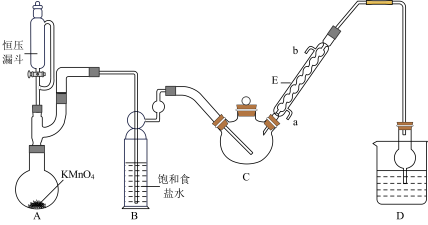
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
②反应过程中C2H5OH和HCl可能会生成副产物C2H5Cl,同时CCl3CHO(三氯乙醛)也能被次氯酸继续氧化生成CCl3COOH(三氯乙酸)
③相关物质的相对分子质量及部分物理性质:
(1)E的作用是__ ,A中所发生反应的离子方程式为____ 。
(2)写出三氯乙醛被次氯酸氧化生成三氯乙酸的化学方程式:____ 。
(3)该设计流程中存在一处缺陷是_______ ,导致引起的后果是____ 。
(4)反应结束后,有人提出先将C中的混合物冷却到室温,再用分液的方法分离出三氯乙酸。你认为此方案是否可行____ (填是或否),原因是____ 。
(5)测定产品纯度:称取产品4.6g配成待测溶液100.00mL,取待测液10.00mL于滴定瓶中,加入0.1000mol•L﹣1碘标准溶液25.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mol•L﹣1Na2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液20.00mL。则产品的纯度为____ (计算结果保留四位有效数字)。滴定原理:CCl3CHO+OH﹣=CHCl3+HCOO-、HCOO-+I2=H++2I﹣+CO2、I2+2 =2I-+
=2I-+

①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
②反应过程中C2H5OH和HCl可能会生成副产物C2H5Cl,同时CCl3CHO(三氯乙醛)也能被次氯酸继续氧化生成CCl3COOH(三氯乙酸)
③相关物质的相对分子质量及部分物理性质:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | |
| C2H5OH | 46 | ﹣114.1 | 78.3 | 与水互溶 |
| CCl3CHO | 147.5 | ﹣57.5 | 97.8 | 可溶于水、乙醇 |
| CCl3COOH | 163.5 | 58 | 198 | 可溶于水、乙醇、三氯乙醛 |
| C2H5Cl | 64.5 | ﹣138.7 | 12.3 | 微溶于水,可溶于乙醇 |
(2)写出三氯乙醛被次氯酸氧化生成三氯乙酸的化学方程式:
(3)该设计流程中存在一处缺陷是
(4)反应结束后,有人提出先将C中的混合物冷却到室温,再用分液的方法分离出三氯乙酸。你认为此方案是否可行
(5)测定产品纯度:称取产品4.6g配成待测溶液100.00mL,取待测液10.00mL于滴定瓶中,加入0.1000mol•L﹣1碘标准溶液25.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mol•L﹣1Na2S2O3溶液滴定至终点。进行三次平行实验,测得平均消耗Na2S2O3溶液20.00mL。则产品的纯度为
 =2I-+
=2I-+
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室里用下列仪器和药品制取纯净的无水氯化铜。根据要求完成以下问题:
(1)按气体从左向右流动,装置②在④左边,则②中加入的液体是___________ ;
(2)装置⑤中发生反应的化学方程式是___________ ;
(3)实验开始时,应先点燃___________ (填装置序号)处的酒精灯,否则CuCl2中含有___________ (填化学式)杂质;
(4)某实验小组组装装置时,在①和⑥之间添加了一个盛有浓硫酸的洗气瓶,其作用是___________ 。
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 仪器及装置图 |  |  |  |  |  |  |
(2)装置⑤中发生反应的化学方程式是
(3)实验开始时,应先点燃
(4)某实验小组组装装置时,在①和⑥之间添加了一个盛有浓硫酸的洗气瓶,其作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】图中为实验室制取氯气及性质验证的装置图:
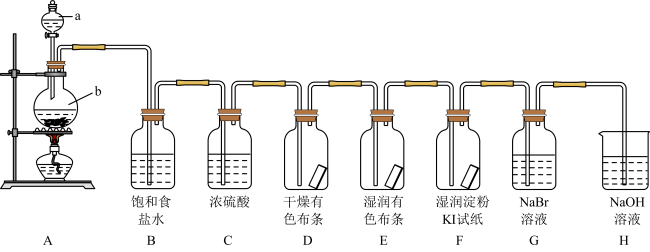
回答下列问题:
(1)仪器a的名称_______ ,写出装置A中反应的化学方程式_______ 。
(2)在装置D中可观察到的现象是_______ ,装置E中可观察到的现象是_______ ,装置F中可观察到的现象是_______ 。
(3)装置B的作用为_______ ,装置C的作用为_______ ,装置H的作用为_______ ,写出装置H的化学方程式_______ 。

回答下列问题:
(1)仪器a的名称
(2)在装置D中可观察到的现象是
(3)装置B的作用为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】如图 A、B、C、D、E 五组仪器(图中 a、b、c 表示止水夹)可以根据需要组装成不同的实验装置。某兴趣小组的同学利用这些实验仪器进行实验,请对其方案进行完善或评价。

(1)将 B、C、E 相连,用浓硫酸和浓盐酸可制取氯化氢,装在分液漏斗中的试剂是_____ ,该实验尾 气吸收装置设计有何不妥?_____ ;改正后将 B、D、E 装置相连,用 D 装置中的丁试管收集满氯化氢气体后,如果要使烧杯中的水进入试管丁的操作是_____ 。
(2)将 A、C、E 相连,并在丙中加入适量水,即可制得氯水,将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下表所示:
请你评价:
实验Ⅰ推出的相应的结论是否合理?___ ;若不合理,请说明理由,(若合理则无需填写)______ 。实验Ⅱ推出的结论是否合理?____ ;若不合理,请说明理由,(若合理则无需填写)_____ 。

(1)将 B、C、E 相连,用浓硫酸和浓盐酸可制取氯化氢,装在分液漏斗中的试剂是
(2)将 A、C、E 相连,并在丙中加入适量水,即可制得氯水,将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下表所示:
| 序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 将氯水滴入品红溶液 | 品红溶液褪色 | 氯气与水反应的产物有漂白性 |
| Ⅱ | 氯水中加入碳酸氢钠粉末 | 有无色气泡产生 | 氯气与水反应的产物具有酸性 |
实验Ⅰ推出的相应的结论是否合理?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】请选择适当的化学试剂和实验用品,用如图所示的装置(C中盛放的是过氧化钠)进行实验,证明过氧化钠可在呼吸面具和潜水艇中做供氧剂。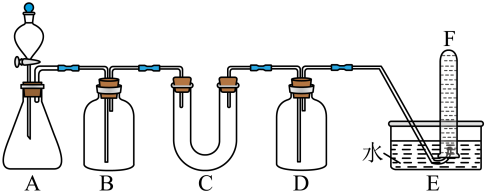
(1)A是实验室中制取CO2的装置。写出A中发生反应的离子方程式:___ 。
(2)填写下表中的空白。
(3)写出C中发生反应的化学方程式:___ 。
(4)F中得到的是___ 。如何验证___ ?

(1)A是实验室中制取CO2的装置。写出A中发生反应的离子方程式:
(2)填写下表中的空白。
| 装置序号 | 加入的试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| D |
(4)F中得到的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某化学兴趣小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去)。
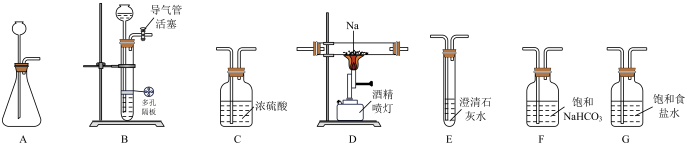
请回答下列问题:
(1)选择必要的仪器,按________ 顺序连接好装置(填装置序号)。
(2)检验装置B气密性的方法:_____________ 。
(3)实验时,在点燃酒精喷灯前必须进行的操作是________ ,待装置E中出现____ 现象时,再点燃酒精喷灯,以上操作的目的是____________ 。
(4)加热一段时间后观察到钠块表面变黑,继续加热后,钠燃烧,有白烟生成。两种产物中有一种是重要的化工原料,在玻璃工业中用量很大。则钠与二氧化碳反应的化学方程式是_______________ 。

请回答下列问题:
(1)选择必要的仪器,按
(2)检验装置B气密性的方法:
(3)实验时,在点燃酒精喷灯前必须进行的操作是
(4)加热一段时间后观察到钠块表面变黑,继续加热后,钠燃烧,有白烟生成。两种产物中有一种是重要的化工原料,在玻璃工业中用量很大。则钠与二氧化碳反应的化学方程式是
您最近一年使用:0次



