下列说法正确的是
| A.冰在室温下能自动融化成水,这是熵增的过程 |
| B.吸热反应一定不能自发进行 |
| C.非自发反应一定不能实现 |
D. , , 的反应,低温能自发进行 的反应,低温能自发进行 |
更新时间:2023-10-02 18:27:53
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
| A.电镀时通常把待镀金属制品作阳极,镀层金属作阴极 |
| B.298K时,2H2S(g) + SO2(g)=3S(s) + 2H2O(l)能自发进行,则其ΔH<0 |
| C.3molH2 和1molN2混合反应生成NH3,转移电子数为6×6.02×1023 |
| D.常温下,pH=2的醋酸溶液与pH=12的NaOH溶液等体积混合后的溶液呈碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.已知C(s)+CO2(g)=2CO(g),该反应高温条件下能自发进行的原因是ΔH>0,ΔS>0 |
| B.已知:金刚石(s)=石墨(s) ΔH<0,则该条件下石墨比金刚石稳定 |
| C.已知中和热为57.3kJ•mol-1,则稀氨水与盐酸反应生成1mol水时放出的热量大于57.3kJ |
| D.已知:2C2H4(g)+6O2(g)=4CO2(g)+4H2O(l) ΔH=-3200.8kJ•mol-1,则C2H4(g)的燃烧热ΔH=-3200.8kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】将E(s)和F(g)加入密闭容器中,在一定条件下发生反应E(s)+4F(g) G(g),已知该反应的平衡常数如表所示。下列说法正确的是
G(g),已知该反应的平衡常数如表所示。下列说法正确的是
 G(g),已知该反应的平衡常数如表所示。下列说法正确的是
G(g),已知该反应的平衡常数如表所示。下列说法正确的是| 温度/℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A.上述反应是熵增反应 |
B.25℃时,反应G(g) E(s)+4F(g)的平衡常数是0.5 E(s)+4F(g)的平衡常数是0.5 |
| C.在80℃时,测得某时刻F、G的浓度均为0.5mol·L-1,则此时v正>v逆 |
| D.恒温恒容下,向容器中再充入少量G(g),达到新平衡时,G的体积百分含量将增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中正确的是
| A.熵增加且放热的反应一定是自发反应 |
| B.自发反应一定是熵增大的反应,非自发反应一定是熵减小或不变的反应 |
| C.凡是放热反应都是能自发进行的反应,而吸热反应都是非自发进行的反应 |
| D.非自发反应在任何条件下都不能发生 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】硫酸是重要的化工原料。稀硫酸具有酸的通性;浓硫酸具有很强的氧化性,能氧化大多数金属单质和部分非金属单质。金属冶炼时产生的含SO2废气经回收处理、催化氧化、吸收后可制得硫酸。2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。对于反应2SO2(g)+O2(g)
2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。对于反应2SO2(g)+O2(g) 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是
 2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。对于反应2SO2(g)+O2(g)
2SO3(g) ΔH=-196.6kJ·mol-1。工业制硫酸尾气中的SO2可用氨水吸收,吸收液经处理后释放出的SO2又可循环利用。对于反应2SO2(g)+O2(g) 2SO3(g),下列说法正确的是
2SO3(g),下列说法正确的是| A.反应的ΔS>0 |
B.反应的平衡常数可表示为K=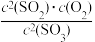 |
| C.增大体系的压强能提高SO2的反应速率和转化率 |
| D.使用催化剂能改变反应路径,提高反应的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述,正确的是( )
| A.酸和盐的混合溶液一定显酸性 |
| B.若S(s)+O2(g)=SO2(g)△H1=-a kJ/mol,S(g)+O2(g)=SO2(g)△H2=-bkJ/mol;则a>b |
| C.Na与H2O的反应是熵增的放热反应,该反应能自发进行 |
| D.2H2(g)+O2(g)=2H2O(g) △H=﹣483.6 kJ/mol,则氢气的燃烧热为241.8 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】有关汽车尾气的消除主反应为 ,在
,在 、
、 时,
时, ,则下列结论正确的是
,则下列结论正确的是
 ,在
,在 、
、 时,
时, ,则下列结论正确的是
,则下列结论正确的是
| A.高温下能自发 | B.任何温度下能自发 |
| C.低温下能自发且速率较大 | D.低温下能自发但速率较小,需催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列过程属非自发的是
| A.NaOH溶于水形成溶液 | B.水电解生成H2和O2 |
| C.气体从高密度处向低密度处扩散 | D.一瓶N2和一瓶H2混合后,形成均匀的混合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】丙烯氢甲酰化可用于合成正丁醛,但体系中会发生副反应,相关方程式如下:
主反应: CH2=CHCH3(g)+CO(g)+H2(g)=CH3CH2CH2CHO(g)(正丁醛) △H1=-123.8 kJ/mol
副反应CH2=CHCH3(g)+CO(g)+H2(g)=(CH3)2CH2CHO(g)( 异丁醛) △H2=-130.1k J/mol
CH2=CHCH3(g)+ H2(g)=CH3CH2CH3 △H3
若在一定温度下,向一个密闭恒容体系中三种原料气均投入1mol,平衡时丙烯的转化率为50%, ,
, ,下列说法正确的是
,下列说法正确的是
主反应: CH2=CHCH3(g)+CO(g)+H2(g)=CH3CH2CH2CHO(g)(正丁醛) △H1=-123.8 kJ/mol
副反应CH2=CHCH3(g)+CO(g)+H2(g)=(CH3)2CH2CHO(g)( 异丁醛) △H2=-130.1k J/mol
CH2=CHCH3(g)+ H2(g)=CH3CH2CH3 △H3
若在一定温度下,向一个密闭恒容体系中三种原料气均投入1mol,平衡时丙烯的转化率为50%,
 ,
, ,下列说法正确的是
,下列说法正确的是| A.相同条件下,正丁醛更稳定 |
B. , ,  主反应在高温条件下更有利于自发 主反应在高温条件下更有利于自发 |
| C.平衡时, 正丁醛与异丁醛物质的量之比为x:(0.4-x) |
| D.平衡时,丙烷的物质的量会随x的变化而变化 |
您最近一年使用:0次

 Mg(l)+Cl2(g)的ΔH>0,ΔS<0
Mg(l)+Cl2(g)的ΔH>0,ΔS<0

