常温下,有关下列4种溶液的叙述正确的是
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸溶液 | 盐酸 |
| pH | 11 | 11 | 3 | 3 |
| A.①中加入少量的氯化铵固体,溶液的pH减小 |
| B.分别取10mL上述溶液稀释至1000mL,四种溶液的pH:②>①>④>③ |
| C.②、③两种溶液等体积混合,所得溶液呈碱性 |
| D.用④滴定①可选择酚酞试液作指示剂 |
更新时间:2023-11-12 18:25:58
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】常温下,等浓度的 磷酸
磷酸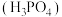 溶液、
溶液、 硫酸
硫酸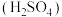 溶液及
溶液及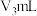 草酸
草酸 溶液分别用
溶液分别用 溶液滴定,滴定曲线如图。
溶液滴定,滴定曲线如图。 的
的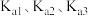 依次为
依次为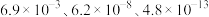 ;
; 的
的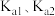 依次为
依次为 。下列说法正确的是
。下列说法正确的是
 磷酸
磷酸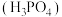 溶液、
溶液、 硫酸
硫酸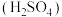 溶液及
溶液及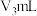 草酸
草酸 溶液分别用
溶液分别用 溶液滴定,滴定曲线如图。
溶液滴定,滴定曲线如图。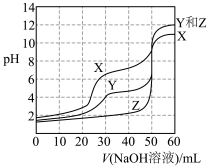
 的
的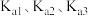 依次为
依次为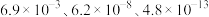 ;
; 的
的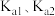 依次为
依次为 。下列说法正确的是
。下列说法正确的是A.曲线X代表 |
B.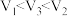 |
C.当V( 溶液) 溶液)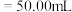 时,曲线Y对应的溶液中: 时,曲线Y对应的溶液中: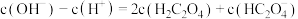 |
D. 溶液中存在: 溶液中存在: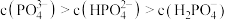 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下,在特制容器中加入20mL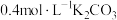 溶液,用
溶液,用 HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是
HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是
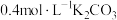 溶液,用
溶液,用 HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是
HCl溶液滴定,利用pH计和气体压力传感器检测,得到如图曲线。下列说法错误的是
A.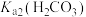 的数量级为 的数量级为 |
| B.滴定过程中,水的电离程度始终在减小 |
C.cd段反应的离子方程式为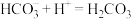 |
D.f点对应的溶液中存在: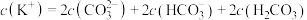 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】一定条件下,乙酸酐[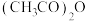 ]醇解反应可
]醇解反应可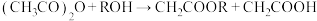 进行完全,利用此反应定量测定有机醇ROH中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
进行完全,利用此反应定量测定有机醇ROH中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入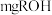 样品充分反应后,加适量水使剩余乙酸酐完全水解:
样品充分反应后,加适量水使剩余乙酸酐完全水解: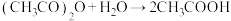 。
。
③加指示剂并用 -甲醇标准溶液滴定至终点消耗标准溶液
-甲醇标准溶液滴定至终点消耗标准溶液 。
。
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用 甲醇标准溶液滴定至终点,消耗标准溶液
甲醇标准溶液滴定至终点,消耗标准溶液 。
。
对于上述实验,下列做法正确的是
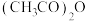 ]醇解反应可
]醇解反应可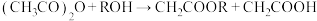 进行完全,利用此反应定量测定有机醇ROH中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
进行完全,利用此反应定量测定有机醇ROH中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:①配制一定浓度的乙酸酐-苯溶液
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入
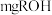 样品充分反应后,加适量水使剩余乙酸酐完全水解:
样品充分反应后,加适量水使剩余乙酸酐完全水解: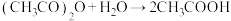 。
。③加指示剂并用
 -甲醇标准溶液滴定至终点消耗标准溶液
-甲醇标准溶液滴定至终点消耗标准溶液 。
。④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
 甲醇标准溶液滴定至终点,消耗标准溶液
甲醇标准溶液滴定至终点,消耗标准溶液 。
。对于上述实验,下列做法正确的是
| A.滴定读数时,应双手一上一下持滴定管 |
| B.滴入半滴标准溶液,锥形瓶中溶液变色,即可判定达滴定终点 |
C.样品中羟基含量(质量分数)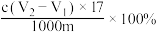 |
| D.步骤③滴定时,不慎将锥形瓶内溶液溅出,将导致测定结果偏小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】25℃时,向20mL浓度均为0.1mol•L-1的盐酸和醋酸的混合溶液中逐滴加入0.1mol•L-1的NaOH溶液(醋酸的Ka=1.8×10-5;用0.1mol•L-1的NaOH溶液滴定20mL等浓度的盐酸,滴定终点的pH突跃范围4.3~9.7)。下列说法不正确的是
| A.恰好中和时,溶液中醋酸根离子浓度为a,向其中加入0.002mol的醋酸钠固体,醋酸根离子浓度大于2a |
| B.滴加NaOH溶液至pH=4.3的过程中,发生反应的离子方程式为:H++OH-=H2O |
| C.滴定过程中,c(Cl-)=c(Ac-)+c(HAc) |
| D.pH=7时,c(Na+)>c(Cl-)>c(Ac-)>c(HAc) |
您最近一年使用:0次
单选题
|
较难
(0.4)
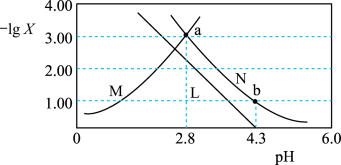
【推荐2】草酸(H2C2O4)是一种易溶于水的二元有机弱酸。常温下,向一定浓度的H2C2O4溶液中加入KOH固体,保持溶液体积和温度不变,测得溶液pH与-lgX[X为c(H2C2O4)、c(C2O )、
)、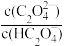 的变化关系如图所示。下列说法正确的是
的变化关系如图所示。下列说法正确的是
 )、
)、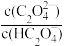 的变化关系如图所示。下列说法正确的是
的变化关系如图所示。下列说法正确的是
A.曲线M表示-lgc(C2O )随pH的变化 )随pH的变化 |
| B.常温下,H2C2O4的一级电离常数Ka1=1×10-1.3 |
| C.从a点至b点溶液中水的电离程度逐渐减小 |
D.b点溶液中:c(K+)>3c(HC2O ) ) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列是25℃时某些盐的溶度积常数和弱酸的电离平衡常数,下列说法正确的是
| 化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
| Ksp或Ka | Ksp=1.8×10-10 | Ksp=9.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
| A.H2CO3、HCO3-、CH3COO-、ClO-在溶液中可以大量共存 |
| B.等体积等浓度的CH3COONa和NaClO中离子总数:CH3COONa<NaClO |
| C.向浓度均为1.0×10-3 mol·L-1的KCl和K2CrO4混合溶液中滴加1.0×10-3 mol·L-1的AgNO3溶液,CrO42-先形成沉淀 |
| D.向0.1 mol·L-1 CH3COOH溶液中滴加NaOH溶液中至c(CH3COOH):c(CH3COO-)=5∶9,此时溶液的pH=5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】25℃时,关于某酸(用H2A表示)下列说法中,不正确的是
| A.pH=a的Na2A溶液中,由水电离产生的c(OH-)=10a-14 |
| B.将pH=a的H2A稀释为pH=a+l的过程中,c(H2A)/c(H+)减小,则H2A为弱酸 |
| C.测NaHA溶液的pH,若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| D.0.2 mol·L-1 H2A 溶液中的 c(H+)=a,0.1 mol·L-1 H2A溶液中的 c(H+)=b,若a<2 b,则H2A为弱酸 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列实验及现象能证明 是一种二元弱酸的有(注:
是一种二元弱酸的有(注: 是作为参照的二元强酸):
是作为参照的二元强酸):
①观察浓度均为0.1 的
的 溶液和
溶液和 溶液分别和大小、纯度均相同的锌粒反应时的剧烈程度:后者>前者
溶液分别和大小、纯度均相同的锌粒反应时的剧烈程度:后者>前者
②分别测浓度均为0.1 的
的 溶液和
溶液和 溶液的pH:前者>后者
溶液的pH:前者>后者
③将浓度均为0.1 的
的 溶液和
溶液和 溶液分别接入电压相同的电路中,观察小灯泡亮度:后者>前者
溶液分别接入电压相同的电路中,观察小灯泡亮度:后者>前者
④室温下,分别测浓度均为0.1 的
的 溶液和NaHA溶液的pH:7>前者>后者
溶液和NaHA溶液的pH:7>前者>后者
⑤室温下,分别测浓度均为0.1 的
的 溶液和
溶液和 溶液的pH:前者>后者
溶液的pH:前者>后者
⑥分别用等浓度的NaOH溶液滴定均为0.1 的
的 溶液和
溶液和 溶液,绘制滴定曲线并观察:前者有两个滴定突跃,后者只有一个滴定突跃
溶液,绘制滴定曲线并观察:前者有两个滴定突跃,后者只有一个滴定突跃
 是一种二元弱酸的有(注:
是一种二元弱酸的有(注: 是作为参照的二元强酸):
是作为参照的二元强酸):①观察浓度均为0.1
 的
的 溶液和
溶液和 溶液分别和大小、纯度均相同的锌粒反应时的剧烈程度:后者>前者
溶液分别和大小、纯度均相同的锌粒反应时的剧烈程度:后者>前者②分别测浓度均为0.1
 的
的 溶液和
溶液和 溶液的pH:前者>后者
溶液的pH:前者>后者③将浓度均为0.1
 的
的 溶液和
溶液和 溶液分别接入电压相同的电路中,观察小灯泡亮度:后者>前者
溶液分别接入电压相同的电路中,观察小灯泡亮度:后者>前者④室温下,分别测浓度均为0.1
 的
的 溶液和NaHA溶液的pH:7>前者>后者
溶液和NaHA溶液的pH:7>前者>后者⑤室温下,分别测浓度均为0.1
 的
的 溶液和
溶液和 溶液的pH:前者>后者
溶液的pH:前者>后者⑥分别用等浓度的NaOH溶液滴定均为0.1
 的
的 溶液和
溶液和 溶液,绘制滴定曲线并观察:前者有两个滴定突跃,后者只有一个滴定突跃
溶液,绘制滴定曲线并观察:前者有两个滴定突跃,后者只有一个滴定突跃| A.3个 | B.4个 | C.5个 | D.全部 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】部分弱酸的电离常数如下表:
下列有关说法正确的是
弱酸 | HCOOH | HCN | H2S |
电离平衡常数(25℃) | Ka=1.8×10-4 | Ka=4.9 X 10-10 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
| A.恰好中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者 |
| B.HCOO-、CN-、HS-在溶液中不可以大量共存 |
| C.NaHS溶液中加入适量KOH后:c (Na+)=c (H2S) +c (HS-) +2c (S2-) |
| D.等体积、等浓度的HCOONa和NaCN两溶液中所含离子总数目HCOONa大于NaCN |
您最近一年使用:0次



