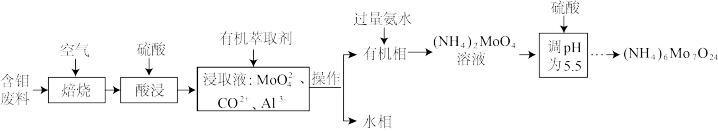
仲钼酸铵[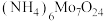 ]是用作测定磷酸盐、镍、锗、二氧化硒、砷酸盐、生物碱和铅等的试剂。用某含钼废料(主要含有
]是用作测定磷酸盐、镍、锗、二氧化硒、砷酸盐、生物碱和铅等的试剂。用某含钼废料(主要含有 、CoS和
、CoS和 )制备仲钼酸铵的工艺流程如下:
)制备仲钼酸铵的工艺流程如下:
回答下列问题:
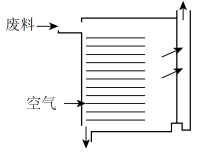
(1)焙烧的过程中采用如图所示的“多层逆流焙烧”,其优点是___________ (任答两点即可)。
(2)实验室完成流程中“操作”所用到的最主要的玻璃仪器是___________ ,该仪器使用前须___________ (填实验操作)。
(3)“调pH为5.5”生成仲钼酸铵的化学方程式为___________ 。
(4)通过电渗析法可由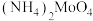 制备八钼酸铵[
制备八钼酸铵[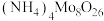 ],工作原理如图所示。阳膜只允许阳离子通过,阴膜只允许阴离子通过,双极膜中间层中的水电离为
],工作原理如图所示。阳膜只允许阳离子通过,阴膜只允许阴离子通过,双极膜中间层中的水电离为 和
和 ,并在直流电场作用下分别向两极迁移。
,并在直流电场作用下分别向两极迁移。
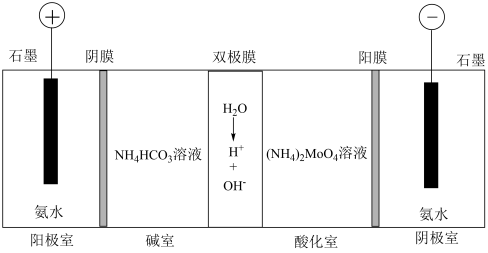
①阳极的电极反应式为___________ 。
②酸化室生成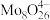 的离子方程式为
的离子方程式为___________ 。
③电解一段时间后,溶液的pH减小的室是___________ (填标号)。
A.阳极室B.碱室C.阴极室
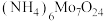 ]是用作测定磷酸盐、镍、锗、二氧化硒、砷酸盐、生物碱和铅等的试剂。用某含钼废料(主要含有
]是用作测定磷酸盐、镍、锗、二氧化硒、砷酸盐、生物碱和铅等的试剂。用某含钼废料(主要含有 、CoS和
、CoS和 )制备仲钼酸铵的工艺流程如下:
)制备仲钼酸铵的工艺流程如下:
回答下列问题:
(1)焙烧的过程中采用如图所示的“多层逆流焙烧”,其优点是

(2)实验室完成流程中“操作”所用到的最主要的玻璃仪器是
(3)“调pH为5.5”生成仲钼酸铵的化学方程式为
(4)通过电渗析法可由
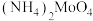 制备八钼酸铵[
制备八钼酸铵[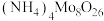 ],工作原理如图所示。阳膜只允许阳离子通过,阴膜只允许阴离子通过,双极膜中间层中的水电离为
],工作原理如图所示。阳膜只允许阳离子通过,阴膜只允许阴离子通过,双极膜中间层中的水电离为 和
和 ,并在直流电场作用下分别向两极迁移。
,并在直流电场作用下分别向两极迁移。
①阳极的电极反应式为
②酸化室生成
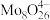 的离子方程式为
的离子方程式为③电解一段时间后,溶液的pH减小的室是
A.阳极室B.碱室C.阴极室
更新时间:2023-11-26 10:53:38
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化.
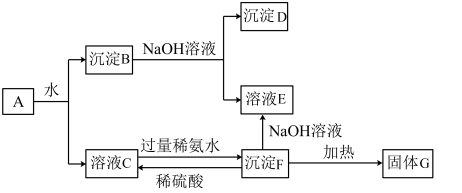
请回答下列问题:
(1)图中分离沉淀B与溶液C的方法是___________ .
(2)D、E、F这3种物质的化学式分别为:
D:___________ E:___________ F:___________
(3)沉淀B与NaOH溶液反应的离子方程式为_______________ ;溶液C与过量稀氨水反应的离子方程式为________________ .
(4)检验溶液中是否含有Fe3+,最佳试剂是___________ ,现象为_________________ .

请回答下列问题:
(1)图中分离沉淀B与溶液C的方法是
(2)D、E、F这3种物质的化学式分别为:
D:
(3)沉淀B与NaOH溶液反应的离子方程式为
(4)检验溶液中是否含有Fe3+,最佳试剂是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】结合氯气的相关知识解决下列问题。
(1)在实验室中制取Cl2,下列收集Cl2的装置中正确的是_______ (填字母)。

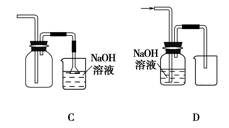
漂白粉能与盐酸发生反应,但盐酸浓度不同时,漂白粉与盐酸混合发生反应的类型不同。
漂白粉与稀盐酸发生复分解反应,化学方程式为_________________________ 。漂白粉与浓盐酸发生氧化还原反应,化学方程式为____________________________________ 。
(2)氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。
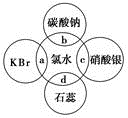
①能证明氯水具有漂白性的是______ (填“a”“b”“c”或“d”)。
②c过程中的现象是________________ 。
(1)在实验室中制取Cl2,下列收集Cl2的装置中正确的是


漂白粉能与盐酸发生反应,但盐酸浓度不同时,漂白粉与盐酸混合发生反应的类型不同。
漂白粉与稀盐酸发生复分解反应,化学方程式为
(2)氯水中含有多种成分,因而具有很多性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d重合部分代表物质间反应,且氯水足量)。

①能证明氯水具有漂白性的是
②c过程中的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】 作为一种广谱型的消毒剂,将逐渐用来取代
作为一种广谱型的消毒剂,将逐渐用来取代 成为自来水的消毒剂。已知
成为自来水的消毒剂。已知 是一种易溶于水而难溶于有机溶剂的气体,实验室制备
是一种易溶于水而难溶于有机溶剂的气体,实验室制备 的原理是用亚氯酸钠固体与氯气反应:
的原理是用亚氯酸钠固体与氯气反应: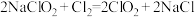 。
。
下图是实验室用于制备和收集一定量较纯净的 的装置(某些夹持装置和垫持用品省略)。其中E中盛有
的装置(某些夹持装置和垫持用品省略)。其中E中盛有 液体(用于除去
液体(用于除去 中的未反应的
中的未反应的 )。
)。
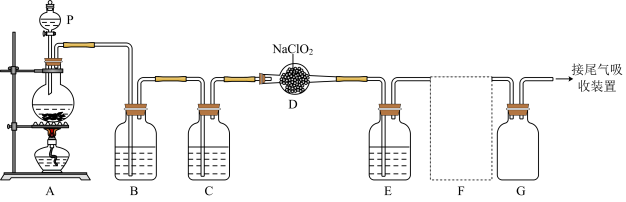
(1)仪器P的名称是___________ 。
(2)写出装置A中烧瓶内发生反应的离子方程式:___________ 。
(3)G瓶的作用是___________ 。
(4)F为 收集装置,应选用的装置是
收集装置,应选用的装置是___________ (填序号)
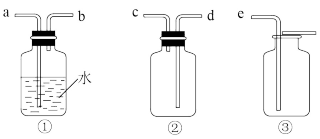
(5)若用 的浓盐酸与足量的
的浓盐酸与足量的 制备
制备 ,则被氧化的
,则被氧化的 的物质的量是___________(填序号)。
的物质的量是___________(填序号)。
 作为一种广谱型的消毒剂,将逐渐用来取代
作为一种广谱型的消毒剂,将逐渐用来取代 成为自来水的消毒剂。已知
成为自来水的消毒剂。已知 是一种易溶于水而难溶于有机溶剂的气体,实验室制备
是一种易溶于水而难溶于有机溶剂的气体,实验室制备 的原理是用亚氯酸钠固体与氯气反应:
的原理是用亚氯酸钠固体与氯气反应: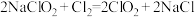 。
。下图是实验室用于制备和收集一定量较纯净的
 的装置(某些夹持装置和垫持用品省略)。其中E中盛有
的装置(某些夹持装置和垫持用品省略)。其中E中盛有 液体(用于除去
液体(用于除去 中的未反应的
中的未反应的 )。
)。
(1)仪器P的名称是
(2)写出装置A中烧瓶内发生反应的离子方程式:
(3)G瓶的作用是
(4)F为
 收集装置,应选用的装置是
收集装置,应选用的装置是
(5)若用
 的浓盐酸与足量的
的浓盐酸与足量的 制备
制备 ,则被氧化的
,则被氧化的 的物质的量是___________(填序号)。
的物质的量是___________(填序号)。A.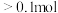 | B. | C.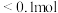 | D.无法判断 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】I.工业金属钛冶炼过程中有一步将原料金红石转化,其反应方程式为:TiO2(金红石)+2C+2Cl2=TiCl4+2CO
已知:
①C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1;
②2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·mol-1;
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=+141kJ·mol-1;
(1)CO的燃烧热是___ 。
(2)请写出金红石转化的热化学方程式___ 。
II.如图所示的三套实验装置中,甲、乙两套装置的电池反应均为Zn+Cu2+=Zn2++Cu,盐桥内装有含琼脂的饱和KCl溶液,回答下列有关问题:

(1)甲装置中铜电极上的电极反应式为___ 。
(2)放电时盐桥中的Cl-将会出现在乙装置__ (填“左”或“右”)侧的容器中,X电极的成分不可能是__ (填字母)
a.铜 b.铁 c.石墨 d.铝
(3)用丙装置在铁上镀铜,则电极材料为铁的是__ (填“Y或Z”),负极上的电极反应式为___ 。
(4)当丙池中某电极的质量减少1.6g时,则消耗的O2在标况下的体积是___ 。
已知:
①C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1;
②2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·mol-1;
③TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g) ΔH=+141kJ·mol-1;
(1)CO的燃烧热是
(2)请写出金红石转化的热化学方程式
II.如图所示的三套实验装置中,甲、乙两套装置的电池反应均为Zn+Cu2+=Zn2++Cu,盐桥内装有含琼脂的饱和KCl溶液,回答下列有关问题:

(1)甲装置中铜电极上的电极反应式为
(2)放电时盐桥中的Cl-将会出现在乙装置
a.铜 b.铁 c.石墨 d.铝
(3)用丙装置在铁上镀铜,则电极材料为铁的是
(4)当丙池中某电极的质量减少1.6g时,则消耗的O2在标况下的体积是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】氯碱工业是化工产业的重要基础,其装置示意图如下图。生产过程中产生的氯酸盐副产物需要处理。
已知:当 升高时,
升高时, 易歧化为
易歧化为 和
和 。
。
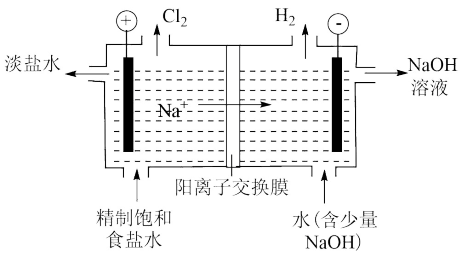
(1)电解饱和食盐水的阴极反应式为_____ 。
(2)下列关于 产生的说法中,合理的是
产生的说法中,合理的是_____ (填序号)。
a. 主要在阴极室产生
主要在阴极室产生
b. 在电极上放电,可能产生
在电极上放电,可能产生
c.阳离子交换膜破损导致 向阳极室迁移,可能产生
向阳极室迁移,可能产生
(3)测定副产物 含量的方法如下图。
含量的方法如下图。
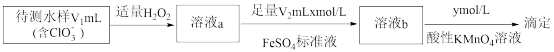
①加入 的目的是消耗水样中残留的
的目的是消耗水样中残留的 和
和 。若测定中未加入
。若测定中未加入 ,则水样中
,则水样中 的浓度将
的浓度将_____ (填“偏大”“偏小”或“不受影响”)。
②滴定测 含量消耗
含量消耗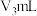 酸性
酸性 溶液,水样中
溶液,水样中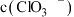 的计算式为
的计算式为_____ 。
(4)可用盐酸处理淡盐水中的 并回收
并回收
①反应的离子方程式为_____ 。
②处理 时,
时, 可能的作用是:
可能的作用是:
ⅰ.增大 ,使
,使 氧化性增强或
氧化性增强或 还原性增强;
还原性增强;
ⅱ.增大 ,
,_____ 。
③用如图装置验证ⅰ,请补全操作和现象:
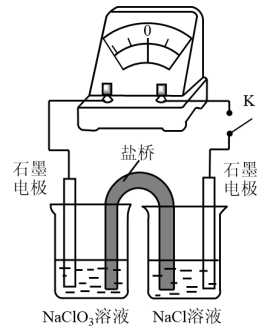
闭合 ,至指针读数稳定后
,至指针读数稳定后_____ 。
已知:当
 升高时,
升高时, 易歧化为
易歧化为 和
和 。
。
(1)电解饱和食盐水的阴极反应式为
(2)下列关于
 产生的说法中,合理的是
产生的说法中,合理的是a.
 主要在阴极室产生
主要在阴极室产生b.
 在电极上放电,可能产生
在电极上放电,可能产生
c.阳离子交换膜破损导致
 向阳极室迁移,可能产生
向阳极室迁移,可能产生
(3)测定副产物
 含量的方法如下图。
含量的方法如下图。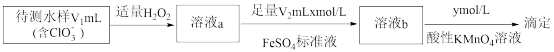
①加入
 的目的是消耗水样中残留的
的目的是消耗水样中残留的 和
和 。若测定中未加入
。若测定中未加入 ,则水样中
,则水样中 的浓度将
的浓度将②滴定测
 含量消耗
含量消耗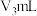 酸性
酸性 溶液,水样中
溶液,水样中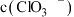 的计算式为
的计算式为(4)可用盐酸处理淡盐水中的
 并回收
并回收
①反应的离子方程式为
②处理
 时,
时, 可能的作用是:
可能的作用是:ⅰ.增大
 ,使
,使 氧化性增强或
氧化性增强或 还原性增强;
还原性增强;ⅱ.增大
 ,
,③用如图装置验证ⅰ,请补全操作和现象:

闭合
 ,至指针读数稳定后
,至指针读数稳定后
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】我国力争于2030年前完成碳达峰,2060年前实现碳中和。 含量的控制和
含量的控制和 资源利用具有重要的研究价值和现实意义。
资源利用具有重要的研究价值和现实意义。
(1)燃煤烟气中的 捕集可通过如下所示的物质转化实现。
捕集可通过如下所示的物质转化实现。
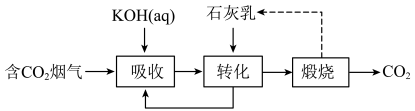
写出
充分 吸收 的化学方程式为
的化学方程式为________________ 。
(2)合成尿素 是利用
是利用 的途径之一。通过两步反应实现,其能量变化示意图所示:
的途径之一。通过两步反应实现,其能量变化示意图所示:
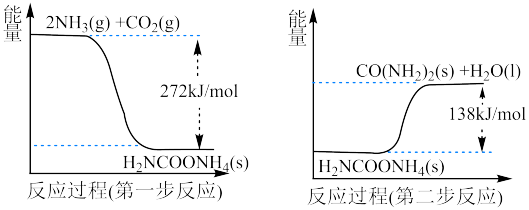
① 与
与 反应生成尿素的热化学方程式为
反应生成尿素的热化学方程式为________________ 。
②工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有________ .(填序号)
a.升高温度 b.加入催化剂
c.将尿素及时分离出去 d.增大反应体系的压强
(3)用 充分吸收
充分吸收 后,将溶液进行电解,可实现
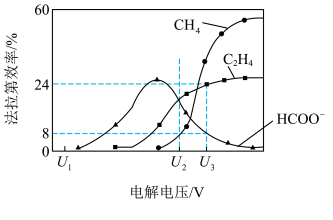
后,将溶液进行电解,可实现 转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的
转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率 (FE%)随电解电压的变化如图所示。
已知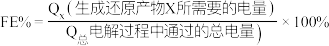
其中,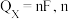 表示电解生成还原产物
表示电解生成还原产物 所转移电子的物质的量,
所转移电子的物质的量, 表示法拉第常数。
表示法拉第常数。
①当电解电压为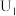 时,电解过程中含碳还原产物的
时,电解过程中含碳还原产物的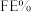 为0,阴极主要还原产物为
为0,阴极主要还原产物为________ (填化学式)。
②当电解电压为 时,阴极生成
时,阴极生成 的电极反应式为
的电极反应式为________________ .
③当电解电压为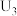 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为________ .
 含量的控制和
含量的控制和 资源利用具有重要的研究价值和现实意义。
资源利用具有重要的研究价值和现实意义。(1)燃煤烟气中的
 捕集可通过如下所示的物质转化实现。
捕集可通过如下所示的物质转化实现。
写出

 的化学方程式为
的化学方程式为(2)合成尿素
 是利用
是利用 的途径之一。通过两步反应实现,其能量变化示意图所示:
的途径之一。通过两步反应实现,其能量变化示意图所示:
①
 与
与 反应生成尿素的热化学方程式为
反应生成尿素的热化学方程式为②工业上合成尿素时,既能加快反应速率,又能提高原料利用率的措施有
a.升高温度 b.加入催化剂
c.将尿素及时分离出去 d.增大反应体系的压强
(3)用
 充分吸收
充分吸收 后,将溶液进行电解,可实现
后,将溶液进行电解,可实现 转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的
转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的
已知
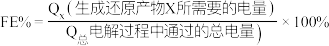
其中,
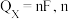 表示电解生成还原产物
表示电解生成还原产物 所转移电子的物质的量,
所转移电子的物质的量, 表示法拉第常数。
表示法拉第常数。①当电解电压为
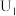 时,电解过程中含碳还原产物的
时,电解过程中含碳还原产物的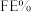 为0,阴极主要还原产物为
为0,阴极主要还原产物为②当电解电压为
 时,阴极生成
时,阴极生成 的电极反应式为
的电极反应式为③当电解电压为
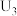 时,电解生成的
时,电解生成的 和
和 的物质的量之比为
的物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】NaCl样品中含有少量的Na2SO4和Na2CO3,按下列流程进行净化。
(1)流程第②③步中应分别使用________ 、_________ 试剂,第⑥步中应进行_________ 操作
(2)写出第⑤步发生反应的化学方程式:______________________ 。
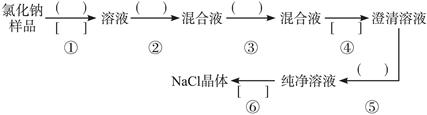
(1)流程第②③步中应分别使用
(2)写出第⑤步发生反应的化学方程式:
您最近一年使用:0次
【推荐2】工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾(K2Cr2O7)。工艺流程及相关物质溶解度曲线如图:
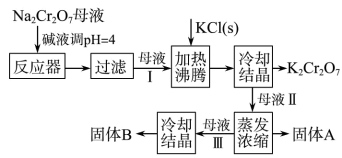
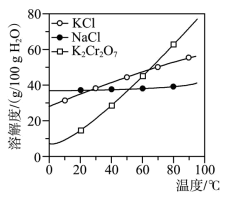
(1)向Na2Cr2O7母液中加碱液调pH的目的是为了除去Fe3+,如何确定母液中Fe3+已除尽?___________
(2)母液Ⅰ的溶质主要为__________ (填化学式);固体B主要为__________ (填化学式)。
(3)流程中要得到母液Ⅲ和固体A的操作为蒸发浓缩、_________ ,原因是________________ 。
(4)工业酸性废水中含 离子会造成铬污染,排放前先将
离子会造成铬污染,排放前先将 还原成Cr3+,并转化成Cr(OH)3除去,工业上采用的方法是向废水中加入NaCl,以铁为电极进行电解,同时鼓入空气。结果溶液的pH值不断升高,溶液由酸性转变为碱性。
还原成Cr3+,并转化成Cr(OH)3除去,工业上采用的方法是向废水中加入NaCl,以铁为电极进行电解,同时鼓入空气。结果溶液的pH值不断升高,溶液由酸性转变为碱性。
①在以上处理过程中, 转化为毒性较低的Cr3+的离子方程式为:
转化为毒性较低的Cr3+的离子方程式为:_________ 。
②在阴极区有Fe(OH)3和Cr(OH)3沉淀生成(已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。已知电解后的溶液中c(Cr3+)为3×10-5 mol·L-1,则溶液中c(Fe3+)为________ mol·L-1。


(1)向Na2Cr2O7母液中加碱液调pH的目的是为了除去Fe3+,如何确定母液中Fe3+已除尽?
(2)母液Ⅰ的溶质主要为
(3)流程中要得到母液Ⅲ和固体A的操作为蒸发浓缩、
(4)工业酸性废水中含
 离子会造成铬污染,排放前先将
离子会造成铬污染,排放前先将 还原成Cr3+,并转化成Cr(OH)3除去,工业上采用的方法是向废水中加入NaCl,以铁为电极进行电解,同时鼓入空气。结果溶液的pH值不断升高,溶液由酸性转变为碱性。
还原成Cr3+,并转化成Cr(OH)3除去,工业上采用的方法是向废水中加入NaCl,以铁为电极进行电解,同时鼓入空气。结果溶液的pH值不断升高,溶液由酸性转变为碱性。①在以上处理过程中,
 转化为毒性较低的Cr3+的离子方程式为:
转化为毒性较低的Cr3+的离子方程式为:②在阴极区有Fe(OH)3和Cr(OH)3沉淀生成(已知Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)。已知电解后的溶液中c(Cr3+)为3×10-5 mol·L-1,则溶液中c(Fe3+)为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】现用金属钠和空气制备纯度较高的Na2O2,可利用的装置如下。回答下列问题(注:Na2O2可以与H2O、CO2反应):
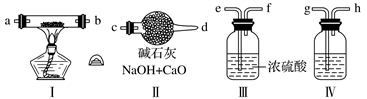
(1)装置Ⅳ中盛放的药品是________ ,其作用是_______________________________ 。
(2)若规定气体的气流方向从左到右,则组合实验装置时各件仪器的正确连接顺序为(各仪器接口的标号字母顺序):空气进入 g ,________ 接________ ,________ 接________ ,________ 接________ (用字母表示)。
(3)装置Ⅱ的作用_____________________________________________ 。
(4)操作中通空气和加热的顺序为_______________________________ 。

(1)装置Ⅳ中盛放的药品是
(2)若规定气体的气流方向从左到右,则组合实验装置时各件仪器的正确连接顺序为(各仪器接口的标号字母顺序):空气进入 g ,
(3)装置Ⅱ的作用
(4)操作中通空气和加热的顺序为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】过氧化钡( )是一种重要的漂白剂,在实验室利用重晶石(主要成分为
)是一种重要的漂白剂,在实验室利用重晶石(主要成分为 )制备
)制备 的工艺流程如图所示:
的工艺流程如图所示:

回答下列问题:
(1)“步骤①”设计如图装置(夹持仪器已省略)制备 并检验所产生的气体X。
并检验所产生的气体X。
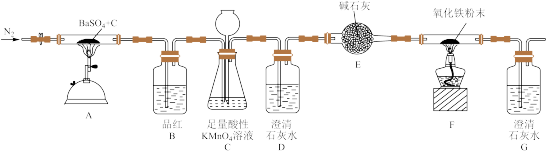
①实验前及实验结束时均要通入 ,其目的分别是
,其目的分别是_______ 、_______ 。
②实验过程中B中品红褪色,C中颜色变淡,D中无现象,G中有白色沉淀生成,气体X的成分为_______ (填化学式);装置C的作用是_______ ,其中发生主要反应的离子方程式为_______ 。
(2)“步骤②”中 固体与
固体与 、
、 发生反应生成
发生反应生成 ,和
,和 的化学方程式为
的化学方程式为_______ ;由于“步骤③”反应剧烈,易产生大量泡沫,为了避免此种情况的发生,应采用措施是_______ 。
(3)“步骤④"中 溶液与双氧水、氨水反应析出
溶液与双氧水、氨水反应析出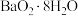 沉淀,发生反应的离子方程式为
沉淀,发生反应的离子方程式为_______ ,反应过程中需要控制反应温度为 左右,其原因主要有:a.该反应是放热反应,降温有利于反应正向进行,提高产率;b.
左右,其原因主要有:a.该反应是放热反应,降温有利于反应正向进行,提高产率;b._______ 。
 )是一种重要的漂白剂,在实验室利用重晶石(主要成分为
)是一种重要的漂白剂,在实验室利用重晶石(主要成分为 )制备
)制备 的工艺流程如图所示:
的工艺流程如图所示:
回答下列问题:
(1)“步骤①”设计如图装置(夹持仪器已省略)制备
 并检验所产生的气体X。
并检验所产生的气体X。
①实验前及实验结束时均要通入
 ,其目的分别是
,其目的分别是②实验过程中B中品红褪色,C中颜色变淡,D中无现象,G中有白色沉淀生成,气体X的成分为
(2)“步骤②”中
 固体与
固体与 、
、 发生反应生成
发生反应生成 ,和
,和 的化学方程式为
的化学方程式为(3)“步骤④"中
 溶液与双氧水、氨水反应析出
溶液与双氧水、氨水反应析出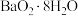 沉淀,发生反应的离子方程式为
沉淀,发生反应的离子方程式为 左右,其原因主要有:a.该反应是放热反应,降温有利于反应正向进行,提高产率;b.
左右,其原因主要有:a.该反应是放热反应,降温有利于反应正向进行,提高产率;b.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】2020年春节前后,新型冠状病毒 严重影响了人们正常生活。含次氯酸钠
严重影响了人们正常生活。含次氯酸钠 的水溶液具备良好的杀菌消毒效果。某化学兴趣小组拟利用实验室的常见药品制备次氯酸钠消毒液,并探讨提高消毒液中次氯酸钠百分比的方法。
的水溶液具备良好的杀菌消毒效果。某化学兴趣小组拟利用实验室的常见药品制备次氯酸钠消毒液,并探讨提高消毒液中次氯酸钠百分比的方法。
Ⅰ 该小组同学采用了高锰酸钾和浓盐酸在图1所示装置①中制氯气,请回答下列问题:
该小组同学采用了高锰酸钾和浓盐酸在图1所示装置①中制氯气,请回答下列问题:
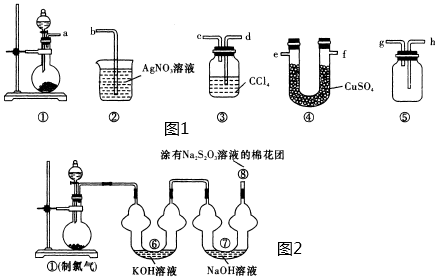
 ①中反应的化学方程式为
①中反应的化学方程式为___________ 。
 甲同学利用图1中的装置①~⑤证明从a出来的氯气潮湿且含有氯化氢,则接口的连接顺序a
甲同学利用图1中的装置①~⑤证明从a出来的氯气潮湿且含有氯化氢,则接口的连接顺序a
___________  填接口编号
填接口编号 ⑤中放入
⑤中放入___________ 。乙同学认为甲同学的装置太复杂,可去掉装置⑤,同时将②中的溶液换成W,溶液W及实验中对应的现象为___________ 。
Ⅱ,该小组同学将氯气通入含氢氧化钠溶液的烧杯中,发现反应放热明显,查阅资料获悉,氯气与碱溶液反应,产物会随反应温度的不同而不同。具体如下: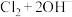
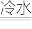
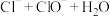
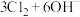
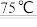
 该小组利用该信息又设计了如图2所示的装置制取
该小组利用该信息又设计了如图2所示的装置制取 和NaClO。
和NaClO。
 该小组应控制的实验条件是
该小组应控制的实验条件是___________ 。反应后,从装置⑥中溶液蒸发浓缩获得晶体,将该晶体与二氧化锰共热,生成了能使带火星的木条复燃气体。
 ⑧处发生反应的离子方程式为
⑧处发生反应的离子方程式为___________ 。
 根据上述Ⅰ、Ⅱ两个实验过程,你认为在实验室制取消毒液并提高次氯酸钠的质量分数,应该注意的事项有
根据上述Ⅰ、Ⅱ两个实验过程,你认为在实验室制取消毒液并提高次氯酸钠的质量分数,应该注意的事项有 列举两条
列举两条 。①
。①___________ ;② ___________ 。
 严重影响了人们正常生活。含次氯酸钠
严重影响了人们正常生活。含次氯酸钠 的水溶液具备良好的杀菌消毒效果。某化学兴趣小组拟利用实验室的常见药品制备次氯酸钠消毒液,并探讨提高消毒液中次氯酸钠百分比的方法。
的水溶液具备良好的杀菌消毒效果。某化学兴趣小组拟利用实验室的常见药品制备次氯酸钠消毒液,并探讨提高消毒液中次氯酸钠百分比的方法。Ⅰ
 该小组同学采用了高锰酸钾和浓盐酸在图1所示装置①中制氯气,请回答下列问题:
该小组同学采用了高锰酸钾和浓盐酸在图1所示装置①中制氯气,请回答下列问题:
 ①中反应的化学方程式为
①中反应的化学方程式为 甲同学利用图1中的装置①~⑤证明从a出来的氯气潮湿且含有氯化氢,则接口的连接顺序a
甲同学利用图1中的装置①~⑤证明从a出来的氯气潮湿且含有氯化氢,则接口的连接顺序a
 填接口编号
填接口编号 ⑤中放入
⑤中放入Ⅱ,该小组同学将氯气通入含氢氧化钠溶液的烧杯中,发现反应放热明显,查阅资料获悉,氯气与碱溶液反应,产物会随反应温度的不同而不同。具体如下:
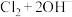
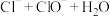
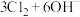
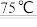
 该小组利用该信息又设计了如图2所示的装置制取
该小组利用该信息又设计了如图2所示的装置制取 和NaClO。
和NaClO。 该小组应控制的实验条件是
该小组应控制的实验条件是 ⑧处发生反应的离子方程式为
⑧处发生反应的离子方程式为 根据上述Ⅰ、Ⅱ两个实验过程,你认为在实验室制取消毒液并提高次氯酸钠的质量分数,应该注意的事项有
根据上述Ⅰ、Ⅱ两个实验过程,你认为在实验室制取消毒液并提高次氯酸钠的质量分数,应该注意的事项有 列举两条
列举两条 。①
。①
您最近一年使用:0次

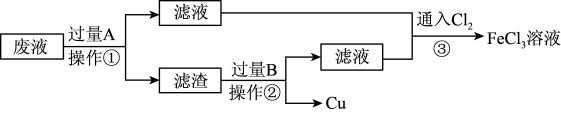
 溶液腐蚀铜(原理为:
溶液腐蚀铜(原理为: )制造印刷线路板。为了从腐蚀废液中回收铜并重新得到
)制造印刷线路板。为了从腐蚀废液中回收铜并重新得到