Ⅰ.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如图:

已知NaHCO3在低温下溶解度较小。
(1)反应Ⅰ的化学方程式为_______ 。
Ⅱ.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中 Na2CO3的含量。
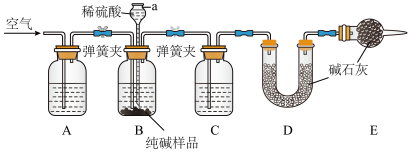
(2)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若_______ ,说明装置不漏气。
(3)装置A中的试剂为_______ ,装置C中的试剂为_______ 。装置E的作用是_______ 。
(4)实验前称取28.80 g样品,实验后测得D装置增重8.80 g,则样品中Na2CO3的质量分数为_______ (保留一位小数);若缺少E装置,会使测定结果_______ (填“偏高”或“偏低”)。

已知NaHCO3在低温下溶解度较小。
(1)反应Ⅰ的化学方程式为
Ⅱ.工业纯碱中常含有少量NaCl,某校化学课外活动小组设计如图所示装置,测定工业纯碱中 Na2CO3的含量。

(2)检验装置B气密性的方法是:塞紧带长颈漏斗的三孔橡胶塞,夹紧两侧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于瓶内的水面,停止加水后,若
(3)装置A中的试剂为
(4)实验前称取28.80 g样品,实验后测得D装置增重8.80 g,则样品中Na2CO3的质量分数为
更新时间:2023-11-26 17:13:45
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室需要0.1mol·L-1NaOH溶液480mL,根据这种溶液的配制情况回答下列问题:

(1)如图所示的仪器中配制溶液肯定不需要的是___________ (填仪器名称),本实验所需玻璃仪器D规格为___________ mL。
(2)配制时,其正确的操作顺序是(字母表示,每个操作只用一次)___________ 。
A.用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(3)在配制NaOH溶液实验中,若出现如下情况,其中将引起所配溶液浓度大于0.1mol/L的是___________ 。(填下列编号)
①容量瓶实验前用蒸馏水洗干净,但未烘干
②定容时俯视液面
③配制过程中遗漏了(2)中步骤A
④加蒸馏水时不慎超过了刻度,立即用胶头滴管将多余的水吸出
(4)如要用Na2O作为原料对该溶液进行配制,求所需Na2O的最少质量。(写出计算过程)_______

(1)如图所示的仪器中配制溶液肯定不需要的是
(2)配制时,其正确的操作顺序是(字母表示,每个操作只用一次)
A.用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(3)在配制NaOH溶液实验中,若出现如下情况,其中将引起所配溶液浓度大于0.1mol/L的是
①容量瓶实验前用蒸馏水洗干净,但未烘干
②定容时俯视液面
③配制过程中遗漏了(2)中步骤A
④加蒸馏水时不慎超过了刻度,立即用胶头滴管将多余的水吸出
(4)如要用Na2O作为原料对该溶液进行配制,求所需Na2O的最少质量。(写出计算过程)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】己二酸(HOOCCH2CH2CH2CH2COOH)是一种工业上有重要意义的二元酸,实验室利用环己醇(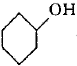 )合成己二酸的反应原理为:
)合成己二酸的反应原理为: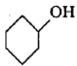 +8HNO3→HOOCCH2CH2CH2CH2COOH+8NO2↑+5H2O
+8HNO3→HOOCCH2CH2CH2CH2COOH+8NO2↑+5H2O
实验装置如下图:
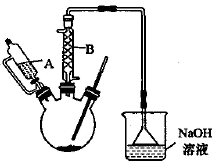
可能用到的有关数据如下表所示:
实验步骤如下:
①在三口烧瓶中加入50mL50%硝酸(密度为 ),再加入1~2粒沸石,滴液漏斗中盛放5.4mL(5.2g)环己醇。
),再加入1~2粒沸石,滴液漏斗中盛放5.4mL(5.2g)环己醇。
②水浴加热三口烧瓶至50℃左右,移去水浴,逐滴加入5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩余的环己醇,维持反应温度在60~65℃之间。
③当环己醇全部加入后,将混合物用80~90℃水浴加热约10min(注意控制温度),直至_______为止。
④趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品。
⑤粗产品经提纯后称重为5.2g。
回答下列问题:
(1)仪器B的名称为_______ 。
(2)步骤②环己醇要逐滴滴加的原因是_______ 。
(3)步骤③中,停止加热的判断依据是_______ 。
(4)烧杯中NaOH溶液的作用是_______ (用离子方程式表示)。
(5)步骤④中为了除去可能的杂质和减少产品损失,可分别用冰水和_______ 洗涤晶体。
(6)粗产品可用_______ 法(填实验操作名称)提纯。
(7)本实验所得己二酸产率为_______ 。(保留一位小数)
 )合成己二酸的反应原理为:
)合成己二酸的反应原理为: +8HNO3→HOOCCH2CH2CH2CH2COOH+8NO2↑+5H2O
+8HNO3→HOOCCH2CH2CH2CH2COOH+8NO2↑+5H2O实验装置如下图:

可能用到的有关数据如下表所示:
| 物质 | 熔点/℃ | 沸点/℃ | 溶解性 | 相对分子质量 |
| 环己醇 | 25.9 | 160.8 | 20℃时水中溶解度为3.6g,可溶于乙醇、苯 | 100 |
| 己二酸 | 152 | 337.5 | 在水中溶解度:15℃时为1.44g,25℃时为2.3g,易溶于乙醇,不溶于苯 | 146 |
①在三口烧瓶中加入50mL50%硝酸(密度为
 ),再加入1~2粒沸石,滴液漏斗中盛放5.4mL(5.2g)环己醇。
),再加入1~2粒沸石,滴液漏斗中盛放5.4mL(5.2g)环己醇。②水浴加热三口烧瓶至50℃左右,移去水浴,逐滴加入5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩余的环己醇,维持反应温度在60~65℃之间。
③当环己醇全部加入后,将混合物用80~90℃水浴加热约10min(注意控制温度),直至_______为止。
④趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤得粗产品。
⑤粗产品经提纯后称重为5.2g。
回答下列问题:
(1)仪器B的名称为
(2)步骤②环己醇要逐滴滴加的原因是
(3)步骤③中,停止加热的判断依据是
(4)烧杯中NaOH溶液的作用是
(5)步骤④中为了除去可能的杂质和减少产品损失,可分别用冰水和
(6)粗产品可用
(7)本实验所得己二酸产率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上用粉碎的黄铁矿(主要成分可表示为 ,其中还有少量
,其中还有少量 等)为原料制备硫酸的流程如图:
等)为原料制备硫酸的流程如图:
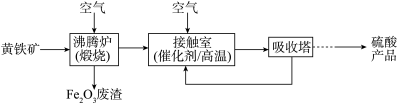
回答下列问题:
(1)硫酸厂沸腾炉排出的矿渣中含有 、CuO,请写出煅烧
、CuO,请写出煅烧 的化学方程式
的化学方程式___________ ,为提高生产效率,工业生产中我们会采用一定的办法加快反应速率,你认为上述流程中能加快速率的做法有___________ (至少写出两条)。
(2)在接触室中发生的是 的催化氧化反应,该反应属于
的催化氧化反应,该反应属于___________ (填字母)。
a.氧化还原反应 b.离子反应 c.化合反应 d.可逆反应
(3)为提高原料的转化率,并减少污染物的产生,落实绿色化学思想,上述流程中可循环利用的物质有___________ 。
(4)国家规定由吸收塔排出的尾气中 的最高含量不得超过
的最高含量不得超过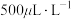 ,否则就要加以处理才能排出。处理方法之一是用足量氨水洗涤烟气脱硫,所得产物
,否则就要加以处理才能排出。处理方法之一是用足量氨水洗涤烟气脱硫,所得产物 可作为肥料。请与出此脱硫过程中可能发生反应的离子方程式:
可作为肥料。请与出此脱硫过程中可能发生反应的离子方程式:___________ ,___________ 。
(5)用含硫质量分数为a%的硫铁矿制硫酸,若高温煅烧时损失b%的硫元素,由 制
制 的转化率为c%,则制取1吨98%的硫酸需这种硫铁矿的质量为
的转化率为c%,则制取1吨98%的硫酸需这种硫铁矿的质量为___________ 吨(列出表达式即可,不必化简)。
 ,其中还有少量
,其中还有少量 等)为原料制备硫酸的流程如图:
等)为原料制备硫酸的流程如图:
回答下列问题:
(1)硫酸厂沸腾炉排出的矿渣中含有
 、CuO,请写出煅烧
、CuO,请写出煅烧 的化学方程式
的化学方程式(2)在接触室中发生的是
 的催化氧化反应,该反应属于
的催化氧化反应,该反应属于a.氧化还原反应 b.离子反应 c.化合反应 d.可逆反应
(3)为提高原料的转化率,并减少污染物的产生,落实绿色化学思想,上述流程中可循环利用的物质有
(4)国家规定由吸收塔排出的尾气中
 的最高含量不得超过
的最高含量不得超过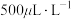 ,否则就要加以处理才能排出。处理方法之一是用足量氨水洗涤烟气脱硫,所得产物
,否则就要加以处理才能排出。处理方法之一是用足量氨水洗涤烟气脱硫,所得产物 可作为肥料。请与出此脱硫过程中可能发生反应的离子方程式:
可作为肥料。请与出此脱硫过程中可能发生反应的离子方程式:(5)用含硫质量分数为a%的硫铁矿制硫酸,若高温煅烧时损失b%的硫元素,由
 制
制 的转化率为c%,则制取1吨98%的硫酸需这种硫铁矿的质量为
的转化率为c%,则制取1吨98%的硫酸需这种硫铁矿的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】生活处处有化学,制作馒头、面包等所用的发酵粉,主要成分是由 、
、 和固体有机酸混合而成的,晓露同学猜想:发酵粉加热或加水时都能产生
和固体有机酸混合而成的,晓露同学猜想:发酵粉加热或加水时都能产生 ,并进行如下实验:
,并进行如下实验:
(1)将 和
和 分别加热,能产生
分别加热,能产生 的物质是
的物质是_______ (填化学式)。
(2)晓露同学用如图所示装置探究发酵粉加水能否产生 ,并探究过氧化钠是否可作呼吸面具的供氧剂。请回答:
,并探究过氧化钠是否可作呼吸面具的供氧剂。请回答:

①A装置中仪器中装发酵粉的仪器名称是_______ 。
②观察到B装置产生白色浑浊,写出反应的离子方程式_______ 。
③C装置中浓硫酸的作用是_______ 。
④收集D装置产生的气体,要验证它是氧气,方法是_______ 。D中反应的化学方程式为_______ 。
 、
、 和固体有机酸混合而成的,晓露同学猜想:发酵粉加热或加水时都能产生
和固体有机酸混合而成的,晓露同学猜想:发酵粉加热或加水时都能产生 ,并进行如下实验:
,并进行如下实验:(1)将
 和
和 分别加热,能产生
分别加热,能产生 的物质是
的物质是(2)晓露同学用如图所示装置探究发酵粉加水能否产生
 ,并探究过氧化钠是否可作呼吸面具的供氧剂。请回答:
,并探究过氧化钠是否可作呼吸面具的供氧剂。请回答:
①A装置中仪器中装发酵粉的仪器名称是
②观察到B装置产生白色浑浊,写出反应的离子方程式
③C装置中浓硫酸的作用是
④收集D装置产生的气体,要验证它是氧气,方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】“侯氏制碱法”促进了我国纯碱工业的发展。某化学兴趣小组在实验室中模拟并改进侯氏制碱法用碳酸氢铵(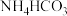 )和氯化钠为主要原料制备碳酸钠的实验流程如图。
)和氯化钠为主要原料制备碳酸钠的实验流程如图。

回答下列问题:
(1)“加热搅拌”中发生反应的化学方程式是___________ ,该反应属于___________ (填基本反应类型)。
(2)“300℃加热”需用到的仪器除酒精灯、坩埚、坩埚钳、泥三角、三角架外,还有___________ 。
(3)除去 溶液中混有的少量
溶液中混有的少量 的最佳方法是
的最佳方法是___________ ,化学方程式为___________ 。
(4)检验 中阳离子的实验方法是
中阳离子的实验方法是___________ 。
(5)现将 和
和 的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体23.4g。则混合物中
的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为___________ 。
(6)若将 和
和 的固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生
的固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生 的体积关系如图所示,则线段)
的体积关系如图所示,则线段)
___________ 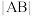 (填“>”“<”或“=”),OA段发生反应的离子方程式为
(填“>”“<”或“=”),OA段发生反应的离子方程式为___________ 。

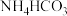 )和氯化钠为主要原料制备碳酸钠的实验流程如图。
)和氯化钠为主要原料制备碳酸钠的实验流程如图。
回答下列问题:
(1)“加热搅拌”中发生反应的化学方程式是
(2)“300℃加热”需用到的仪器除酒精灯、坩埚、坩埚钳、泥三角、三角架外,还有
(3)除去
 溶液中混有的少量
溶液中混有的少量 的最佳方法是
的最佳方法是(4)检验
 中阳离子的实验方法是
中阳离子的实验方法是(5)现将
 和
和 的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体23.4g。则混合物中
的固体均匀混合物等分成两份。第一份充分加热至恒重,固体质量减少6.2g;第二份与足量稀盐酸充分反应后,加热、蒸干、灼烧,得到固体23.4g。则混合物中 和
和 的物质的量之比为
的物质的量之比为(6)若将
 和
和 的固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生
的固体混合物溶于水,向溶液中加入盐酸,所加盐酸的体积与产生 的体积关系如图所示,则线段)
的体积关系如图所示,则线段)
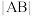 (填“>”“<”或“=”),OA段发生反应的离子方程式为
(填“>”“<”或“=”),OA段发生反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】我国制碱专家侯德榜先生潜心研究制碱技术,发明了侯氏制碱法。工业上以侯氏制碱法为基础生产焦亚硫酸钠 的工艺流程如下:
的工艺流程如下:
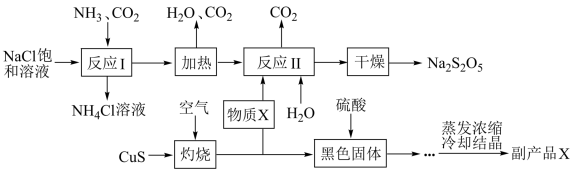
已知:反应Ⅱ包含 等多步反应。
等多步反应。
(1)反应Ⅰ的化学方程式为___________ ;在进行反应Ⅰ时,向饱和 溶液中先通入
溶液中先通入___________ (填“ ”或“
”或“ ”)。
”)。
(2)图中物质X是 ,“灼烧”时发生反应的化学方程式为
,“灼烧”时发生反应的化学方程式为___________ 。
(3)已知 与稀硫酸反应放
与稀硫酸反应放 ,其离子方程式为
,其离子方程式为___________ 。
(4)副产品X化学式为___________ ;生产中可循环利用的物质为___________ (化学式)。
 的工艺流程如下:
的工艺流程如下:
已知:反应Ⅱ包含
 等多步反应。
等多步反应。(1)反应Ⅰ的化学方程式为
 溶液中先通入
溶液中先通入 ”或“
”或“ ”)。
”)。(2)图中物质X是
 ,“灼烧”时发生反应的化学方程式为
,“灼烧”时发生反应的化学方程式为(3)已知
 与稀硫酸反应放
与稀硫酸反应放 ,其离子方程式为
,其离子方程式为(4)副产品X化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某校化学兴趣小组实验室模拟工业制备硫氰化钾(KSCN)实验装置如图:

实验步骤如下:
(1)制备NH4SCN溶液:CS2+2NH3 NH4SCN+H2S。该反应比较缓慢。
NH4SCN+H2S。该反应比较缓慢。
①实验前,应进行的操作是___ ,三颈烧瓶内盛放有CS2、水和催化剂,三颈烧瓶的下层CS2液体必须浸没导气管口的目的是___ 。
②实验开始时打开K1,加热装置A、D,缓缓地向装置D中充入气体,装置A试管内发生反应的化学方程式是___ 。
(2)制备KSCN溶液:移去A处的酒精灯,关闭K1,打开K2,利用耐碱分液漏斗边加液边加热,则此时装置D中发生反应的化学方程式是___ ,D中橡皮管的作用是___ 。
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压浓缩、___ 、过滤、干燥,得到硫氰化钾晶体。

实验步骤如下:
(1)制备NH4SCN溶液:CS2+2NH3
 NH4SCN+H2S。该反应比较缓慢。
NH4SCN+H2S。该反应比较缓慢。①实验前,应进行的操作是
②实验开始时打开K1,加热装置A、D,缓缓地向装置D中充入气体,装置A试管内发生反应的化学方程式是
(2)制备KSCN溶液:移去A处的酒精灯,关闭K1,打开K2,利用耐碱分液漏斗边加液边加热,则此时装置D中发生反应的化学方程式是
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压浓缩、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的流程如下:
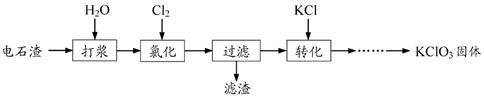
(1)氯化过程控制电石渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。
①生成Ca(ClO)2的化学方程式为________ 。
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有________ (填序号)。
A.适当减缓通入Cl2速率
B.充分搅拌浆料
C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O。氯化完成后过滤。
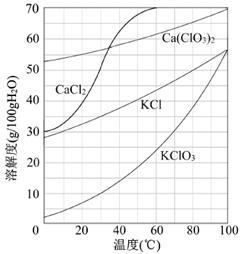
①滤渣的主要成分为____ (填化学式)。
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] ∶n[CaCl2]_____ 1∶5(填“>”、“<”或“=”)。
(3)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,若溶液中KClO3的含量为100g▪L-1,从该溶液中尽可能多地析出KClO3固体的方法是____ 。

(1)氯化过程控制电石渣过量,在75℃左右进行。氯化时存在Cl2与Ca(OH)2作用生成Ca(ClO)2的反应,Ca(ClO)2进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2。
①生成Ca(ClO)2的化学方程式为
②提高Cl2转化为Ca(ClO3)2的转化率的可行措施有
A.适当减缓通入Cl2速率
B.充分搅拌浆料
C.加水使Ca(OH)2完全溶解
(2)氯化过程中Cl2转化为Ca(ClO3)2的总反应方程式为6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O。氯化完成后过滤。

①滤渣的主要成分为
②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] ∶n[CaCl2]
(3)向滤液中加入稍过量KCl固体可将Ca(ClO3)2转化为KClO3,若溶液中KClO3的含量为100g▪L-1,从该溶液中尽可能多地析出KClO3固体的方法是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】金属钒主要用于冶炼特种钢,被誉为“合金的维生素”。人们在化工实践中,以富钒炉渣(其中的钒以 、
、 等形式存在,还有少量的
等形式存在,还有少量的 、
、 等)为原料提取金属钒的工艺流程如下图所示。
等)为原料提取金属钒的工艺流程如下图所示。

提示:①钒有多种价态,其中+5价最稳定;② 在碱性条件下可转化为
在碱性条件下可转化为 。
。
(1)试列举可加快“高温氧化”速率的措施_______ (填一措施即可)。
(2)气体X、气体Y和滤渣1的化学式分别为_______ 、______ 、_______ 。
(3)“高温氧化”过程中,若有1mol 被氧化,则转移电子数为
被氧化,则转移电子数为______  。
。
(4)试写出“焙烧”时 发生反应的化学方程式为
发生反应的化学方程式为______ 。
(5)硅参与“高温还原”反应的化学方程式为_______ 。
(6)钒比铁的金属性强,“粗钒”中含少量铁和硅,工业上通过电解精炼“粗钒”可得到99.5%的纯钒,以熔融 电解质,则“粗钒”应连接电源的
电解质,则“粗钒”应连接电源的___ 极,阴极的电极反应式为______ 。
 、
、 等形式存在,还有少量的
等形式存在,还有少量的 、
、 等)为原料提取金属钒的工艺流程如下图所示。
等)为原料提取金属钒的工艺流程如下图所示。
提示:①钒有多种价态,其中+5价最稳定;②
 在碱性条件下可转化为
在碱性条件下可转化为 。
。(1)试列举可加快“高温氧化”速率的措施
(2)气体X、气体Y和滤渣1的化学式分别为
(3)“高温氧化”过程中,若有1mol
 被氧化,则转移电子数为
被氧化,则转移电子数为 。
。(4)试写出“焙烧”时
 发生反应的化学方程式为
发生反应的化学方程式为(5)硅参与“高温还原”反应的化学方程式为
(6)钒比铁的金属性强,“粗钒”中含少量铁和硅,工业上通过电解精炼“粗钒”可得到99.5%的纯钒,以熔融
 电解质,则“粗钒”应连接电源的
电解质,则“粗钒”应连接电源的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】利用 合成尿素是
合成尿素是 资源化的重要途径,可产生巨大的经济价值。
资源化的重要途径,可产生巨大的经济价值。
(1)20世纪初,工业上以 和
和 为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
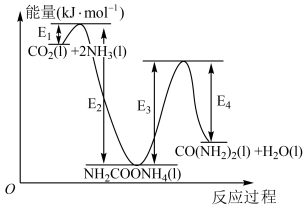
①反应物液氨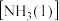 分子间除存在范德华力外,还存在
分子间除存在范德华力外,还存在___________ (填作用力名称)。
②写出在该条件下由 和
和 合成尿素的热化学方程式:
合成尿素的热化学方程式:___________ 。
(2)近年研究发现,电催化 和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的
和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的 溶液通入
溶液通入 至饱和,经电解获得尿素,其原理如图所示。
至饱和,经电解获得尿素,其原理如图所示。
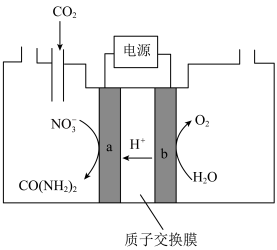
①电解过程中生成尿素的电极反应式为___________ 。
②目前以 和
和 为原料的电化学尿素合成可达到
为原料的电化学尿素合成可达到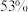 的法拉第效率
的法拉第效率 。已知:
。已知: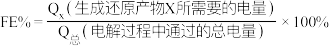 ,其中,
,其中,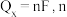 表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下
表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下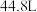 的
的 ,可获得尿素的质量为
,可获得尿素的质量为___________ 。(尿素的相对分子质量:60)
(3)尿素样品含氮量的测定方法如下。
已知:溶液中 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。

①消化液中的含氮粒子是___________ 。
②步骤ⅳ中标准 溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有___________ 。
 合成尿素是
合成尿素是 资源化的重要途径,可产生巨大的经济价值。
资源化的重要途径,可产生巨大的经济价值。(1)20世纪初,工业上以
 和
和 为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
为原料在一定温度压强下合成尿素,反应过程中能量变化如图。
①反应物液氨
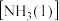 分子间除存在范德华力外,还存在
分子间除存在范德华力外,还存在②写出在该条件下由
 和
和 合成尿素的热化学方程式:
合成尿素的热化学方程式:(2)近年研究发现,电催化
 和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的
和含氮物质可合成尿素,同时可解决含氮废水污染问题。常温常压下,向一定浓度的 溶液通入
溶液通入 至饱和,经电解获得尿素,其原理如图所示。
至饱和,经电解获得尿素,其原理如图所示。
①电解过程中生成尿素的电极反应式为
②目前以
 和
和 为原料的电化学尿素合成可达到
为原料的电化学尿素合成可达到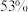 的法拉第效率
的法拉第效率 。已知:
。已知: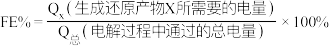 ,其中,
,其中,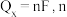 表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下
表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。则电解时阳极每产生标况下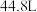 的
的 ,可获得尿素的质量为
,可获得尿素的质量为(3)尿素样品含氮量的测定方法如下。
已知:溶液中
 不能直接用
不能直接用 溶液准确滴定。
溶液准确滴定。
①消化液中的含氮粒子是
②步骤ⅳ中标准
 溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
溶液的浓度和消耗的体积分别为c和V,计算样品含氮量还需要的实验数据有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某研究性学习小组探究FeSO4的化学性质并测定某药片中FeSO4的含量,回答下列问题。
(1)探究FeSO4溶液的酸碱性。实验测得FeSO4溶液呈_______ (填“酸性”、“中性”、“碱性”)。
(2)利用如图装置探究FeSO4的稳定性。

(2)已知:绿矾为FeSO4·7H2O晶体,受热分解产物为4种氧化物。
①实验中观察到Ⅰ中固体逐渐变为红棕色,Ⅱ中有白色沉淀生成。Ⅱ中现象表明绿矾分解产物有_______ (填化学式)。
②预测Ⅲ中现象为_______ ,设计实验证明Ⅲ中现象有可逆性,操作和现象为:取少量Ⅲ中溶液于试管中,_______ 。
③Ⅳ中NaOH溶液的作用是吸收尾气,防止污染空气。反应的化学方程式为_______ 。
(3)缺铁性贫血往往口服主要成分为FeSO4的药片。现用氧化还原滴定法测定某品牌药片中FeSO4含量,反应原理为:MnO +5Fe2+ +8H+ =Mn2+ +5Fe3+ +4H2O。称取8.0g药片,剥掉表面糖衣,将药片捣碎,配成100mL溶液,用KMnO4溶液滴定。
+5Fe2+ +8H+ =Mn2+ +5Fe3+ +4H2O。称取8.0g药片,剥掉表面糖衣,将药片捣碎,配成100mL溶液,用KMnO4溶液滴定。
该药片中FeSO4的质量分数为_______ ,若盛装KMnO4溶液的滴定管用蒸馏水洗净后没有润洗,则测定结果将_______ 。(填“偏大”、“偏小”、“不变”)。
(1)探究FeSO4溶液的酸碱性。实验测得FeSO4溶液呈
(2)利用如图装置探究FeSO4的稳定性。

(2)已知:绿矾为FeSO4·7H2O晶体,受热分解产物为4种氧化物。
①实验中观察到Ⅰ中固体逐渐变为红棕色,Ⅱ中有白色沉淀生成。Ⅱ中现象表明绿矾分解产物有
②预测Ⅲ中现象为
③Ⅳ中NaOH溶液的作用是吸收尾气,防止污染空气。反应的化学方程式为
(3)缺铁性贫血往往口服主要成分为FeSO4的药片。现用氧化还原滴定法测定某品牌药片中FeSO4含量,反应原理为:MnO
 +5Fe2+ +8H+ =Mn2+ +5Fe3+ +4H2O。称取8.0g药片,剥掉表面糖衣,将药片捣碎,配成100mL溶液,用KMnO4溶液滴定。
+5Fe2+ +8H+ =Mn2+ +5Fe3+ +4H2O。称取8.0g药片,剥掉表面糖衣,将药片捣碎,配成100mL溶液,用KMnO4溶液滴定。| 滴定次数 | 待测FeSO4溶液体积/mL | 0.1000 mol/LKMnO4溶液体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 0.00 | 25.11 |
| 2 | 25.00 | 0.56 | 30.56 |
| 3 | 25.00 | 0.22 | 25.11 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】铝热法冶炼金属铬的矿渣中含有Cr2O3、Al2O3及少量Fe2O3,从中提取铬与铝有酸法和碱法两种工艺。请回答:
I.酸法。矿渣经硫酸浸取后,浸取液通过电沉积得到单质Cr;向剩余溶液中加碱回收得到Al(OH)3。
(1)为提高矿渣的浸取率,可采取的措施有_______ (写出两点)。
(2)电沉积时,阴极发生的电极反应式为_______ 。
II.碱法。工艺流程如下:

已知:①“焙烧”后固体成分为Na2CrO4、NaAlO2、NaFeO2。
② 、Zn2+均可与EDTA1:1结合成络离子;Zn2+可与PAN1:1结合成紫红色络合物,且结合能力弱于EDTA。
、Zn2+均可与EDTA1:1结合成络离子;Zn2+可与PAN1:1结合成紫红色络合物,且结合能力弱于EDTA。
(3)浸渣的主要成分为Fe(OH)3,则“浸取”时发生反应的离子方程式为_______ 。
(4)“浸取”后所得溶液中Al的含量可用EDTA滴定法测定:
①取20.00mL浸取液于锥形瓶中,加入c1mol·L-1EDTA标准液V1mL(稍过量);
②依次用盐酸、醋酸钠—醋酸缓冲溶液调溶液至酸性,加热后滴入PAN指示剂;
③用c2mol·L-1ZnSO4标准液滴定至溶液恰好呈紫红色,消耗标准液V2mL。
则“浸取”后所得溶液中Al的含量为_______ g·L-1(填计算式即可)。
(5)“碳分”时通入CO2后,通过_______ (填操作名称),即可得到纯净的Al2O3。
(6)“还原”时发生主要反应的离子方程式为_______ 。
I.酸法。矿渣经硫酸浸取后,浸取液通过电沉积得到单质Cr;向剩余溶液中加碱回收得到Al(OH)3。
(1)为提高矿渣的浸取率,可采取的措施有
(2)电沉积时,阴极发生的电极反应式为
II.碱法。工艺流程如下:

已知:①“焙烧”后固体成分为Na2CrO4、NaAlO2、NaFeO2。
②
 、Zn2+均可与EDTA1:1结合成络离子;Zn2+可与PAN1:1结合成紫红色络合物,且结合能力弱于EDTA。
、Zn2+均可与EDTA1:1结合成络离子;Zn2+可与PAN1:1结合成紫红色络合物,且结合能力弱于EDTA。(3)浸渣的主要成分为Fe(OH)3,则“浸取”时发生反应的离子方程式为
(4)“浸取”后所得溶液中Al的含量可用EDTA滴定法测定:
①取20.00mL浸取液于锥形瓶中,加入c1mol·L-1EDTA标准液V1mL(稍过量);
②依次用盐酸、醋酸钠—醋酸缓冲溶液调溶液至酸性,加热后滴入PAN指示剂;
③用c2mol·L-1ZnSO4标准液滴定至溶液恰好呈紫红色,消耗标准液V2mL。
则“浸取”后所得溶液中Al的含量为
(5)“碳分”时通入CO2后,通过
(6)“还原”时发生主要反应的离子方程式为
您最近一年使用:0次



