请按照要求用对应的化学术语回答下列问题。
(1) 是一种酸式盐,请写出
是一种酸式盐,请写出 在水中的电离方程式
在水中的电离方程式___________ 。
(2)将饱和 溶液滴入到沸水中,继续煮沸至液体变为红褐色,反应的离子方程式为
溶液滴入到沸水中,继续煮沸至液体变为红褐色,反应的离子方程式为___________ 。
(3) 可以作为供氧剂,其与
可以作为供氧剂,其与 反应时若生成标准状况下11.2L
反应时若生成标准状况下11.2L  ,则电子转移数目为
,则电子转移数目为___________ 。
(4) 溶于水可以产生具有漂白性的物质,
溶于水可以产生具有漂白性的物质, 与水反应的离子方程式为:
与水反应的离子方程式为:___________ 。
(5)某温度下将 通入KOH溶液里,反应后得到KCl、KClO、
通入KOH溶液里,反应后得到KCl、KClO、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为11∶1,则
的个数之比为11∶1,则 与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为___________ 。
(6)在标准状况下,将V L氨气溶于0.1L水中,所得溶液的密度为 ,则此氨水的物质的量浓度为
,则此氨水的物质的量浓度为___________  。
。
(1)
 是一种酸式盐,请写出
是一种酸式盐,请写出 在水中的电离方程式
在水中的电离方程式(2)将饱和
 溶液滴入到沸水中,继续煮沸至液体变为红褐色,反应的离子方程式为
溶液滴入到沸水中,继续煮沸至液体变为红褐色,反应的离子方程式为(3)
 可以作为供氧剂,其与
可以作为供氧剂,其与 反应时若生成标准状况下11.2L
反应时若生成标准状况下11.2L  ,则电子转移数目为
,则电子转移数目为(4)
 溶于水可以产生具有漂白性的物质,
溶于水可以产生具有漂白性的物质, 与水反应的离子方程式为:
与水反应的离子方程式为:(5)某温度下将
 通入KOH溶液里,反应后得到KCl、KClO、
通入KOH溶液里,反应后得到KCl、KClO、 的混合溶液,其中
的混合溶液,其中 与
与 的个数之比为11∶1,则
的个数之比为11∶1,则 与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为
与KOH反应时,被还原的氯原子和被氧化的氯原子的个数之比为(6)在标准状况下,将V L氨气溶于0.1L水中,所得溶液的密度为
 ,则此氨水的物质的量浓度为
,则此氨水的物质的量浓度为 。
。
更新时间:2023-11-29 11:32:44
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表为“鲜花保鲜剂”的配比表。
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是_______。
(2)配制240 mL的上述“鲜花保鲜剂”所需的仪器有:烧杯、玻璃棒、药匙、电子天平、 _______ 、_______ 。
(3)在溶液配制过程中,下列操作对配制结果没有影响的是_______。
(4)“鲜花保鲜剂”中K+(蔗糖和阿司匹林中不含K+)的物质的量浓度为_______ mol/L。
| 成分 | 质量(g) | 摩尔质量(g/mol) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.87 | 174 |
| 阿可匹林 | 0.17 | 180 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.075 | 170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是_______。
| A.蔗糖 | B.硫酸钾 | C.高锰酸钾 | D.硝酸银 |
(3)在溶液配制过程中,下列操作对配制结果没有影响的是_______。
| A.定容时俯视容量瓶刻度线 |
| B.容量瓶在使用前未干燥,里面有少量蒸馏水 |
| C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净 |
| D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】有下列物质:①Na2CO3·10H2O晶体 ②铜 ③硫酸溶液 ④CO2 ⑤NaHSO4固体 ⑥Ba(OH)2固体 ⑦红褐色的氢氧化铁胶体 ⑧氨水 ⑨蔗糖 ⑩Al2(SO4)3固体。
(1)上述物质属于电解质的有___________ (填编号,下同)。属于非电解质的是___________ 。
(2)17.1 g⑩溶于水配成 250 mL 溶液, SO 的物质的量浓度为
的物质的量浓度为___________ 。
(3)写出固体⑤溶于水中的电离方程式___________ 。
(4)胶体是一种常见的分散系,向煮沸的蒸馏水中逐滴加入几滴饱和的___________ (填化学式)溶液,继续煮沸至___________ ,停止加热,可制得Fe(OH)3胶体,制取Fe(OH)3胶体的化学方程式为___________ 。162.5 g FeCl3与沸水形成的Fe(OH)3胶体粒子数___________ NA(填“>”,“<”“=”)
(1)上述物质属于电解质的有
(2)17.1 g⑩溶于水配成 250 mL 溶液, SO
 的物质的量浓度为
的物质的量浓度为(3)写出固体⑤溶于水中的电离方程式
(4)胶体是一种常见的分散系,向煮沸的蒸馏水中逐滴加入几滴饱和的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】64.0gCu与200mL10.0mol·L-1的浓硝酸反应,标准状况下测得反应产生的NO、NO2混合气体13.44L,且充分反应后铜仍有剩余。请计算:
(1)混合气体中NO与NO2的物质的量之比为___________ ;
(2)向反应后的溶液中滴加稀硫酸可使铜完全溶解,若该过程中只有NO气体生成,则还能产生NO的物质的量为___________ 。
(3)若铜完全反应,最终溶液中铜离子的物质的量浓度是______ (假设溶液体积变化忽略不计)
(1)混合气体中NO与NO2的物质的量之比为
(2)向反应后的溶液中滴加稀硫酸可使铜完全溶解,若该过程中只有NO气体生成,则还能产生NO的物质的量为
(3)若铜完全反应,最终溶液中铜离子的物质的量浓度是
您最近一年使用:0次
【推荐2】(1)某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。(As为砷元素)
①已知KBrO3在反应中得到电子,则该反应的还原剂是____________________
②已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为_____________
③根据上述反应可推知_______
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4> KBrO3
c.还原性:AsH3>X d.还原性:X > AsH3
(2)①向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发如下反应:Mn2++S2O82-+H2O→MnO4-+SO42-+H+,该反应常用于检验Mn2+的存在。其特征现象是_________________ ,若反应中有0.1 mol还原剂参加反应,则消耗氧化剂的物质的量为__________
②将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:NaBiO3+MnSO4+H2SO4→Na2SO4+Bi2(SO4)3+NaMnO4+H2O,配平上述反应的化学方程式,并用双线桥标出电子转移的方向和数目__________ ;
①已知KBrO3在反应中得到电子,则该反应的还原剂是
②已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为
③根据上述反应可推知
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4> KBrO3
c.还原性:AsH3>X d.还原性:X > AsH3
(2)①向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发如下反应:Mn2++S2O82-+H2O→MnO4-+SO42-+H+,该反应常用于检验Mn2+的存在。其特征现象是
②将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:NaBiO3+MnSO4+H2SO4→Na2SO4+Bi2(SO4)3+NaMnO4+H2O,配平上述反应的化学方程式,并用双线桥标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
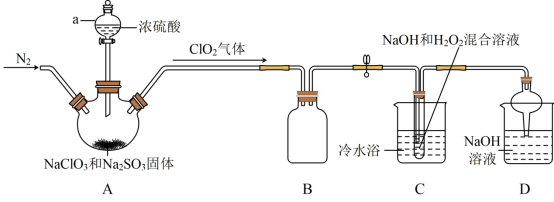
【推荐3】二氧化氯(ClO2)与亚氯酸钠(NaClO2)都具有强氧化性。两者作漂白剂时,不伤害织物;作饮用水消毒剂时,不残留异味。某研究性学习小组利用如图装置由二氧化氯制备NaClO2·3H2O,并探究其性质。
①ClO2易与碱反应生成亚氯酸盐和氯酸盐。
②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
利用题中原理制备出NaClO2·3H2O晶体的试样,可以用“间接碘量法”测定试样(杂质与I-不发生反应)的纯度,过程如下:(已知:I2+2 =
=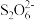 +2I-)取样品0.6000g于锥形瓶中,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,然后用0.5000mol·L-1Na2S2O3标准溶液滴定,当出现
+2I-)取样品0.6000g于锥形瓶中,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,然后用0.5000mol·L-1Na2S2O3标准溶液滴定,当出现_______ (填实验现象),达到滴定终点,共消耗该标准溶液25.00mL,经计算该试样中NaClO2·3H2O的百分含量为_______ (结果保留3位有效数字)。
①ClO2易与碱反应生成亚氯酸盐和氯酸盐。
②NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
利用题中原理制备出NaClO2·3H2O晶体的试样,可以用“间接碘量法”测定试样(杂质与I-不发生反应)的纯度,过程如下:(已知:I2+2
 =
=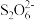 +2I-)取样品0.6000g于锥形瓶中,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,然后用0.5000mol·L-1Na2S2O3标准溶液滴定,当出现
+2I-)取样品0.6000g于锥形瓶中,加入足量KI固体和适量稀H2SO4,再滴加几滴淀粉溶液,然后用0.5000mol·L-1Na2S2O3标准溶液滴定,当出现
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氯气及其化合物在工农业生产和人类生活中都有着重要的应用。
(1)NaClO有较强的氧化性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式_________________________ 。
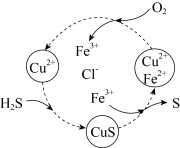
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应可以回收S,其物质转化如图所示。该图示的总反应为_________________________ 。
(3)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用Al粉还原NO3-,产物是N2。发生的反应可表示如下,请完成方程式的配平。
___ Al+___ NO3-+___ =___ AlO2-+___ N2↑+___ H2O
(1)NaClO有较强的氧化性,所以是常用的消毒剂和漂白剂,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式
(2)将H2S和空气的混合气体通入FeCl3、FeCl2、CuCl2的混合溶液中反应可以回收S,其物质转化如图所示。该图示的总反应为

(3)自来水中的NO3-对人类健康产生危害。为了降低自来水中NO3-的浓度,某研究人员提出在碱性条件下用Al粉还原NO3-,产物是N2。发生的反应可表示如下,请完成方程式的配平。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】饮用水质量是关系人类健康的重要问题。
(1)Cl2是最早用于饮用水消毒的物质,写出Cl2溶于水发生反应的离子方程式:___________ 。
(2)ClO2是一种高效、低毒的消毒剂,逐渐取代Cl2成为生产自来水的消毒剂,工业上用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应中氧化剂与还原剂物质的量之比为___________ 。
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,比Cl2、ClO2氧化性更强,是无二次污染的绿色水处理剂。高铁酸钾溶于水放出氧气,能杀菌消毒,生成能吸附水中悬浮物的氢氧化铁胶体。用一个离子方程式表示高铁酸钾处理水的过程___________ 。干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应的还原剂是___________ ,每生成1 mol Na2FeO4转移___________ mol电子。
(1)Cl2是最早用于饮用水消毒的物质,写出Cl2溶于水发生反应的离子方程式:
(2)ClO2是一种高效、低毒的消毒剂,逐渐取代Cl2成为生产自来水的消毒剂,工业上用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应中氧化剂与还原剂物质的量之比为
(3)高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,比Cl2、ClO2氧化性更强,是无二次污染的绿色水处理剂。高铁酸钾溶于水放出氧气,能杀菌消毒,生成能吸附水中悬浮物的氢氧化铁胶体。用一个离子方程式表示高铁酸钾处理水的过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】含氯化合物在生活生产中具有广泛作用。完成下列问题:
(1)含氯产品①中钢瓶上应贴的标签为___________。
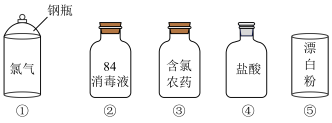
(2)关于保存液氯、液溴的说法正确的是___________。
(3)关于液氯与新制氯水叙述正确的是___________。
(4)氯水久置易变质,检验一瓶氯水是否已经完全变质,可选用的试剂是___________。
(5)某实验小组想验证氯水中 光照分解的产物,将图1新制氯水置于三颈瓶内,将
光照分解的产物,将图1新制氯水置于三颈瓶内,将 传感器、氯离子传感器、氧气传感器分别插入三颈瓶中,用强光照射氯水,进行实验并采集数据,获得相关变化曲线。则图2中纵坐标不可以表示的物理量是___________。(注:酸性溶液中,
传感器、氯离子传感器、氧气传感器分别插入三颈瓶中,用强光照射氯水,进行实验并采集数据,获得相关变化曲线。则图2中纵坐标不可以表示的物理量是___________。(注:酸性溶液中, 越大,
越大, 越小,溶液酸性越强)
越小,溶液酸性越强)
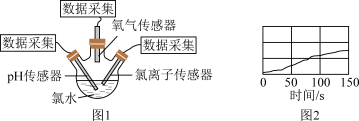
(6)漂粉精的有效成分为___________ (填写化学式)。实验证实,某批次的漂白粉碱性明显大于正常的漂白粉。原因可能是该批次的产品中混有较多的___________ (填写化学式)。请你用化学方程式表示家庭使用漂粉精漂白的原理___________ 。
(7)现有一种漂粉精: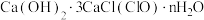 的"有效氯"为
的"有效氯"为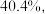 则式中
则式中 值应是
值应是___________ 。(漂白粉的消毒能力以酸化时释放出来的氯气量作标准,用来衡量含氯消毒剂的消毒能力,以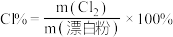 (有效氯含量)表示)
(有效氯含量)表示)
(1)含氯产品①中钢瓶上应贴的标签为___________。

A. | B. | C. | D. |
(2)关于保存液氯、液溴的说法正确的是___________。
| A.液氯贮存在干燥的钢瓶中 | B.液溴保存时需加入一些水覆盖 |
| C.常温下保存液氯应采用低压 | D.液溴应保存在棕色的广口瓶中 |
(3)关于液氯与新制氯水叙述正确的是___________。
| A.都含有氯离子 | B.都含氯分子 |
| C.都是电解质 | D.都能导电 |
(4)氯水久置易变质,检验一瓶氯水是否已经完全变质,可选用的试剂是___________。
| A.硝酸银溶液 | B.酚酞溶液 | C.碳酸钠溶液 | D.紫色石蕊溶液 |
(5)某实验小组想验证氯水中
 光照分解的产物,将图1新制氯水置于三颈瓶内,将
光照分解的产物,将图1新制氯水置于三颈瓶内,将 传感器、氯离子传感器、氧气传感器分别插入三颈瓶中,用强光照射氯水,进行实验并采集数据,获得相关变化曲线。则图2中纵坐标不可以表示的物理量是___________。(注:酸性溶液中,
传感器、氯离子传感器、氧气传感器分别插入三颈瓶中,用强光照射氯水,进行实验并采集数据,获得相关变化曲线。则图2中纵坐标不可以表示的物理量是___________。(注:酸性溶液中, 越大,
越大, 越小,溶液酸性越强)
越小,溶液酸性越强)
A.氯水的 | B.氢离子的浓度 | C.氯离子的浓度 | D.氧气的体积分数 |
(6)漂粉精的有效成分为
(7)现有一种漂粉精:
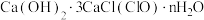 的"有效氯"为
的"有效氯"为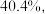 则式中
则式中 值应是
值应是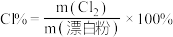 (有效氯含量)表示)
(有效氯含量)表示)
您最近一年使用:0次
【推荐1】实验室可用多种方法制取氯气。其变化可表述为
①2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
②2KMnO4+l6HCl(浓) = 2KCl+2MnCl2+5Cl2↑+8H2O
③MnO2+4HCl (浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(1)用单线桥法表示第一个反应电子转移的方向和数目:_______________________________________________________________ 。
(2)请将第二个化学方程式改写为离子方程式:_______________________________________________________________ 。
(3)浓盐酸在后两个反应中显示出来的性质是________ (填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若要制得相同质量的氯气,上述三种方法中电子转移的数目之比________ 。
①2NaCl+2H2O
 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑②2KMnO4+l6HCl(浓) = 2KCl+2MnCl2+5Cl2↑+8H2O
③MnO2+4HCl (浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(1)用单线桥法表示第一个反应电子转移的方向和数目:
(2)请将第二个化学方程式改写为离子方程式:
(3)浓盐酸在后两个反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若要制得相同质量的氯气,上述三种方法中电子转移的数目之比
您最近一年使用:0次
【推荐2】根据反应NH3+Cl2=NH4Cl+N2回答下列问题。
(1)配平系数为___________ ,
(2)氧化剂___________ ,还原剂___________ ;
(3)1molNH3参与反应转移电子数是___________ (用 表示);
表示);
(4)当生成28gN2时,被氧化的物质的物质的量是___________ mol。
(1)配平系数为
(2)氧化剂
(3)1molNH3参与反应转移电子数是
 表示);
表示);氧化剂与氧化产物的质量比
(4)当生成28gN2时,被氧化的物质的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】按要求填空:
(1)高铁酸钠( )是一种新型的净水剂,可以通过下述反应制取:
)是一种新型的净水剂,可以通过下述反应制取:
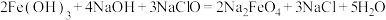 。
。
① 中Fe元素的化合价是
中Fe元素的化合价是___________ ,反应中被还原的元素是___________ (用元素符号表示)
②用双线桥法表示反应中电子转移的方向和数目:___________ 。
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以用化学方法处理
的浓度,可以用化学方法处理 ,其化学方程式为
,其化学方程式为 。
。
①上述反应中,氧化剂是___________ (用化学式表示)
②在上述反应中,每生成1个 分子,转移电子数目为
分子,转移电子数目为___________ 个。
(1)高铁酸钠(
 )是一种新型的净水剂,可以通过下述反应制取:
)是一种新型的净水剂,可以通过下述反应制取: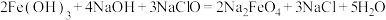 。
。①
 中Fe元素的化合价是
中Fe元素的化合价是②用双线桥法表示反应中电子转移的方向和数目:
(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以用化学方法处理
的浓度,可以用化学方法处理 ,其化学方程式为
,其化学方程式为 。
。①上述反应中,氧化剂是
②在上述反应中,每生成1个
 分子,转移电子数目为
分子,转移电子数目为
您最近一年使用:0次



