18世纪70年代,瑞典化学家舍勒将软锰矿与浓盐酸混合加热,制得了黄绿色、有刺激性气味的氯气。氯气可形成多种含氯酸盐,广泛应用于杀菌、消毒及化工领域。某研究性学习小组的同学们模拟科学家的研究过程进行了如下实验,制备收集纯净干燥的氯气。

回答下列问题:
(1)仪器a的名称为___________ ,写出装置甲中发生反应的化学方程式___________ ,该反应中,氧化剂和还原剂的物质的量之比为___________ 。
(2)装置乙中的试剂为___________ ,可除去 中的
中的 ;装置丙中盛放浓硫酸,其目的是
;装置丙中盛放浓硫酸,其目的是__________ 。
(3)作为气体收集的装置图丁,最合适的是___________ (填标号)。

(4)装置戊中反应的离子方程式为___________ ,这样可以吸收多余的氯气,防止污染空气。

回答下列问题:
(1)仪器a的名称为
(2)装置乙中的试剂为
 中的
中的 ;装置丙中盛放浓硫酸,其目的是
;装置丙中盛放浓硫酸,其目的是(3)作为气体收集的装置图丁,最合适的是

(4)装置戊中反应的离子方程式为
更新时间:2023-11-29 17:59:10
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】尿素[CO(NH2)2]是目前使用量较大的一种化学氮肥。某化学实验小组以尿素为原料制备 (水合肼)并验证水合肼还原性的实验流程如图1所示:
(水合肼)并验证水合肼还原性的实验流程如图1所示:

已知① 沸点用196.6℃;
沸点用196.6℃;
② 沸点为118℃,且能与NaClO剧烈反应生成
沸点为118℃,且能与NaClO剧烈反应生成 。
。
I. 的制备
的制备
(1)从图2的A~E中选择合适的装置制备并收集较纯净的 ,各装置合理的连接顺序为a→_______→_______→_______→_______→_______→_______→d。
,各装置合理的连接顺序为a→_______→_______→_______→_______→_______→_______→d。__________

(2)“步骤一”在高温条件下会有副反应发生,为确保该步骤在低温环境下进行,常采取的措施为_______ ,该步骤发生反应的离子方程式为_______ 。
(3)“步骤二”在图3所示装置中完成。为了避免生成 ,将滴液漏斗b中的NaClO与NaOH混合液缓慢滴入盛有mg尿素的三颈烧瓶a中,边滴加边搅拌,温度迅速升高到120℃。
,将滴液漏斗b中的NaClO与NaOH混合液缓慢滴入盛有mg尿素的三颈烧瓶a中,边滴加边搅拌,温度迅速升高到120℃。

①仪器c的名称为_______
②生成水合肼的化学方程式为_______ 。
Ⅱ.验证 的还原性
的还原性
(4)将“步骤二”制得的水合肼配成1000mL溶液,移出25mL于锥形瓶中,滴加2滴淀粉溶液,用0.05mol/L的 溶液滴定,当滴定完全时,消耗
溶液滴定,当滴定完全时,消耗 溶液VmL。
溶液VmL。
①滴定过程中水合肼被氧化为 ,反应的化学方程式为
,反应的化学方程式为_______ 。
②配成的水合肼的浓度
_______ mol/L(用含V的代数式表示)。
③ 的产率为
的产率为_______ (用含m、V的代数式表示)。
 (水合肼)并验证水合肼还原性的实验流程如图1所示:
(水合肼)并验证水合肼还原性的实验流程如图1所示:
已知①
 沸点用196.6℃;
沸点用196.6℃;②
 沸点为118℃,且能与NaClO剧烈反应生成
沸点为118℃,且能与NaClO剧烈反应生成 。
。I.
 的制备
的制备(1)从图2的A~E中选择合适的装置制备并收集较纯净的
 ,各装置合理的连接顺序为a→_______→_______→_______→_______→_______→_______→d。
,各装置合理的连接顺序为a→_______→_______→_______→_______→_______→_______→d。
(2)“步骤一”在高温条件下会有副反应发生,为确保该步骤在低温环境下进行,常采取的措施为
(3)“步骤二”在图3所示装置中完成。为了避免生成
 ,将滴液漏斗b中的NaClO与NaOH混合液缓慢滴入盛有mg尿素的三颈烧瓶a中,边滴加边搅拌,温度迅速升高到120℃。
,将滴液漏斗b中的NaClO与NaOH混合液缓慢滴入盛有mg尿素的三颈烧瓶a中,边滴加边搅拌,温度迅速升高到120℃。
①仪器c的名称为
②生成水合肼的化学方程式为
Ⅱ.验证
 的还原性
的还原性(4)将“步骤二”制得的水合肼配成1000mL溶液,移出25mL于锥形瓶中,滴加2滴淀粉溶液,用0.05mol/L的
 溶液滴定,当滴定完全时,消耗
溶液滴定,当滴定完全时,消耗 溶液VmL。
溶液VmL。①滴定过程中水合肼被氧化为
 ,反应的化学方程式为
,反应的化学方程式为②配成的水合肼的浓度

③
 的产率为
的产率为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】工业上,向 500~600 ℃的铁屑中通入氯气生产无水氯化铁。现用如图所示的装置模拟上述过程进行实验。

(1)写出仪器的名称:a_______ ,b_______ 。
(2)A 中反应的化学方程式为_______ 。C 中反应的化学方程式为_______ 。
(3)装置 B 中加入的试剂是_______ 。
(4)已知:高温时 H2O+C=H2+CO。其中H2O是_______ 剂,C是_______ 剂。
(5)下列四种基本反应类型的反应中,一定是氧化还原反应的是_______ (填序号同下),一定不是氧化还原反应的是_______ ,可能是氧化还原反应得是_______
①化合反应 ②分解反应 ③置换反应 ④复分解反应

(1)写出仪器的名称:a
(2)A 中反应的化学方程式为
(3)装置 B 中加入的试剂是
(4)已知:高温时 H2O+C=H2+CO。其中H2O是
(5)下列四种基本反应类型的反应中,一定是氧化还原反应的是
①化合反应 ②分解反应 ③置换反应 ④复分解反应
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】实验室可以用纯净的氯气和铁粉反应制取少量氯化铁固体,其反应装置示意图如下:
回答下列问题:
(1)A装置可制取氯气,反应前分液漏斗中药品为________ ,圆底烧瓶中药品为________ 。
(2)写出A装置中制取氯气所发生的化学方程式是_____________________________ 。
(3)装置B中盛放的试剂是________________________ 。
(4)装置E的作用是______________________________ 。

回答下列问题:
(1)A装置可制取氯气,反应前分液漏斗中药品为
(2)写出A装置中制取氯气所发生的化学方程式是
(3)装置B中盛放的试剂是
(4)装置E的作用是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表列出了①~⑨九种元素在元素周期表中的位置:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为__________ 。
(2)在①~④四种元素的最高价氧化物对应的水化物中碱性最强的是__________ (填碱的化学式)。
(3)在⑤~⑦三种元素的最简单氢化物中,沸点最高的是__________ (用化学式填空)。
(4)写出⑧的单质与氢氧化钠溶液反应的化学方程式__________ 。
(5)写出①与⑦形成原子个数比为1:1的化合物的电子式__________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ⑤ | ⑥ | ⑦ | |||||
| 三 | ① | ③ | ④ | ⑧ | ⑨ | |||
| 四 | ② |
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为
(2)在①~④四种元素的最高价氧化物对应的水化物中碱性最强的是
(3)在⑤~⑦三种元素的最简单氢化物中,沸点最高的是
(4)写出⑧的单质与氢氧化钠溶液反应的化学方程式
(5)写出①与⑦形成原子个数比为1:1的化合物的电子式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】氯气、“84”消毒液、漂白粉等都是含氯的消毒剂,某化学兴趣小组利用如图装置制备“84”消毒液、漂白粉,并收集纯净干燥的氯气。回答下列问题:

(1)盛装浓盐酸的仪器的名称为___________ ,装置甲中发生反应的化学方程式为___________ 。
(2)装置丁用来收集纯净且干燥的氯气,进气口为___________ (填a或b);装置乙盛装的试剂是___________ 。(填名称)
(3)将氯气通入装置己中制备“84”漂白液,则装置己中发生反应的离子方程式为___________ ,有同学认为装置己还有一个作用,该作用为___________ 。
(4)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为___________ 。

(1)盛装浓盐酸的仪器的名称为
(2)装置丁用来收集纯净且干燥的氯气,进气口为
(3)将氯气通入装置己中制备“84”漂白液,则装置己中发生反应的离子方程式为
(4)装置戊中盛装石灰乳用来制备漂白粉,则装置戊中发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】生活中常用的消毒剂有含氯消毒剂、双氧水等。
Ⅰ.实验室模拟获得少量漂白粉的装置如图

(1)实验室可以用 和浓盐酸反应制取氮气,反应方程式如下:
和浓盐酸反应制取氮气,反应方程式如下:
①浓盐酸在反应中显示出来的性质是___________ ;
②请用双线桥表示该反应电子转移的方向和数目:___________
 ;
;
③D装置的作用是___________ 。
(2)已知:a.氯气和石灰乳在反应的过程中会放出热量。
b.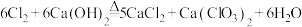
①写出制取漂白粉的化学方程式:___________ 。
②兴趣小组制得的漂白粉中 的含量远超过预期,而
的含量远超过预期,而 含量明显偏低,主要原因可能是
含量明显偏低,主要原因可能是___________ 。
Ⅱ.亚氯酸钠( )是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
)是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
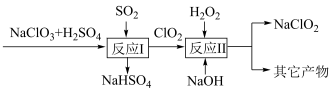
(3)①反应Ⅰ的氧化剂是___________ (写化学式,下同)。
②反应Ⅱ中其它产物除了 外还有
外还有___________ ,当 和
和 的物质的量为
的物质的量为 混合时完全反应,则反应Ⅱ的化学方程式为
混合时完全反应,则反应Ⅱ的化学方程式为___________ 。
Ⅰ.实验室模拟获得少量漂白粉的装置如图

(1)实验室可以用
 和浓盐酸反应制取氮气,反应方程式如下:
和浓盐酸反应制取氮气,反应方程式如下:
①浓盐酸在反应中显示出来的性质是
②请用双线桥表示该反应电子转移的方向和数目:
 ;
;③D装置的作用是
(2)已知:a.氯气和石灰乳在反应的过程中会放出热量。
b.
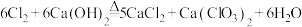
①写出制取漂白粉的化学方程式:
②兴趣小组制得的漂白粉中
 的含量远超过预期,而
的含量远超过预期,而 含量明显偏低,主要原因可能是
含量明显偏低,主要原因可能是Ⅱ.亚氯酸钠(
 )是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
)是一种高效的消毒剂和漂白剂。Mathieson法制备亚氯酸钠的流程如图:
(3)①反应Ⅰ的氧化剂是
②反应Ⅱ中其它产物除了
 外还有
外还有 和
和 的物质的量为
的物质的量为 混合时完全反应,则反应Ⅱ的化学方程式为
混合时完全反应,则反应Ⅱ的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如图所示。
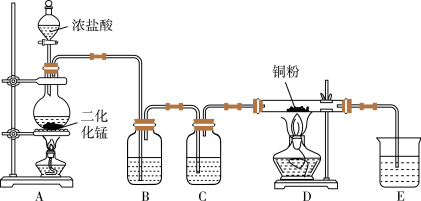
回答下列问题:
(1)写出在A中发生反应的化学方程式为:__ ;
(2)B中选用的试剂是__ ,其作用是__ ;
(3)E中选用的试剂是__ ,其作用是__ ;
(4)若用含有0.2molHCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12L的原因是__ 。

回答下列问题:
(1)写出在A中发生反应的化学方程式为:
(2)B中选用的试剂是
(3)E中选用的试剂是
(4)若用含有0.2molHCl的浓盐酸与足量的MnO2反应制Cl2,制得的Cl2体积(标准状况下)总是小于1.12L的原因是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】已知非金属单质硫(S)是淡黄色固体粉末,难溶于水。为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:

(1)装置A的分液漏斗中盛装的试剂是______ ,烧瓶中加入的试剂是______ 。
(2)画出虚线框内的实验装置图,并注明所加试剂,说明装置的作用______ 。
(3)装置B中盛放的试剂是______ (选填下列所给试剂的代码),
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
化学反应方程式是______ 。
(4)还有哪些事实能够说明氯元素的非金属性比硫元素的非金属性强(试举一例)______ 。

(1)装置A的分液漏斗中盛装的试剂是
(2)画出虚线框内的实验装置图,并注明所加试剂,说明装置的作用
(3)装置B中盛放的试剂是
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
化学反应方程式是
(4)还有哪些事实能够说明氯元素的非金属性比硫元素的非金属性强(试举一例)
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】下列是实验室制取乙炔、洗气和性质实验所需的装置及试剂,按要求回答下列问题:

1)请选出制取乙炔气体所需的装置________ (填字母,选错扣分)
2)如果将产生的气体按照发生、洗气、性质实验装置的顺序从左到右连接起来,请写出接口连接的数字顺序:发生装置出口____ 接 ____ 接____ 接_____ 或_____ 。(填数字)
3)写出制取乙炔的化学方程式:____________________________________________ 。
4)装置C的作用 是________________________________________________________ 。
5)如果要进行乙炔的可燃性实验,首先应该__________________________________ 。

1)请选出制取乙炔气体所需的装置
2)如果将产生的气体按照发生、洗气、性质实验装置的顺序从左到右连接起来,请写出接口连接的数字顺序:发生装置出口
3)写出制取乙炔的化学方程式:
4)装置C的作用 是
5)如果要进行乙炔的可燃性实验,首先应该
您最近一年使用:0次



