某工厂产生的烧渣(主要含 、
、 ,还有一定量的
,还有一定量的 )可用于制绿矾晶体(
)可用于制绿矾晶体( ),其工艺流程如下:
),其工艺流程如下:
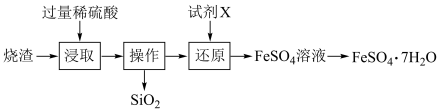
查阅资料: 不溶于水,也不与稀硫酸反应。
不溶于水,也不与稀硫酸反应。
(1) 的名称是
的名称是___________ ,上图“操作”是指一个实验基本操作,其名称为___________ 。
(2)“浸取”步骤中, 、
、 和稀硫酸发生反应的化学方程式分别为:
和稀硫酸发生反应的化学方程式分别为: 、
、___________ 。
(3)为提高“浸取”步骤的反应速率,可采取的具体措施有___________ (写1条,不考虑“搅拌”和“使用催化剂”)。
(4)“还原”步骤的目的是将 转化为
转化为 ,试剂
,试剂 可用
可用 或
或 。
。
①若试剂X是 ,转化原理为
,转化原理为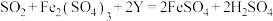 ,则
,则 的化学式是
的化学式是___________ 。
②若试剂 是
是 ,转化原理为
,转化原理为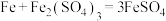 。化工生产中②比①好,其原因是
。化工生产中②比①好,其原因是___________ 。
(5)从 溶液得到
溶液得到 的方法是
的方法是___________ 。
 、
、 ,还有一定量的
,还有一定量的 )可用于制绿矾晶体(
)可用于制绿矾晶体( ),其工艺流程如下:
),其工艺流程如下:
查阅资料:
 不溶于水,也不与稀硫酸反应。
不溶于水,也不与稀硫酸反应。(1)
 的名称是
的名称是(2)“浸取”步骤中,
 、
、 和稀硫酸发生反应的化学方程式分别为:
和稀硫酸发生反应的化学方程式分别为: 、
、(3)为提高“浸取”步骤的反应速率,可采取的具体措施有
(4)“还原”步骤的目的是将
 转化为
转化为 ,试剂
,试剂 可用
可用 或
或 。
。①若试剂X是
 ,转化原理为
,转化原理为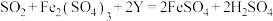 ,则
,则 的化学式是
的化学式是②若试剂
 是
是 ,转化原理为
,转化原理为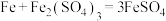 。化工生产中②比①好,其原因是
。化工生产中②比①好,其原因是(5)从
 溶液得到
溶液得到 的方法是
的方法是
更新时间:2023-10-31 11:01:36
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学实验室以一种工业上的废渣(废渣主要含有 和少量 Fe、Al 的氧化物)为原料,制备
和少量 Fe、Al 的氧化物)为原料,制备 .实验流程如图所示:
.实验流程如图所示:

(1)为了加快废渣的酸溶速率,可采取的办法有______ (任写一点),酸溶时废渣中主要成分发生反应的离子方程式为________ 。
(2)加入30% H2O2的目的是_________ 。
(3)用萃取分液的方法除去溶液中的Fe3+,加入30%H2O2后,检验溶液中是否含有Fe2+的最佳试剂是_______ 。
(4)向滤液中加入Na2CO3溶液生成MgCO3沉淀并用蒸馏水洗涤,确认沉淀洗净的操作及现象是___________ 。
 和少量 Fe、Al 的氧化物)为原料,制备
和少量 Fe、Al 的氧化物)为原料,制备 .实验流程如图所示:
.实验流程如图所示: 
(1)为了加快废渣的酸溶速率,可采取的办法有
(2)加入30% H2O2的目的是
(3)用萃取分液的方法除去溶液中的Fe3+,加入30%H2O2后,检验溶液中是否含有Fe2+的最佳试剂是
(4)向滤液中加入Na2CO3溶液生成MgCO3沉淀并用蒸馏水洗涤,确认沉淀洗净的操作及现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】碱性锌锰电池的工作原理:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,其中的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料——MnxZn(1−x)Fe2O4,其工艺流程如下图所示:
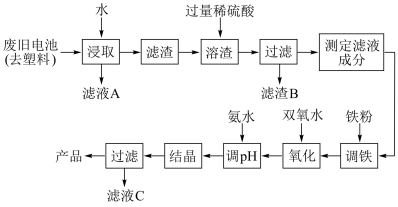
(1)已知MnxZn(1−x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素的化合价为______ 。
(2)“浸取”工序得到的滤液A经蒸发结晶,可以获得化工产品M,M的电子式为_____ 。
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,写出该反应的离子方程式:_______ 。
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式MnxZn(1−x)Fe2O4相符合。
①写出“调铁”工序中发生反应的离子方程式:________________ 、__________________ 。
②若测得滤液的成分为c(Mn2+)+c(Zn2+)=a mol·L−1,c(Fe2+)+c(Fe3+)=b mol·L−1,滤液体积为1 m3,“调铁”工序中,需加入的铁粉质量为___________ kg(忽略溶液体积变化,用含a、b的代数式表示)。
(5)在“氧化”工序中,加入双氧水的目的是______________________ ;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是______________________ 。
(6)用氨水“调pH”后,经“结晶”、“过滤”可得到产品和滤液C,从滤液C中还可分离出一种氮肥,该氮肥的溶液中离子浓度由大到小的排序为______________________ 。

(1)已知MnxZn(1−x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素的化合价为
(2)“浸取”工序得到的滤液A经蒸发结晶,可以获得化工产品M,M的电子式为
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,写出该反应的离子方程式:
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式MnxZn(1−x)Fe2O4相符合。
①写出“调铁”工序中发生反应的离子方程式:
②若测得滤液的成分为c(Mn2+)+c(Zn2+)=a mol·L−1,c(Fe2+)+c(Fe3+)=b mol·L−1,滤液体积为1 m3,“调铁”工序中,需加入的铁粉质量为
(5)在“氧化”工序中,加入双氧水的目的是
(6)用氨水“调pH”后,经“结晶”、“过滤”可得到产品和滤液C,从滤液C中还可分离出一种氮肥,该氮肥的溶液中离子浓度由大到小的排序为
您最近一年使用:0次
【推荐3】尿素[CO(NH2)2]的合成与利用,体现了化学科学与技术的不断进步。
(1) 与
与 在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为
在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为___________ 。
(2)电催化法合成尿素
2021年,科学家设计出一种在 催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。
催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。


①甲醛和羟胺( )缩合生成甲胺(
)缩合生成甲胺( )的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了
)的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了___________ 化学键。
②已知在制备和反应过程中,催化剂表面的电子能自发从 端转移到Bi端,
端转移到Bi端, 能成功吸附在Bi端的原因可能是
能成功吸附在Bi端的原因可能是___________ 。
③实际生产时可忽略步骤Ⅲ可能出现的副产物 和
和 ,原因是
,原因是___________ 。
(3)尿素能应用于脱除烟气中的污染物。控制其他条件相同,将混有 、
、 、
、 、
、 和
和 的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测
的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测 、
、 的脱除率
的脱除率 [
[ ]。
]。
①实验测得,烟气中少量 有利于
有利于 的脱除,这是利用了
的脱除,这是利用了 的
的___________ 性。
②当无 存在,且烟气中
存在,且烟气中 与
与 的物质的量浓度相等时,
的物质的量浓度相等时, 达到最大值。该条件下尿素脱除
达到最大值。该条件下尿素脱除 的化学反应方程式为
的化学反应方程式为___________ 。
③当无 存在,且烟气中
存在,且烟气中 超过一定数值时,测得
超过一定数值时,测得 变为负值,其原因是
变为负值,其原因是___________ 。
(1)
 与
与 在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为
在一定条件下制得尿素,实现了由无机物到有机物的合成,该反应的化学方程式为(2)电催化法合成尿素
2021年,科学家设计出一种在
 催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。
催化剂表面合成尿素的方法,其可能的反应机理如图-1所示。反应部分历程及能量关系如图-2所示。

①甲醛和羟胺(
 )缩合生成甲胺(
)缩合生成甲胺( )的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了
)的实现,为科学家利用碳源和氮源小分子合成尿素提供了基础。这是由于该缩合反应形成了②已知在制备和反应过程中,催化剂表面的电子能自发从
 端转移到Bi端,
端转移到Bi端, 能成功吸附在Bi端的原因可能是
能成功吸附在Bi端的原因可能是③实际生产时可忽略步骤Ⅲ可能出现的副产物
 和
和 ,原因是
,原因是(3)尿素能应用于脱除烟气中的污染物。控制其他条件相同,将混有
 、
、 、
、 、
、 和
和 的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测
的模拟烟气匀速通过装有尿素溶液的装置,在装置出口处检测 、
、 的脱除率
的脱除率 [
[ ]。
]。①实验测得,烟气中少量
 有利于
有利于 的脱除,这是利用了
的脱除,这是利用了 的
的②当无
 存在,且烟气中
存在,且烟气中 与
与 的物质的量浓度相等时,
的物质的量浓度相等时, 达到最大值。该条件下尿素脱除
达到最大值。该条件下尿素脱除 的化学反应方程式为
的化学反应方程式为③当无
 存在,且烟气中
存在,且烟气中 超过一定数值时,测得
超过一定数值时,测得 变为负值,其原因是
变为负值,其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某同学用某种粗盐(含可溶的Ca2+、Mg2+)进行提纯实验,步骤见下图:

请回答:
(1)步骤①和②的操作名称是______________ .
(2)步骤③判断加入盐酸“适量”的方法是__________________________ ;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止________________ ,当蒸发皿中有较多量固体出现时,应________________ ,用余热使水分蒸干.
(3)若固体A中含CaCO3、MgCO3,取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口,小烧杯中观察的现象是________________________ ,写出发生反应的离子方程式_______________________________ .

请回答:
(1)步骤①和②的操作名称是
(2)步骤③判断加入盐酸“适量”的方法是
(3)若固体A中含CaCO3、MgCO3,取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口,小烧杯中观察的现象是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】亚铁氰化钾的化学式为K4[Fe(CN)6],一种用含NaCN废水合成该化合物的主要工艺流程如图:
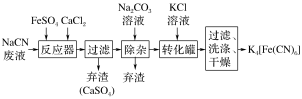
请依据工艺流程图中的信息,回答下列问题:
①在“除杂”步骤中弃渣的主要成分为________ (填化学式)。
②在“反应器”中发生的主要反应的化学方程式为_______________________ 。
③相同温度下溶解度:Na4[Fe(CN)6]________ K4[Fe(CN)6](填“>”“<”或“=”)。

请依据工艺流程图中的信息,回答下列问题:
①在“除杂”步骤中弃渣的主要成分为
②在“反应器”中发生的主要反应的化学方程式为
③相同温度下溶解度:Na4[Fe(CN)6]
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】以高钛渣(主要成分为Ti3O5,含少量SiO2、FeO、Fe2O3)为原料制备白色颜料TiO2的一种工艺流程如下:

已知:Na2TiO3难溶于碱性溶液;H2TiO3中的杂质Fe2+比Fe3+更易水洗除去。
(1)熔盐:
①为加快反应速率,在维持反应物颗粒大小、反应温度一定的条件下,可采取的措施是__________ 。
②NaOH固体与Ti3O5在空气中加热至500~550 ℃时生成Na2TiO3,该反应的化学方程式为_________ 。
(2)过滤:
①“滤液”中主要溶质为NaOH,还含有少量________ (填化学式)。
②除杂后的滤液中获得的NaOH可循环利用,则“水浸”时,用水量不宜过大的主要原因是_________ 。
(3)水解:“酸溶”后获得的TiOSO4经加热煮沸,生成难溶于水的H2TiO3,该反应的化学方程式为______ 。
(4)脱色:H2TiO3中因存在少量Fe(OH)3而影响TiO2产品的颜色,“脱色”步骤中Ti2(SO4)3的作用是_________ 。

已知:Na2TiO3难溶于碱性溶液;H2TiO3中的杂质Fe2+比Fe3+更易水洗除去。
(1)熔盐:
①为加快反应速率,在维持反应物颗粒大小、反应温度一定的条件下,可采取的措施是
②NaOH固体与Ti3O5在空气中加热至500~550 ℃时生成Na2TiO3,该反应的化学方程式为
(2)过滤:
①“滤液”中主要溶质为NaOH,还含有少量
②除杂后的滤液中获得的NaOH可循环利用,则“水浸”时,用水量不宜过大的主要原因是
(3)水解:“酸溶”后获得的TiOSO4经加热煮沸,生成难溶于水的H2TiO3,该反应的化学方程式为
(4)脱色:H2TiO3中因存在少量Fe(OH)3而影响TiO2产品的颜色,“脱色”步骤中Ti2(SO4)3的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】某化学兴趣小组模拟工业上从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3等杂质)中提取氧化铝的工艺流程如下:(已知溶液D中通入过量的CO2得到白色沉淀)

请回答下列问题:
(1)操作Ⅰ的名称为________ 。
(2)不溶物A是_________________ (填化学式),写出A与氢氧化钠溶液反应的离子方程式_________________________________ 。
(3)+3价的铝常或多或少地置换硅酸盐中+4价的硅而形成铝硅酸盐。已知某种铝硅酸盐主要成分的化学式为Al2Si2O5(OH)4,请将其改写成氧化物的组合形式________ 。
(4)溶液D中Al元素的主要存在形式为_____________ (填离子符号)
(5)写出E→G的化学方程式____________________________________________ 。

请回答下列问题:
(1)操作Ⅰ的名称为
(2)不溶物A是
(3)+3价的铝常或多或少地置换硅酸盐中+4价的硅而形成铝硅酸盐。已知某种铝硅酸盐主要成分的化学式为Al2Si2O5(OH)4,请将其改写成氧化物的组合形式
(4)溶液D中Al元素的主要存在形式为
(5)写出E→G的化学方程式
您最近一年使用:0次
【推荐2】锆(40Zr)是现代工业中重要的金属原料,具有良好的可塑性,其抗蚀性能强于钛。以锆英石(主要成分是ZrSiO4,还含有少量A12O3、SiO2、Fe2O3等杂质)为原料生产锆及其化合物的流程如图所示:

(1)分馏属于_______ (填“物理变化”或“化学变化”)。
(2)锆英石_______ (填“能”或“不能”)直接用稀盐酸浸取后再分馏,理由是_______ 。
(3)“高温气化”中ZrSiO4发生反应得到ZrC14的反应的化学方程式为_______ 。
(4)流程中ZrC14与水反应后经过滤、洗涤、干燥等操作可获得ZrOC12·8H2O,检验该物质是否洗涤干净的实验操作为_______ 。
(5)工业上使用惰性电极电解K2ZrF6与KC1组成的熔盐来制取金属锆。阳极上的电极反应式为_______ ,每转移0.4mole-,理论上阴极增加的质量为_______ 。

(1)分馏属于
(2)锆英石
(3)“高温气化”中ZrSiO4发生反应得到ZrC14的反应的化学方程式为
(4)流程中ZrC14与水反应后经过滤、洗涤、干燥等操作可获得ZrOC12·8H2O,检验该物质是否洗涤干净的实验操作为
(5)工业上使用惰性电极电解K2ZrF6与KC1组成的熔盐来制取金属锆。阳极上的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】焦亚硫酸钠 是常用的抗氧化剂,在空气中、受热时均易分解。
是常用的抗氧化剂,在空气中、受热时均易分解。
(1)化学兴趣小组同学利用如图所示装置(部分夹持装置已略去,实验前已除去装置中的空气)制取 并探究
并探究 的性质。
的性质。

Ⅰ.打开 和
和 ,关闭
,关闭 ,制取
,制取
① 中
中 元素化合价为
元素化合价为 ,其中
,其中 的化合价为
的化合价为___________ ;装置C中干燥管的作用是___________ 。
② 中通入过量
中通入过量 充分反应后,经冷却结晶时发生反应
充分反应后,经冷却结晶时发生反应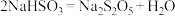 可获得
可获得 晶体。
晶体。 中生成
中生成 的化学方程式为
的化学方程式为___________ 。
③ 中所得
中所得 晶体常用饱和
晶体常用饱和 水溶液洗涤。用饱和
水溶液洗涤。用饱和 水溶液洗涤的目的除洗去产物表面的杂质离子外还有
水溶液洗涤的目的除洗去产物表面的杂质离子外还有___________ 。
II.更换 瓶中的溶液,探究
瓶中的溶液,探究 的性质。
的性质。
④将 中溶液更换为品红的乙醇溶液,无明显现象;而将
中溶液更换为品红的乙醇溶液,无明显现象;而将 通入品红的水溶液中,溶液褪色。由此可推知,使品红水溶液褪色的物质可能是
通入品红的水溶液中,溶液褪色。由此可推知,使品红水溶液褪色的物质可能是___________ 。(写化学式)
(2)葡萄酒中常加入 作抗氧化剂。测定某葡萄酒中
作抗氧化剂。测定某葡萄酒中 残留量的实验步骤如下:取
残留量的实验步骤如下:取 葡萄酒样品,用
葡萄酒样品,用 的
的 标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液
标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液 ,已知滴定过程中发生的反应为:
,已知滴定过程中发生的反应为: (未配平)。计算该葡萄酒中
(未配平)。计算该葡萄酒中 的残留量
的残留量___________ (以 为单位,写出计算过程)。
为单位,写出计算过程)。
 是常用的抗氧化剂,在空气中、受热时均易分解。
是常用的抗氧化剂,在空气中、受热时均易分解。(1)化学兴趣小组同学利用如图所示装置(部分夹持装置已略去,实验前已除去装置中的空气)制取
 并探究
并探究 的性质。
的性质。
Ⅰ.打开
 和
和 ,关闭
,关闭 ,制取
,制取
①
 中
中 元素化合价为
元素化合价为 ,其中
,其中 的化合价为
的化合价为②
 中通入过量
中通入过量 充分反应后,经冷却结晶时发生反应
充分反应后,经冷却结晶时发生反应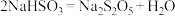 可获得
可获得 晶体。
晶体。 中生成
中生成 的化学方程式为
的化学方程式为③
 中所得
中所得 晶体常用饱和
晶体常用饱和 水溶液洗涤。用饱和
水溶液洗涤。用饱和 水溶液洗涤的目的除洗去产物表面的杂质离子外还有
水溶液洗涤的目的除洗去产物表面的杂质离子外还有II.更换
 瓶中的溶液,探究
瓶中的溶液,探究 的性质。
的性质。④将
 中溶液更换为品红的乙醇溶液,无明显现象;而将
中溶液更换为品红的乙醇溶液,无明显现象;而将 通入品红的水溶液中,溶液褪色。由此可推知,使品红水溶液褪色的物质可能是
通入品红的水溶液中,溶液褪色。由此可推知,使品红水溶液褪色的物质可能是(2)葡萄酒中常加入
 作抗氧化剂。测定某葡萄酒中
作抗氧化剂。测定某葡萄酒中 残留量的实验步骤如下:取
残留量的实验步骤如下:取 葡萄酒样品,用
葡萄酒样品,用 的
的 标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液
标准液滴定至恰好完全反应(以淀粉溶液作指示剂),消耗碘标准液 ,已知滴定过程中发生的反应为:
,已知滴定过程中发生的反应为: (未配平)。计算该葡萄酒中
(未配平)。计算该葡萄酒中 的残留量
的残留量 为单位,写出计算过程)。
为单位,写出计算过程)。
您最近一年使用:0次



