工业中制取高铁酸钾( ),是先制取高铁酸钠,然后在低温下,往高铁酸钠溶液中加入KOH至饱和就可以析出高铁酸钾。
),是先制取高铁酸钠,然后在低温下,往高铁酸钠溶液中加入KOH至饱和就可以析出高铁酸钾。
湿法制备 的主要反应为:
的主要反应为: ;
;
干法制备 的主要反应为:
的主要反应为: 。
。
下列有关说法不正确的是
 ),是先制取高铁酸钠,然后在低温下,往高铁酸钠溶液中加入KOH至饱和就可以析出高铁酸钾。
),是先制取高铁酸钠,然后在低温下,往高铁酸钠溶液中加入KOH至饱和就可以析出高铁酸钾。湿法制备
 的主要反应为:
的主要反应为: ;
;干法制备
 的主要反应为:
的主要反应为: 。
。下列有关说法不正确的是
A.湿法和干法制备中,生成质量相同的 转移电子数目不同 转移电子数目不同 |
| B.高铁酸钾在低温下的溶解度比高铁酸钠的溶解度小 |
C.干法制备的主要反应中,每生成0.5mol ,转移电子数为 ,转移电子数为 |
D. 处理水时,既能杀菌消毒,生成的 处理水时,既能杀菌消毒,生成的 胶体还能吸附水中的悬浮杂质 胶体还能吸附水中的悬浮杂质 |
更新时间:2023-12-14 08:55:40
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】将amol的铁铜混合物投入到200mL2mol/L的稀HNO3中,充分反应后(假定还原产物只有NO)金属无剩余,下列说法正确的是 ( )
| A.被还原的HNO不可能是2a/3mol |
| B.溶液中剩余的n(NO3一)≤(0.4—2a/3)mol |
| C.溶液中不可能同时存在Fe2+、Fe3+、Cu2+ |
| D.当被还原的硝酸为0.8amol,则溶液中一定含有Fe2+ |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】还原沉淀法是处理含铬(含Cr2O 和CrO
和CrO )工业废水的常用方法,过程如下:
)工业废水的常用方法,过程如下:
CrO
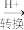 Cr2O
Cr2O
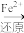 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
已知转换过程中的反应为:2CrO (aq)+2H+(aq)
(aq)+2H+(aq)  Cr2O
Cr2O (aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO
(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO 有10/11转化为Cr2O
有10/11转化为Cr2O ,下列说法不正确的是
,下列说法不正确的是
 和CrO
和CrO )工业废水的常用方法,过程如下:
)工业废水的常用方法,过程如下:CrO

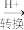 Cr2O
Cr2O
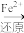 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓已知转换过程中的反应为:2CrO
 (aq)+2H+(aq)
(aq)+2H+(aq)  Cr2O
Cr2O (aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO
(aq)+H2O(l)。转化后所得溶液中铬元素的含量为28.6 g/L,CrO 有10/11转化为Cr2O
有10/11转化为Cr2O ,下列说法不正确的是
,下列说法不正确的是| A.溶液颜色保持不变,说明上述可逆反应达到平衡状态 |
| B.若用绿矾(FeSO4·7H2O)作还原剂,处理1 L废水,至少需要458.7 g |
| C.常温下转化反应的平衡常数K=1×1014,则转化后所得溶液的pH=5 |
| D.常温下Ksp[Cr(OH)3]=1×10-32,要使处理后废水中的c(Cr3+)降至1×10-5 mol·L-1,应调溶液的pH=5 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】Na2FeO4是一种高效的水处理剂,下列用于解释事实的离子方程式中不正确的是
| A.Na2FeO4在酸性溶液中不稳定,与水反应生成Fe3+和O2,离子方程式为:4FeO42-+10H2O+4Fe3+=== 20OH-+3O2↑ |
| B.工业上可用FeCl3、NaOH、NaClO三种物质反应制得Na2FeO4离子方程式为:2Fe3++10OH-+3ClO-===2FeO42-+3Cl-+5H2O |
| C.Na2FeO4消毒杀菌时得到的Fe3+可以净水,Fe3+能产生净水物质的原因是:Fe3++3H2O===Fe(OH)3(胶体)+3H+ |
| D.工业上可用铁做阳极,电解浓NaOH溶液的方法制Na2FeO4,阳极的电极反应为:Fe-6e-+8OH-===FeO42-+4H2O |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知反应: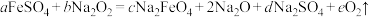 ,
, 。下列关于该反应的说法错误的是
。下列关于该反应的说法错误的是
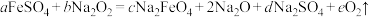 ,
, 。下列关于该反应的说法错误的是
。下列关于该反应的说法错误的是A. 可以对水体进行杀菌消毒、净化 可以对水体进行杀菌消毒、净化 |
B. 在该反应中既是氧化剂又是还原剂 在该反应中既是氧化剂又是还原剂 |
C.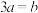 |
D.每生成 ,转移4mol电子 ,转移4mol电子 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】高铁酸钾是一种重要的绿色净水剂,具有净水和消毒双重功能。某课外学习小组设计如图所示方案制备高铁酸钾。下列说法不正确的是
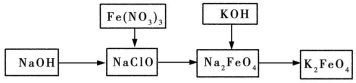
| A.高铁酸钾中铁元素的化合价为+6,具有强氧化性 |
| B.反应2Fe3++3ClO−+10OH−=2FeO42-+3Cl−+5H2O中,生成2 mol FeO42-时,转移6 mol 电子 |
| C.制备高铁酸钾的化学方程式为2KOH+Na2FeO4=K2FeO4+2NaOH,根据复分解反应原理,高铁酸钠的溶解度大于高铁酸钾的溶解度 |
| D.明矾、硫酸铁、高铁酸钾都能净水,其净水原理完全相同 |
您最近半年使用:0次
【推荐1】工业上以铬铁矿[主要成分是 ]为原料冶炼铬的某流程中发生反应为:
]为原料冶炼铬的某流程中发生反应为: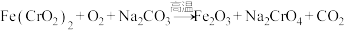 (未配平),该反应中Cr只有+3、+6两种价态。下列关于该反应的说法中正确的是
(未配平),该反应中Cr只有+3、+6两种价态。下列关于该反应的说法中正确的是
 ]为原料冶炼铬的某流程中发生反应为:
]为原料冶炼铬的某流程中发生反应为: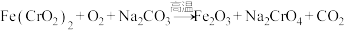 (未配平),该反应中Cr只有+3、+6两种价态。下列关于该反应的说法中正确的是
(未配平),该反应中Cr只有+3、+6两种价态。下列关于该反应的说法中正确的是A. 中Fe为+3价 中Fe为+3价 |
| B.反应中氧化剂与还原剂的物质的量之比为2∶3 |
C.反应中每转移4.0mol ,将有1.0mol的 ,将有1.0mol的 被消耗 被消耗 |
D.反应中每氧化1.0mol的Cr原子,将生成2.0mol的 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,下图为钠投入液氨中的溶剂化图。钠沉入液氨中,快速得到深蓝色溶液,并慢慢产生气泡。下列说法错误的是


| A.钠的密度比液氨大 |
| B.溶液的导电性增强 |
| C.0.1mol钠投入液氨生成0.01molH2时,Na共失去0.02mol电子 |
| D.钠和液氨可发生以下反应:2NH3 + 2Na=2NaNH2 + H2↑ |
您最近半年使用:0次

 可知氧化性
可知氧化性
 中氧化剂与还原剂物质的量之比为
中氧化剂与还原剂物质的量之比为
 和
和 混合溶液中加入少量锌粉,
混合溶液中加入少量锌粉, 优先被氧化
优先被氧化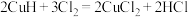 中,每转移6个电子,被氢元素还原的
中,每转移6个电子,被氢元素还原的 为1个
为1个

