合成氨反应 是目前最有效的工业固氮方法,解决数亿人口生存问题。
是目前最有效的工业固氮方法,解决数亿人口生存问题。
(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用*标注。
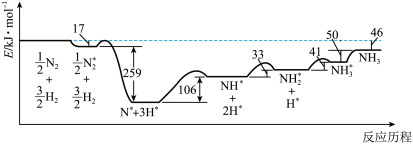
该反应在___________ (填“任何”“较低温”“较高温”)条件下可以自发进行;上述历程中反应速率最慢的步骤的方程式为___________ 。
(2)在T℃、压强为0.9MPa条件下,向一恒压密闭容器中通入 的混合气体,体系中各气体的含量与时间变化关系如图所示。已知:分压=总压×体积分数。
的混合气体,体系中各气体的含量与时间变化关系如图所示。已知:分压=总压×体积分数。
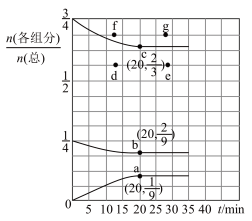
①以下叙述不能 说明该条件下反应达到平衡状态的是___________ (填字母)。
A.氨气的体积分数保持不变 B.容器中 保持不变
保持不变
C.气体平均相对分子质量保持不变 D.气体密度保持不变
E.
②反应20min时达到平衡,则0~20min内
________  ,
,
_________ 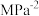 。(
。( 为以分压表示的平衡常数,代入数据列出计算式,不必化简)
为以分压表示的平衡常数,代入数据列出计算式,不必化简)
③若起始条件相同,在恒容容器中发生反应,则达到平衡时 的含量符合图中
的含量符合图中___________ 点(填“d”“e”“f”或“g”)。
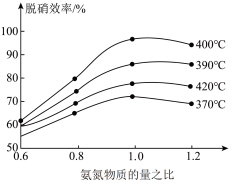
(3)氨化脱硝过程发生反应
 ,请根据下图分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
,请根据下图分析420℃的脱硝效率低于390℃的脱硝效率可能的原因___________ 。
 是目前最有效的工业固氮方法,解决数亿人口生存问题。
是目前最有效的工业固氮方法,解决数亿人口生存问题。(1)反应历程中各步势能变化如图所示,其中吸附在催化剂表面的物种用*标注。

该反应在
(2)在T℃、压强为0.9MPa条件下,向一恒压密闭容器中通入
 的混合气体,体系中各气体的含量与时间变化关系如图所示。已知:分压=总压×体积分数。
的混合气体,体系中各气体的含量与时间变化关系如图所示。已知:分压=总压×体积分数。
①以下叙述
A.氨气的体积分数保持不变 B.容器中
 保持不变
保持不变C.气体平均相对分子质量保持不变 D.气体密度保持不变
E.

②反应20min时达到平衡,则0~20min内

 ,
,
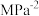 。(
。( 为以分压表示的平衡常数,代入数据列出计算式,不必化简)
为以分压表示的平衡常数,代入数据列出计算式,不必化简)③若起始条件相同,在恒容容器中发生反应,则达到平衡时
 的含量符合图中
的含量符合图中(3)氨化脱硝过程发生反应

 ,请根据下图分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
,请根据下图分析420℃的脱硝效率低于390℃的脱硝效率可能的原因
更新时间:2023-12-12 11:12:03
|
相似题推荐
【推荐1】乙醇水蒸气重整制氢是制备氢气的常用方法,体系中发生的主要反应有:
I.C2H5OH(g)+H2O(g)=2CO(g)+4H2(g) △H1
II.C2H5OH(g)+3H2O(g)=2CO2(g)+6H2(g) △H2=+173kJ·mol-1
III.CO(g)+H2O(g)=CO2(g)+H2(g) △H3=-41.2kJ·mol-1
IV.C2H5OH(g)+2H2(g)=2CH4(g)+H2O(g) △H4=-156.2kJ·mol-1
(1)△H1=____ kJ·mol-1。
(2)压强为100kPa的条件下,图1是平衡时体系中各产物的物质的量分数与温度的关系,图2是H2的平衡产率与温度及起始时 的关系。
的关系。
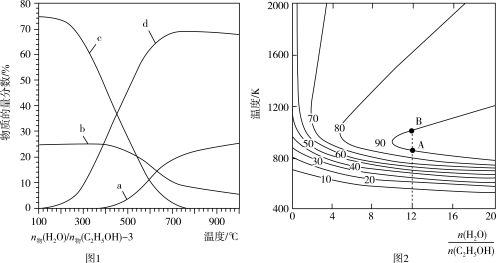
①图1中c线对应的产物为____ (填“CO2”、“H2”或“CH4”)。
②图2中B点H2的产率与A点相等的原因是___ 。
(3)反应温度T℃、0.1MPa的恒压密闭容器中,充入1mol乙醇和xmolH2O(g),若只发生反应CH3CH2OH(g)+3H2O(g) 2CO2(g)+6H2(g),平衡时,乙醇转化率为α,CO2的压强为
2CO2(g)+6H2(g),平衡时,乙醇转化率为α,CO2的压强为____ MPa,反应平衡常数Kp=____ (以分压表示,分压=总压×物质的量分数。列出计算式即可)
(4)CH3CH2OH(g)在催化剂Rh/CeO2上反应制取氢气的机理如图:
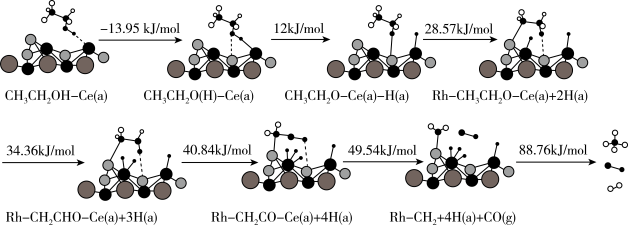
①出生成CO(g)步骤的化学方程式____ 。
②下列措施可以提高CH3CH2OH在催化剂表面吸附率的有____ (填标号)。
a..减小乙醇蒸气的分压 b.增大催化剂的比表面积
I.C2H5OH(g)+H2O(g)=2CO(g)+4H2(g) △H1
II.C2H5OH(g)+3H2O(g)=2CO2(g)+6H2(g) △H2=+173kJ·mol-1
III.CO(g)+H2O(g)=CO2(g)+H2(g) △H3=-41.2kJ·mol-1
IV.C2H5OH(g)+2H2(g)=2CH4(g)+H2O(g) △H4=-156.2kJ·mol-1
(1)△H1=
(2)压强为100kPa的条件下,图1是平衡时体系中各产物的物质的量分数与温度的关系,图2是H2的平衡产率与温度及起始时
 的关系。
的关系。
①图1中c线对应的产物为
②图2中B点H2的产率与A点相等的原因是
(3)反应温度T℃、0.1MPa的恒压密闭容器中,充入1mol乙醇和xmolH2O(g),若只发生反应CH3CH2OH(g)+3H2O(g)
 2CO2(g)+6H2(g),平衡时,乙醇转化率为α,CO2的压强为
2CO2(g)+6H2(g),平衡时,乙醇转化率为α,CO2的压强为(4)CH3CH2OH(g)在催化剂Rh/CeO2上反应制取氢气的机理如图:

①出生成CO(g)步骤的化学方程式
②下列措施可以提高CH3CH2OH在催化剂表面吸附率的有
a..减小乙醇蒸气的分压 b.增大催化剂的比表面积
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】苯乙烯是合成树脂、离子交换树脂及合成橡胶等的重要单体,常用乙苯为原料合成。
(1)逆水煤气变换耦合反应:CO2和乙苯为原料制备苯乙烯的机理如下:
 (g)
(g) H2(g) +
H2(g) +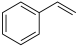 (g) ΔH= +117.6 kJ/mol
(g) ΔH= +117.6 kJ/mol
CO2(g)+H2(g) = CO(g)+ H2O(g) ΔH= +41.2 kJ/mol
则 CO2(g)+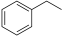 (g)
(g)
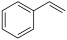 (g)+CO(g)+H2O(g) 的ΔH为
(g)+CO(g)+H2O(g) 的ΔH为_______ 。
(2)乙苯直接脱氢制苯乙烯,反应原理如下:
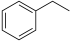 (g)
(g) H2(g) +
H2(g) + (g) ΔH= +123.5 kJ/mol
(g) ΔH= +123.5 kJ/mol
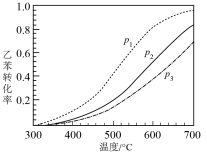
反应在不同压强下进行,实验测得乙苯的平衡转化率随温度(T)的变化关系如图所示,压强(p1、p2、p3)由大到小的顺序为_______ ,理由是_______ 。
(3)乙苯脱氢耦合二氧化碳转化。Ar气氛下,高价态的钒镁氧化物晶体(V)作为的催化活性中心进行乙苯脱氢,耦合CO2转化为CO,实现晶格氧再生和二氧化碳转化,反应机理如图所示:

用简要的文字描述乙苯脱氢耦合二氧化碳转化过程_______ 。
(4)含苯乙烯的废水的排放会对环境造成严重的污染,现采用电解法进行处理,其工作原理如下图(电解液是含苯乙烯和硫酸的废水,pH=6.2), 已知:·OH(羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成CO2和H2O。

①M连接电源的_______ (“正极”或“负极”)。
②苯乙烯被·OH氧化的化学反应方程式为_______ 。
(1)逆水煤气变换耦合反应:CO2和乙苯为原料制备苯乙烯的机理如下:
 (g)
(g) H2(g) +
H2(g) + (g) ΔH= +117.6 kJ/mol
(g) ΔH= +117.6 kJ/molCO2(g)+H2(g) = CO(g)+ H2O(g) ΔH= +41.2 kJ/mol
则 CO2(g)+
 (g)
(g)
 (g)+CO(g)+H2O(g) 的ΔH为
(g)+CO(g)+H2O(g) 的ΔH为(2)乙苯直接脱氢制苯乙烯,反应原理如下:
 (g)
(g) H2(g) +
H2(g) + (g) ΔH= +123.5 kJ/mol
(g) ΔH= +123.5 kJ/mol反应在不同压强下进行,实验测得乙苯的平衡转化率随温度(T)的变化关系如图所示,压强(p1、p2、p3)由大到小的顺序为

(3)乙苯脱氢耦合二氧化碳转化。Ar气氛下,高价态的钒镁氧化物晶体(V)作为的催化活性中心进行乙苯脱氢,耦合CO2转化为CO,实现晶格氧再生和二氧化碳转化,反应机理如图所示:

用简要的文字描述乙苯脱氢耦合二氧化碳转化过程
(4)含苯乙烯的废水的排放会对环境造成严重的污染,现采用电解法进行处理,其工作原理如下图(电解液是含苯乙烯和硫酸的废水,pH=6.2), 已知:·OH(羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成CO2和H2O。

①M连接电源的
②苯乙烯被·OH氧化的化学反应方程式为
您最近一年使用:0次
【推荐3】我国力争于2030年前做到“碳达峰”,2060年前实现“碳中和”,因此 的综合利用是研究热点之一、乙醇是一种重要的燃料与化工原料,现以
的综合利用是研究热点之一、乙醇是一种重要的燃料与化工原料,现以 为原料探究制备乙醇。回答下列问题:
为原料探究制备乙醇。回答下列问题:
(1)已知 、
、 的燃烧热分别为
的燃烧热分别为 、
、 ,
, ,
, ,则
,则
___________ 。
(2) ,该反应的Arrhenius经验公式的实验数据如图中曲线m所示,已知Arrhenius经验公式为
,该反应的Arrhenius经验公式的实验数据如图中曲线m所示,已知Arrhenius经验公式为 (
( 为活化能,假设受温度影响忽略不计,k为速率常数,R和C为常数),则该反应的活化能
为活化能,假设受温度影响忽略不计,k为速率常数,R和C为常数),则该反应的活化能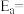
___________  。当改变外界条件时,实验数据如图中的曲线n所示,则实验可能改变的外界条件是
。当改变外界条件时,实验数据如图中的曲线n所示,则实验可能改变的外界条件是___________ 。

(3)为研究反应 ,某科研小组设计了以下三种已装有固体催化剂的密闭容器装置:
,某科研小组设计了以下三种已装有固体催化剂的密闭容器装置:

在初始体积与温度相同的条件下,甲、乙、丙中均按 和
和 投料,达平衡时,三个容器中
投料,达平衡时,三个容器中 的气体体积分数从大到小的顺序为
的气体体积分数从大到小的顺序为___________ (用“甲、乙、丙”表示)。
(4)在恒容密闭容器中,起始充入 和
和 ,发生反应
,发生反应 ,在体系压强为
,在体系压强为 ,反应达到平衡时,四种组分的气体体积分数随温度T的变化如图所示。图中表示
,反应达到平衡时,四种组分的气体体积分数随温度T的变化如图所示。图中表示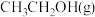 变化的曲线是
变化的曲线是___________ (填“a”“b”“c”或“d”);在温度为 时,
时, 平衡转化率为
平衡转化率为___________ (保留三位有效数字),列出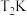 时该反应的平衡常数的计算式
时该反应的平衡常数的计算式
___________ 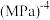 (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。

 的综合利用是研究热点之一、乙醇是一种重要的燃料与化工原料,现以
的综合利用是研究热点之一、乙醇是一种重要的燃料与化工原料,现以 为原料探究制备乙醇。回答下列问题:
为原料探究制备乙醇。回答下列问题:(1)已知
 、
、 的燃烧热分别为
的燃烧热分别为 、
、 ,
, ,
, ,则
,则
(2)
 ,该反应的Arrhenius经验公式的实验数据如图中曲线m所示,已知Arrhenius经验公式为
,该反应的Arrhenius经验公式的实验数据如图中曲线m所示,已知Arrhenius经验公式为 (
( 为活化能,假设受温度影响忽略不计,k为速率常数,R和C为常数),则该反应的活化能
为活化能,假设受温度影响忽略不计,k为速率常数,R和C为常数),则该反应的活化能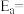
 。当改变外界条件时,实验数据如图中的曲线n所示,则实验可能改变的外界条件是
。当改变外界条件时,实验数据如图中的曲线n所示,则实验可能改变的外界条件是
(3)为研究反应
 ,某科研小组设计了以下三种已装有固体催化剂的密闭容器装置:
,某科研小组设计了以下三种已装有固体催化剂的密闭容器装置:
在初始体积与温度相同的条件下,甲、乙、丙中均按
 和
和 投料,达平衡时,三个容器中
投料,达平衡时,三个容器中 的气体体积分数从大到小的顺序为
的气体体积分数从大到小的顺序为(4)在恒容密闭容器中,起始充入
 和
和 ,发生反应
,发生反应 ,在体系压强为
,在体系压强为 ,反应达到平衡时,四种组分的气体体积分数随温度T的变化如图所示。图中表示
,反应达到平衡时,四种组分的气体体积分数随温度T的变化如图所示。图中表示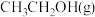 变化的曲线是
变化的曲线是 时,
时, 平衡转化率为
平衡转化率为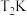 时该反应的平衡常数的计算式
时该反应的平衡常数的计算式
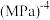 (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】运用化学反应原理研究合成氨反应有重要意义。请回答下列问题,
(1)生成氢气:将水蒸气通过红热的炭即产生水煤气。C(s)+H2O(g)⇌H2(g)+CO(g) ΔH= +131.3 kJ·mol-1, ΔS = +133.7 J·mol-1·K-1,该反应在低温下___________ (“能”或“不能”)自发进行。
(2)已知在T ℃时,反应N2(g)+3H2(g)⇌2NH3(g)的平衡常数K = 0.5,相关化学键键能数据如表:
①T℃时, 2NH3(g)⇌N2(g)+3H2(g)的ΔH =___________ 。
②T℃时,在1L密闭容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为4 mol 、2 mol 、4 mol,则此时反应v正(N2)___________ v逆(N2)(填“>”“<”“=”或“不能确定” )。。
(3)近期,我国科学家为了解决合成氨反应速率和平衡产率的矛盾,选择使用Fe-TiO2-xHy双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为547℃,而TiO2-xHy的温度为415℃)。结合图示解释该双催化剂的工作原理___________ 。________________ 。
(5)以氨为原料生产尿素的方程式为2NH3(g)+CO2(g)⇌CO(NH2)2(1)+H2O(g)。
①为进一步提高NH3的平衡转化率,下列措施能达到目的的是___________ (填字母)。
A.增大CO2的浓度 B.增大压强
C.及时转移生成的尿素 D.使用更高效的催化剂
②尿素的合成分两步进行:
a.2NH3(g)+CO2(g)⇌NH2COONH4 (1) ΔH =-117 kJ/mol
b.NH2COONH4(1)⇌CO(NH2)2(1)+H2O(g) ΔH = +15 kJ/mol,
第一步反应速率快,可判断活化能较大的是___________ (填“第一步”或“第二步”)。
③某实验小组为了模拟工业合成尿素,在恒温恒容的真空密闭容器中充入一定量的CO2和NH3发生反应: 2NH3(g)+CO2(g)⇌CO(NH2)2(1)+H2O(g),反应过程中NH3的体积分数如图所示。实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数___________ (MPa)-2(已知:分压=总压 ×体积分数)。
(1)生成氢气:将水蒸气通过红热的炭即产生水煤气。C(s)+H2O(g)⇌H2(g)+CO(g) ΔH= +131.3 kJ·mol-1, ΔS = +133.7 J·mol-1·K-1,该反应在低温下
(2)已知在T ℃时,反应N2(g)+3H2(g)⇌2NH3(g)的平衡常数K = 0.5,相关化学键键能数据如表:
| 化学键 | N≡N | H-H | N-H |
| 键能/(kJ·mol-1) | 946 | 436 | 390.8 |
②T℃时,在1L密闭容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为4 mol 、2 mol 、4 mol,则此时反应v正(N2)
(3)近期,我国科学家为了解决合成氨反应速率和平衡产率的矛盾,选择使用Fe-TiO2-xHy双催化剂,通过光辐射产生温差(如体系温度为495℃时,Fe的温度为547℃,而TiO2-xHy的温度为415℃)。结合图示解释该双催化剂的工作原理

(5)以氨为原料生产尿素的方程式为2NH3(g)+CO2(g)⇌CO(NH2)2(1)+H2O(g)。
①为进一步提高NH3的平衡转化率,下列措施能达到目的的是
A.增大CO2的浓度 B.增大压强
C.及时转移生成的尿素 D.使用更高效的催化剂
②尿素的合成分两步进行:
a.2NH3(g)+CO2(g)⇌NH2COONH4 (1) ΔH =-117 kJ/mol
b.NH2COONH4(1)⇌CO(NH2)2(1)+H2O(g) ΔH = +15 kJ/mol,
第一步反应速率快,可判断活化能较大的是
③某实验小组为了模拟工业合成尿素,在恒温恒容的真空密闭容器中充入一定量的CO2和NH3发生反应: 2NH3(g)+CO2(g)⇌CO(NH2)2(1)+H2O(g),反应过程中NH3的体积分数如图所示。实验测得体系平衡时的压强为10MPa,计算该反应的平衡常数

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】甲烷制甲醇具有重大的研究价值。
(1)合成气制甲醇

①该反应在_______ 下自发进行(填“高温”、“低温”或“任意温度”)。
②378 K时,0.5 L刚性容器中通入1 mol CO和2 mol ,平衡时压强变为原来的
,平衡时压强变为原来的 ,则该反应的平衡常数
,则该反应的平衡常数
_______ 。
(2)甲烷重整制合成气,主要反应如下:
ⅰ.

ⅱ.

各反应平衡常数与温度的关系如图。

①
_______ 0(填“>”或“<”),理由是_______ 。
②通过调整投料比可调控平衡时合成气 的值。1000 K,平衡时
的值。1000 K,平衡时 ,则
,则
_______ ,应控制投料比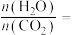
_______ 。
(3)我国科学家研发的一种Au/BP催化剂,可将甲烷定向氧化为甲醇。催化剂的作用机理:
ⅰ.光照条件下, ;
;
ⅱ.黑暗体系 被氧化的反应机理如图。
被氧化的反应机理如图。

①活化 中C-H键的微粒是
中C-H键的微粒是_______ (填“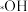 ”或“
”或“ ”)。
”)。
②该催化剂能够有效减少甲醇进一步被氧化的原因是V→TS4的能垒高于_______ 。
(1)合成气制甲醇


①该反应在
②378 K时,0.5 L刚性容器中通入1 mol CO和2 mol
 ,平衡时压强变为原来的
,平衡时压强变为原来的 ,则该反应的平衡常数
,则该反应的平衡常数
(2)甲烷重整制合成气,主要反应如下:
ⅰ.


ⅱ.


各反应平衡常数与温度的关系如图。

①

②通过调整投料比可调控平衡时合成气
 的值。1000 K,平衡时
的值。1000 K,平衡时 ,则
,则
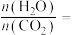
(3)我国科学家研发的一种Au/BP催化剂,可将甲烷定向氧化为甲醇。催化剂的作用机理:
ⅰ.光照条件下,
 ;
;ⅱ.黑暗体系
 被氧化的反应机理如图。
被氧化的反应机理如图。
①活化
 中C-H键的微粒是
中C-H键的微粒是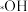 ”或“
”或“ ”)。
”)。②该催化剂能够有效减少甲醇进一步被氧化的原因是V→TS4的能垒高于
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】2021年国务院政府工作报告指出,要做好碳达峰、碳中和各项工作,制定2030年前碳排放达峰行动方案。二氧化碳加氢制备甲醇既可以实现二氧化碳的资源化利用,又可以有效缓解温室效应问题。
已知:(I)CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+40.9 kJ/mol
(II)CO(g)+2H2(g)=CH3OH(g) ΔH2=—90.3 kJ/mol
(Ⅲ)CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH3
(1)ΔH3=___________ ;上述3个反应ΔS<0的有___________ (填反应序号)。
(2)提高反应(Ⅲ)平衡转化率的方法有___________ 。
(3)当反应压力2 MPa、原料气CO2和H2体积比1:3时,一定范围内温度对CO2转化率、CH3OH选择性、CH3OH产率的影响如下图所示。CH3OH产率在250℃时达到最大的主要原因是___________ 。

(4)在240℃、4MPa恒压条件下发生反应(Ⅲ),原料气体积组成为V(H2):V(CO2):V(N2)=3:1:1,平衡时CO2的转化率为50%,则CH3OH的压强为___________ ,反应(Ⅲ)的平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压x物质的量分数)。
(5)某温度下,反应(Ⅲ)在初期阶段的速率方程为r=k×p(CO2)×p3(H2)×(1—Kp)。其中:k为反应速率常数,随温度升高而增大,Kp为该反应的平衡常数。对于处于初期阶段的该反应,若增加CO2压强,则r___________ (填“增大”“不变”或“减小”,下同);若升高温度,则r___________ 。
已知:(I)CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+40.9 kJ/mol
(II)CO(g)+2H2(g)=CH3OH(g) ΔH2=—90.3 kJ/mol
(Ⅲ)CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH3
(1)ΔH3=
(2)提高反应(Ⅲ)平衡转化率的方法有
(3)当反应压力2 MPa、原料气CO2和H2体积比1:3时,一定范围内温度对CO2转化率、CH3OH选择性、CH3OH产率的影响如下图所示。CH3OH产率在250℃时达到最大的主要原因是

(4)在240℃、4MPa恒压条件下发生反应(Ⅲ),原料气体积组成为V(H2):V(CO2):V(N2)=3:1:1,平衡时CO2的转化率为50%,则CH3OH的压强为
(5)某温度下,反应(Ⅲ)在初期阶段的速率方程为r=k×p(CO2)×p3(H2)×(1—Kp)。其中:k为反应速率常数,随温度升高而增大,Kp为该反应的平衡常数。对于处于初期阶段的该反应,若增加CO2压强,则r
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】 在化工生产中有重要作用.天然气法合成
在化工生产中有重要作用.天然气法合成 相关反应如下:
相关反应如下:
反应I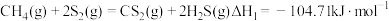
反应Ⅱ
(1) 、
、 随温度变化不大。温度不同时,反应体系中
随温度变化不大。温度不同时,反应体系中 不同。合成
不同。合成 总反应
总反应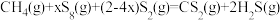 的
的 随温度T变化如图。
随温度T变化如图。
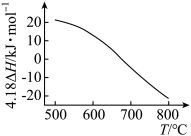
①

________  。
。
②为提高 平衡转化率,控制温度范围在
平衡转化率,控制温度范围在________ (填标号),理由是________ 。
A.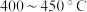 B.
B.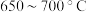 C.
C.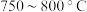 D.
D. 以上
以上
(2)合成 总反应中硫蒸气达到饱和时,反应时间t与
总反应中硫蒸气达到饱和时,反应时间t与 初始浓度
初始浓度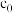 和
和 转化率
转化率 满足关系
满足关系 ,式中k为速率常数。
,式中k为速率常数。
① 、
、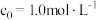 时,测得
时,测得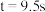 、
、 ,则
,则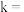
________ 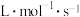 。
。
② 时,计划在
时,计划在 内转化率达
内转化率达 ,应控制初始浓度
,应控制初始浓度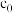 大于
大于________  。
。
(3)利用工业废气 替代硫磺矿生产
替代硫磺矿生产 的反应为
的反应为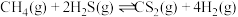 。反应物投料比采用
。反应物投料比采用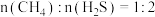 ,维持体系压强为
,维持体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图。
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图。
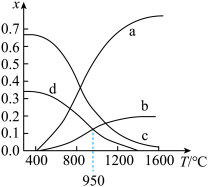
①图中表示 的曲线是
的曲线是________ (填“a”“b”“c”或“d”)。
② 时,该反应的
时,该反应的
________ (以分压表示,分压 总压
总压 物质的量分数)。
物质的量分数)。
③相比以硫磺矿为原料,使用 的优点是
的优点是________ ,缺点是________ 。
 在化工生产中有重要作用.天然气法合成
在化工生产中有重要作用.天然气法合成 相关反应如下:
相关反应如下:反应I
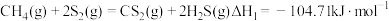
反应Ⅱ

(1)
 、
、 随温度变化不大。温度不同时,反应体系中
随温度变化不大。温度不同时,反应体系中 不同。合成
不同。合成 总反应
总反应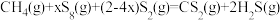 的
的 随温度T变化如图。
随温度T变化如图。
①


 。
。②为提高
 平衡转化率,控制温度范围在
平衡转化率,控制温度范围在A.
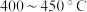 B.
B.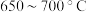 C.
C.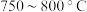 D.
D. 以上
以上(2)合成
 总反应中硫蒸气达到饱和时,反应时间t与
总反应中硫蒸气达到饱和时,反应时间t与 初始浓度
初始浓度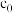 和
和 转化率
转化率 满足关系
满足关系 ,式中k为速率常数。
,式中k为速率常数。①
 、
、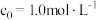 时,测得
时,测得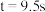 、
、 ,则
,则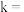
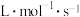 。
。②
 时,计划在
时,计划在 内转化率达
内转化率达 ,应控制初始浓度
,应控制初始浓度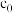 大于
大于 。
。(3)利用工业废气
 替代硫磺矿生产
替代硫磺矿生产 的反应为
的反应为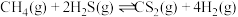 。反应物投料比采用
。反应物投料比采用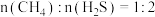 ,维持体系压强为
,维持体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图。
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图。
①图中表示
 的曲线是
的曲线是②
 时,该反应的
时,该反应的
 总压
总压 物质的量分数)。
物质的量分数)。③相比以硫磺矿为原料,使用
 的优点是
的优点是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】 和
和 在特殊条件下会出现某些特殊的性质。
在特殊条件下会出现某些特殊的性质。
(1)采用碱液吸收 并进行电化学氧化可得到硫单质。当
并进行电化学氧化可得到硫单质。当 浓度较低时常用纯碱溶液进行吸收。下表为
浓度较低时常用纯碱溶液进行吸收。下表为 、
、 的电离平衡常数。
的电离平衡常数。
纯碱溶液吸收少量 的离子方程式为
的离子方程式为___________ 。
(2)温度、压强分别超过临界温度(374.2℃)、临界压强(221MPa)的水称为超临界水。超临界水能够与氧气等氧化剂以任意比例互溶,由此形成了超临界水氧化技术。一定实验条件下,运用超临界水氧化技术氧化乙醇的结果如图-1、图-2所示,其中x为以碳元素计的物质的量分数,t为反应时间。
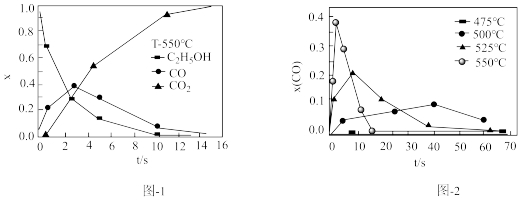
①由图-1,乙醇氧化过程中存在中间产物,该中间产物的化学式为_______ 。
②由图-2,随温度升高,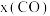 峰值出现的时间提前,且峰值更高,其可能的原因是
峰值出现的时间提前,且峰值更高,其可能的原因是_______ 。
(3)过氧化氢的电离方程式为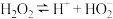 。研究表明,过氧化氢溶液中
。研究表明,过氧化氢溶液中 的浓度越大,过氧化氢的分解速率越快。常温下,不同浓度的过氧化氢分解率与
的浓度越大,过氧化氢的分解速率越快。常温下,不同浓度的过氧化氢分解率与 的关系如图-3所示。
的关系如图-3所示。
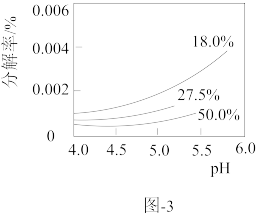
一定浓度的过氧化氢,随 增大分解率增大的原因是
增大分解率增大的原因是___________ 。
(4)研究表明, 对不同原子的结合能力具有差异性,
对不同原子的结合能力具有差异性, 在
在 表面电还原生成
表面电还原生成 的机理如下图:
的机理如下图:

用简洁的语言描述图-4中涉及的转化过程___________ 。
 和
和 在特殊条件下会出现某些特殊的性质。
在特殊条件下会出现某些特殊的性质。(1)采用碱液吸收
 并进行电化学氧化可得到硫单质。当
并进行电化学氧化可得到硫单质。当 浓度较低时常用纯碱溶液进行吸收。下表为
浓度较低时常用纯碱溶液进行吸收。下表为 、
、 的电离平衡常数。
的电离平衡常数。| 电离平衡常数 |  |  |
 |  | 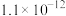 |
 | 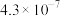 | 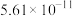 |
纯碱溶液吸收少量
 的离子方程式为
的离子方程式为(2)温度、压强分别超过临界温度(374.2℃)、临界压强(221MPa)的水称为超临界水。超临界水能够与氧气等氧化剂以任意比例互溶,由此形成了超临界水氧化技术。一定实验条件下,运用超临界水氧化技术氧化乙醇的结果如图-1、图-2所示,其中x为以碳元素计的物质的量分数,t为反应时间。

①由图-1,乙醇氧化过程中存在中间产物,该中间产物的化学式为
②由图-2,随温度升高,
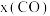 峰值出现的时间提前,且峰值更高,其可能的原因是
峰值出现的时间提前,且峰值更高,其可能的原因是(3)过氧化氢的电离方程式为
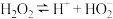 。研究表明,过氧化氢溶液中
。研究表明,过氧化氢溶液中 的浓度越大,过氧化氢的分解速率越快。常温下,不同浓度的过氧化氢分解率与
的浓度越大,过氧化氢的分解速率越快。常温下,不同浓度的过氧化氢分解率与 的关系如图-3所示。
的关系如图-3所示。
一定浓度的过氧化氢,随
 增大分解率增大的原因是
增大分解率增大的原因是(4)研究表明,
 对不同原子的结合能力具有差异性,
对不同原子的结合能力具有差异性, 在
在 表面电还原生成
表面电还原生成 的机理如下图:
的机理如下图:
用简洁的语言描述图-4中涉及的转化过程
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如表:
(1)①由上表数据可知该反应的△H_____ 0(填填“>”、“”或“<”)。
②下列措施能用勒夏特列原理解释是______ (填序号)。
a.增大压强有利于合成氨 b.使用合适的催化剂有利于快速生成氨
c.生产中需要升高温度至500℃左右 d.需要使用过量的N2,提高H2转化率
(2)0.2mol NH3溶于水后再与含有0.2mol H2SO4的稀溶液完全反应放热Q kJ,请你用热化学方程式表示其反应式_________________ 。
(3)原料气H2可通过反应CH4 (g) +H2O (g) CO (g) +3H2(g) 获取,已知该反应中,当初始混合气中的
CO (g) +3H2(g) 获取,已知该反应中,当初始混合气中的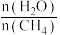 恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
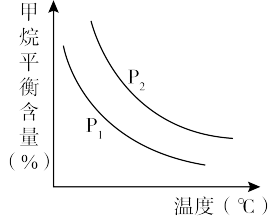
①图中,两条曲线表示压强的关系是: P1__ P2(填“>”、“=”或“<”)。
②其它条件一定,升高温度,氢气的产率会______ (填“增大”,“减小”或“不变”)。
(4)原料气H2还可通过反应CO (g) +H2O (g) CO2 (g) +H2(g) 获取。T℃时,向容积固定为5L的容器中充入1mol H2O (g) 和1mol CO,反应达平衡后,测得CO的浓度0.08 mol/L,该温度下反应的平衡常数K值为
CO2 (g) +H2(g) 获取。T℃时,向容积固定为5L的容器中充入1mol H2O (g) 和1mol CO,反应达平衡后,测得CO的浓度0.08 mol/L,该温度下反应的平衡常数K值为_________ 。
| 温度(℃) | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
(1)①由上表数据可知该反应的△H
②下列措施能用勒夏特列原理解释是
a.增大压强有利于合成氨 b.使用合适的催化剂有利于快速生成氨
c.生产中需要升高温度至500℃左右 d.需要使用过量的N2,提高H2转化率
(2)0.2mol NH3溶于水后再与含有0.2mol H2SO4的稀溶液完全反应放热Q kJ,请你用热化学方程式表示其反应式
(3)原料气H2可通过反应CH4 (g) +H2O (g)
 CO (g) +3H2(g) 获取,已知该反应中,当初始混合气中的
CO (g) +3H2(g) 获取,已知该反应中,当初始混合气中的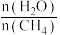 恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
①图中,两条曲线表示压强的关系是: P1
②其它条件一定,升高温度,氢气的产率会
(4)原料气H2还可通过反应CO (g) +H2O (g)
 CO2 (g) +H2(g) 获取。T℃时,向容积固定为5L的容器中充入1mol H2O (g) 和1mol CO,反应达平衡后,测得CO的浓度0.08 mol/L,该温度下反应的平衡常数K值为
CO2 (g) +H2(g) 获取。T℃时,向容积固定为5L的容器中充入1mol H2O (g) 和1mol CO,反应达平衡后,测得CO的浓度0.08 mol/L,该温度下反应的平衡常数K值为
您最近一年使用:0次



