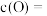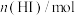化学反应速率
(1)表示方法
通常用单位时间内反应物浓度的 1 或生成物浓度的 2 来表示。
(2)数学表达式及单位
v= ,单位为mol·L-1·min-1或mol·L-1·s-1。
,单位为mol·L-1·min-1或mol·L-1·s-1。
(3)化学反应速率与化学计量数的关系
同一反应在同一时间内,用不同物质来表示的反应速率可能 3 ,但反应速率的数值之比等于这些物质在化学方程式中的 4 之比。如在反应aA(g)+bB(g)⇌cC(g)+dD(g)中,存在v(A)∶v(B)∶v(C)∶v(D)=a∶b∶c∶d。
(4)同一化学反应中反应快慢的比较方法
由于同一化学反应的反应速率用不同物质表示时数值可能 5 ,所以比较反应的快慢不能只看数值的大小,而要进行一定的转化。
①看单位是否统一,若不统一,换算成相同的单位。
②换算成同一物质表示的速率,再比较数值的大小。
③比较化学反应速率与化学计量数的比值,即对于一般反应aA+bB=cC+dD,比较 与
与 ,若
,若 >
> ,则A表示的反应速率比B的大。
,则A表示的反应速率比B的大。
(1)表示方法
通常用单位时间内反应物浓度的
(2)数学表达式及单位
v=
 ,单位为mol·L-1·min-1或mol·L-1·s-1。
,单位为mol·L-1·min-1或mol·L-1·s-1。(3)化学反应速率与化学计量数的关系
同一反应在同一时间内,用不同物质来表示的反应速率可能
(4)同一化学反应中反应快慢的比较方法
由于同一化学反应的反应速率用不同物质表示时数值可能
①看单位是否统一,若不统一,换算成相同的单位。
②换算成同一物质表示的速率,再比较数值的大小。
③比较化学反应速率与化学计量数的比值,即对于一般反应aA+bB=cC+dD,比较
 与
与 ,若
,若 >
> ,则A表示的反应速率比B的大。
,则A表示的反应速率比B的大。
2023高三·全国·专题练习 查看更多[1]
(已下线)化学反应速率及其影响因素
更新时间:2023-12-16 11:38:43
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】煅烧硫铁矿(主要成分为FeS2)的反应为:4FeS2+11O2 2Fe2O3+8SO2。试回答下列问题。
2Fe2O3+8SO2。试回答下列问题。
(1)可用哪些物质来表示该反应的化学反应速率_______ 。
(2)某时刻时测得,生成SO2的速率为0.64mol/(L•s),则氧气减少的速率为_______ mol/(L•s)。
(3)该工业生产中将矿石粉碎的目的:_______ 。
 2Fe2O3+8SO2。试回答下列问题。
2Fe2O3+8SO2。试回答下列问题。(1)可用哪些物质来表示该反应的化学反应速率
(2)某时刻时测得,生成SO2的速率为0.64mol/(L•s),则氧气减少的速率为
(3)该工业生产中将矿石粉碎的目的:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】为倡导“节能减排”和“低碳经济”,降低大气中CO2的含量及有效地开发利用CO2,工业上可以用CO2来生产燃料甲醇。在体积为2L的密闭容器中,充入1mol CO2、3mol H2,一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
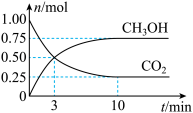
(1)在3min末,H2的浓度为_______ ,这时,反应速率 υ(正)_______ υ(逆)(选填>、<或 =)。
(2)从反应开始到平衡,平均反应速率υ(CO2)=_______ 。达到平衡时,H2的转化率为_______ 。
(3)下列措施不能提高反应速率的是_______。
(4)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:υ(H2)=0.3 mol∙L−1∙s−1;乙:υ(CO2)=0.12 mol∙L−1∙s−1;丙:υ(CH3OH)=4.8 mol∙L−1∙min−1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为_______ 。
(5)在一体积固定的密闭容器中投入一定量的CO2和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是_______ 。
A.反应中CO2与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1mol CO2,同时生成1mol CH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
 CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
(1)在3min末,H2的浓度为
(2)从反应开始到平衡,平均反应速率υ(CO2)=
(3)下列措施不能提高反应速率的是_______。
| A.升高温度 | B.加入催化剂 | C.增大压强 | D.及时分离出CH3OH |
(5)在一体积固定的密闭容器中投入一定量的CO2和H2进行上述反应。下列叙述中能说明上述反应达到平衡状态的是
A.反应中CO2与CH3OH的物质的量之比为1:1
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗1mol CO2,同时生成1mol CH3OH
D.CH3OH的质量分数在混合气体中保持不变
E.混合气体的密度保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】恒温下,向容积为2.0 L的恒容密闭容器中通入0.40 mol HI,发生反应 ,0~6 min内,
,0~6 min内, 随时间变化关系如下表:
随时间变化关系如下表:
(1)0~2 min内的平均反应速率
______  ,3~5 min内的平均反应速率
,3~5 min内的平均反应速率
______  。
。
(2)对比0~2 min和3~5 min内的平均反应速率,二者不相等,出现这种现象的原因是______ 。
 ,0~6 min内,
,0~6 min内, 随时间变化关系如下表:
随时间变化关系如下表:时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 0.40 | 0.30 | 0.24 | 0.20 | 0.18 | 0.16 | 0.16 |

 ,3~5 min内的平均反应速率
,3~5 min内的平均反应速率
 。
。(2)对比0~2 min和3~5 min内的平均反应速率,二者不相等,出现这种现象的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】T℃、2L密闭容器中某一反应不同时刻各物质的量如图(E为固体,其余为气体).回答下列问题:
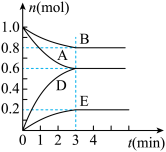
(1)写出该反应的化学方程式______________________________________ .
(2)反应开始至3min时,用D表示的平均反应速率为______ mol/(L•min).
(3)若升高温度,则v(正)________ ,v(逆)________ (填“加快”或“减慢”)。
(4)若反应在甲、乙两个相同容器内同时进行,分别测得甲中v(A)=0.3 mol·L-1·min-1,乙中v(B)=0.2 mol·L-1·min-1,则________ 容器中反应更快。

(1)写出该反应的化学方程式
(2)反应开始至3min时,用D表示的平均反应速率为
(3)若升高温度,则v(正)
(4)若反应在甲、乙两个相同容器内同时进行,分别测得甲中v(A)=0.3 mol·L-1·min-1,乙中v(B)=0.2 mol·L-1·min-1,则
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】恒温恒容时,NO2和N2O4之间发生反应:N2O4(g)⇌2NO2(g),如图所示。
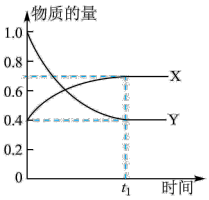
(1)曲线____ (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)若升高温度,则v(NO2)____ (填“增大”或“减小”)。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3 mol·L-1·min-1,乙中v(N2O4)=0.2 mol·L-1·min-1,则________ 中反应更快。

(1)曲线
(2)若升高温度,则v(NO2)
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3 mol·L-1·min-1,乙中v(N2O4)=0.2 mol·L-1·min-1,则
您最近一年使用:0次

 催化时,
催化时, 的分解可分为以下两步反应进行:
的分解可分为以下两步反应进行: (慢)
(慢)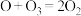 (快)
(快)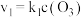 ,第二步的速率方程为
,第二步的速率方程为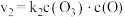 。其中O为活性氧原子,它在第一步慢反应中生成,然后又很快的在第二步反应中消耗,因此,我们可以认为活性氧原子变化的速率为零。请用
。其中O为活性氧原子,它在第一步慢反应中生成,然后又很快的在第二步反应中消耗,因此,我们可以认为活性氧原子变化的速率为零。请用 、
、 组成的代数式表示
组成的代数式表示