乙烯产量是衡量一个国家石油化工发展水平的重要标志,羟基氮化硼可高效催化乙烷氧化脱氢制乙烯。
主反应: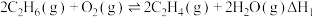
副反应: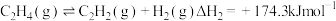
(1) 的燃烧热
的燃烧热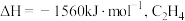 的燃烧热
的燃烧热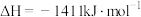 ,
,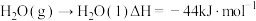 ,则
,则
___________ 。
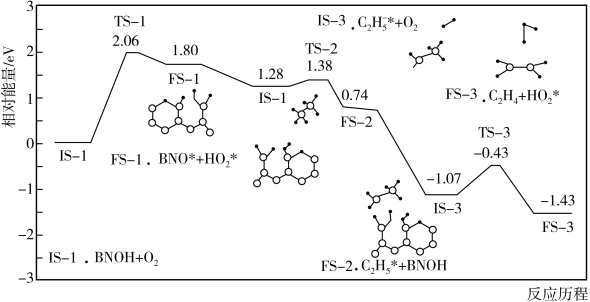
(2)主反应的部分反应历程如下图所示(图中IS表示起始态,TS表示过渡态,FS表示终态)。这一部分反应中慢反应的活化能
___________  。
。
(3)提高乙烯平衡产率的方法是___________ (任写两条),提高乙烯单位时间产量的关键因素是___________ 。
(4)工业上催化氧化制乙烯时,通常在乙烷和氧气的混合气体中掺入惰性气体,即将一定比例的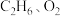 和
和 混合气体以一定的流速通过两种不同的催化剂进行反应,相同时间内测得乙烯的产率如下图所示。
混合气体以一定的流速通过两种不同的催化剂进行反应,相同时间内测得乙烯的产率如下图所示。
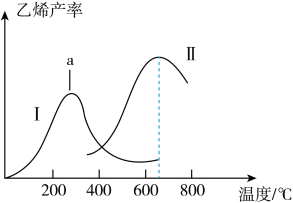
①曲线1中,a点右侧乙烯产量随温度升高而降低的原因是___________ 。
②两种催化剂比较,催化剂Ⅱ的优点与不足是___________ 。
(5)一定温度下,维持压强始终为p,向反应装置中通入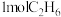 、
、 和
和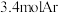 的混合气体,经过
的混合气体,经过 后,反应达到平衡,此时乙烷的转化率为
后,反应达到平衡,此时乙烷的转化率为 ,乙烯选择性为
,乙烯选择性为 ,(乙烯选择性
,(乙烯选择性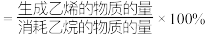 )。
)。
①反应速率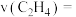
___________ 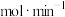 。
。
②已知:气体分压 气体总压
气体总压 气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ,则主反应在该温度下的
,则主反应在该温度下的
___________ (列出计算式即可,不必化简)。
主反应:
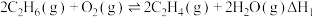
副反应:
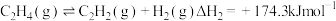
(1)
 的燃烧热
的燃烧热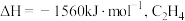 的燃烧热
的燃烧热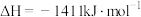 ,
,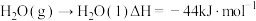 ,则
,则
(2)主反应的部分反应历程如下图所示(图中IS表示起始态,TS表示过渡态,FS表示终态)。这一部分反应中慢反应的活化能

 。
。
(3)提高乙烯平衡产率的方法是
(4)工业上催化氧化制乙烯时,通常在乙烷和氧气的混合气体中掺入惰性气体,即将一定比例的
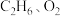 和
和 混合气体以一定的流速通过两种不同的催化剂进行反应,相同时间内测得乙烯的产率如下图所示。
混合气体以一定的流速通过两种不同的催化剂进行反应,相同时间内测得乙烯的产率如下图所示。
①曲线1中,a点右侧乙烯产量随温度升高而降低的原因是
②两种催化剂比较,催化剂Ⅱ的优点与不足是
(5)一定温度下,维持压强始终为p,向反应装置中通入
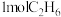 、
、 和
和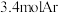 的混合气体,经过
的混合气体,经过 后,反应达到平衡,此时乙烷的转化率为
后,反应达到平衡,此时乙烷的转化率为 ,乙烯选择性为
,乙烯选择性为 ,(乙烯选择性
,(乙烯选择性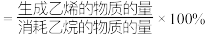 )。
)。①反应速率
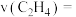
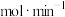 。
。②已知:气体分压
 气体总压
气体总压 气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数
气体的物质的量分数,用平衡分压代替平衡浓度可以得到平衡常数 ,则主反应在该温度下的
,则主反应在该温度下的
更新时间:2023-12-17 10:14:05
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】氢气作为清洁能源有着广泛的应用前景,含硫天然气制备氢气的流程如下。

请回答下列问题:
Ⅰ.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如图所示。
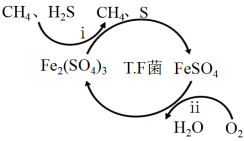
(1)过程i中H2S发生了___ (填“氧化”或“还原”)反应。
(2)过程ii的离子方程式是___ 。
(3)已知:①Fe3+在pH=1.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
请结合以上信息,判断工业脱硫应选择的最佳pH范围,并说明原因:___ 。
II.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。
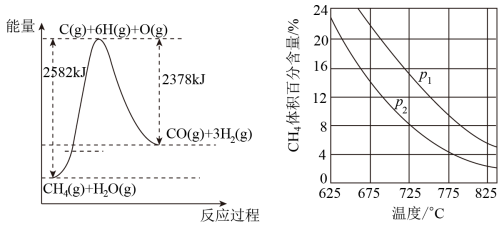
(4)①该过程的热化学方程式是___ 。
②比较压强p1和p2的大小关系:p1___ p2(选填“>”“<”或“=”)。
III.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
IV.H2提纯:将CO2和H2分离得到H2的过程示意图如图。
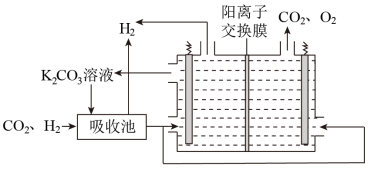
(5)①吸收池中发生反应的离子方程式是___ 。
②结合电极反应式,简述K2CO3溶液的再生原理:___ 。

请回答下列问题:
Ⅰ.转化脱硫:将天然气压入吸收塔,30℃时,在T.F菌作用下,酸性环境中脱硫过程示意图如图所示。

(1)过程i中H2S发生了
(2)过程ii的离子方程式是
(3)已知:①Fe3+在pH=1.9时开始沉淀,pH=3.2时沉淀完全。
②30℃时,在T.F菌作用下,不同pH的FeSO4溶液中Fe2+的氧化速率如下表。
| pH | 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.4 | 2.7 | 3.0 |
| Fe2+氧化速率/(g·L-1·h-1) | 4.5 | 5.3 | 6.2 | 6.8 | 7.0 | 6.6 | 6.2 | 5.6 |
II.蒸气转化:在催化剂的作用下,水蒸气将CH4氧化。结合如图回答问题。

(4)①该过程的热化学方程式是
②比较压强p1和p2的大小关系:p1
III.CO变换:500℃时,CO进一步与水反应生成CO2和H2。
IV.H2提纯:将CO2和H2分离得到H2的过程示意图如图。

(5)①吸收池中发生反应的离子方程式是
②结合电极反应式,简述K2CO3溶液的再生原理:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9kJ·mol-1 NO(g)+1/2O2(g)=NO2(g) △H=-58.2kJ·mol-1 SO2(g)+O3(g)=SO3(g)+O2(g) △H=-241.6kJ·mol-1
(1)反应3NO(g)+O3(g)=3NO2(g)的△H=_______ mol·L-1。

(2)室温下,固定进入反应器的NO、SO2的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)、n(NO2)和n(SO2)随反应前n(O3):n(NO)的变化见右图。
①当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是_________________
②增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是___________________ 。
(3)当用CaSO3水悬浮液吸收经O3预处理的烟气时,溶液(pH约为 8)中SO32-将NO2转化为NO2-,其离子方程式为:_________________________________________________________________________________
(4)CaSO3水悬浮液中加入Na2SO4溶液,达到平衡后溶液中c(SO32-)=_____________________________ [用c(SO42-)、Ksp(CaSO3)和Ksp(CaSO4)表示];CaSO3水悬浮液中加入Na2SO4溶液能提高NO2的吸收速率,其主要原因是__________________________________________________________________
(5)甲醇燃料电池在碱性溶液中的电极反应式。正极_________________________________ ;负极____________________________________________________________________________
(1)反应3NO(g)+O3(g)=3NO2(g)的△H=

(2)室温下,固定进入反应器的NO、SO2的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)、n(NO2)和n(SO2)随反应前n(O3):n(NO)的变化见右图。
①当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是
②增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是
(3)当用CaSO3水悬浮液吸收经O3预处理的烟气时,溶液(pH约为 8)中SO32-将NO2转化为NO2-,其离子方程式为:
(4)CaSO3水悬浮液中加入Na2SO4溶液,达到平衡后溶液中c(SO32-)=
(5)甲醇燃料电池在碱性溶液中的电极反应式。正极
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】亚硝酰氯(NOCl)是有机合成中的重要试剂,工业上可由NO与Cl2反应制得,回答下列问题:
Ⅰ.(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
2NO2(g)+NaCl(s) ⇌ NaNO3(s)+NOCl(g) ΔH1;K1
4NO2(g)+2NaCl(s) ⇌ 2NaNO3(s)+2NO(g)+Cl2(g) ΔH2;K2
2NO(g)+Cl2(g) ⇌ 2NOCl(g) ΔH3;K3
则ΔH3=___________ (用ΔH1和ΔH2表示),K3=___________ (用K1和K2表示)
Ⅱ.工业上通常用如下反应制备亚硝酰氯:2NO(g)+Cl2(g) ⇌2NOCl(g) ΔH<0.
(1)已知上述反应中逆反应速率的表达式为v逆=k·cn(NOCl)。300℃时,测得逆反应速率与NOCl的浓度的关系如表所示:
当c(NOCl)=0.50 mol·L-1时,v逆=___________ mol·L-1·s-1
(2)保持恒温恒容条件,将物质的量之和为3 mol的NO和Cl2以不同的氮氯比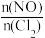 进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:

①图中T1、T2的关系为T1___________ T2(填“>”“<”或“=”);图中纵坐标为物质___________ 的转化率。图中A、B、C三点对应的NOCl体积分数最大的是___________ (填“A”“B”或“C”)。
②若容器容积为1 L,经过10min到达A点,该时间段内化学反应速率υ(NO)=___________ 。B点的平衡常数为___________ 。
③若在温度为T1,容积为1 L的容器中,充入0.5molNO、1molCl2、2molNOCl,υ(正)___________ υ(逆)(填“<”“>”或“=”)
Ⅰ.(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
2NO2(g)+NaCl(s) ⇌ NaNO3(s)+NOCl(g) ΔH1;K1
4NO2(g)+2NaCl(s) ⇌ 2NaNO3(s)+2NO(g)+Cl2(g) ΔH2;K2
2NO(g)+Cl2(g) ⇌ 2NOCl(g) ΔH3;K3
则ΔH3=
Ⅱ.工业上通常用如下反应制备亚硝酰氯:2NO(g)+Cl2(g) ⇌2NOCl(g) ΔH<0.
(1)已知上述反应中逆反应速率的表达式为v逆=k·cn(NOCl)。300℃时,测得逆反应速率与NOCl的浓度的关系如表所示:
| c(NOCl)/(mol/L) | v逆 /(mol∙L-1∙s-1) |
| 0.20 | 1.6×10-9 |
| 0.40 | 6.4×10-9 |
(2)保持恒温恒容条件,将物质的量之和为3 mol的NO和Cl2以不同的氮氯比
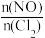 进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
①图中T1、T2的关系为T1
②若容器容积为1 L,经过10min到达A点,该时间段内化学反应速率υ(NO)=
③若在温度为T1,容积为1 L的容器中,充入0.5molNO、1molCl2、2molNOCl,υ(正)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】氮及其化合物在科研及生产中均有重要的应用。回答下列问题:
(1)NH3与O2在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
反应i:4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ΔH1= -905kJ·mol-1
反应ii:4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g) ΔH2= -1268kJ·mol-1
该条件下N2被O2生成NO的热化学方程式为_______ 。
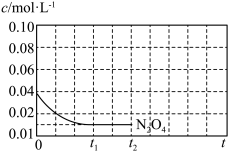
(2)已知:N2O4(g)⇌2NO2(g) ΔH>0,将0.04mol N2O4气体充入1L的恒容密闭容器中,控制反应温度为T1,c(N2O4)随t(时间)变化曲线如图。
①下列可以作为反应达到平衡的判据是_______ 。
A.容器内压强不变 B.v正(N2O4)=2v逆(NO2) C.K不变
D.混合气体的密度不变 E.混合气体的颜色不变
②t1时刻反应达到平衡,若t1=15min,计算0~15 min内的平均反应速率v(NO2)=_______ ,此时反应的平衡常数K=_______ 。
③反应温度T1时,画出0~t2时段,c(NO2)随t变化曲线。保持其他条件不变,改变反应温度为T2(T2>T1),再次画出0~t2时段,c(NO2)随t变化趋势的曲线_______ 。
(3)升高温度,绝大多数的化学反应速率增大,但是NO氧化反应2NO(g)+O2(g)⇌2NO2(g) ΔH< 0,该反应的速率却随温度的升高而减小。查阅资料得知NO氧化反应的反应历程分两步,每步反应的速率方程中k正和k逆随温度的升高都增大。
I. 2NO(g)⇌N2O2(g)(快) ΔH1<0;速率方程为v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2)
II. N2O2(g)+O2(g)⇌2NO2(g)(慢) ΔH2<0;速率方程为v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2)
①根据速率方程分析,决定NO氧化反应速率的步骤是_______ (填“I”或“II”),升高温度该反应速率减小的原因是_______ 。
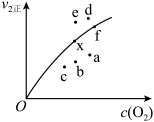
②一定温度下,反应达到平衡状态,由实验数据得到v2正~c(O2)的关系可用如图表示。当x点升高到某一温度时,反应重新达到平衡,则变为相应的点为_______ (填字母)。
(1)NH3与O2在一定压强和800℃条件下发生催化氧化反应时,可发生不同反应:
反应i:4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g) ΔH1= -905kJ·mol-1
反应ii:4NH3(g)+3O2(g)⇌2N2(g)+6H2O(g) ΔH2= -1268kJ·mol-1
该条件下N2被O2生成NO的热化学方程式为
(2)已知:N2O4(g)⇌2NO2(g) ΔH>0,将0.04mol N2O4气体充入1L的恒容密闭容器中,控制反应温度为T1,c(N2O4)随t(时间)变化曲线如图。

①下列可以作为反应达到平衡的判据是
A.容器内压强不变 B.v正(N2O4)=2v逆(NO2) C.K不变
D.混合气体的密度不变 E.混合气体的颜色不变
②t1时刻反应达到平衡,若t1=15min,计算0~15 min内的平均反应速率v(NO2)=
③反应温度T1时,画出0~t2时段,c(NO2)随t变化曲线。保持其他条件不变,改变反应温度为T2(T2>T1),再次画出0~t2时段,c(NO2)随t变化趋势的曲线
(3)升高温度,绝大多数的化学反应速率增大,但是NO氧化反应2NO(g)+O2(g)⇌2NO2(g) ΔH< 0,该反应的速率却随温度的升高而减小。查阅资料得知NO氧化反应的反应历程分两步,每步反应的速率方程中k正和k逆随温度的升高都增大。
I. 2NO(g)⇌N2O2(g)(快) ΔH1<0;速率方程为v1正=k1正·c2(NO),v1逆=k1逆·c(N2O2)
II. N2O2(g)+O2(g)⇌2NO2(g)(慢) ΔH2<0;速率方程为v2正=k2正·c(N2O2)·c(O2),v2逆=k2逆·c2(NO2)
①根据速率方程分析,决定NO氧化反应速率的步骤是
②一定温度下,反应达到平衡状态,由实验数据得到v2正~c(O2)的关系可用如图表示。当x点升高到某一温度时,反应重新达到平衡,则变为相应的点为

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】近年来我国在应对气候变化工作中取得显著成效,并向国际社会承诺2030年实现“碳达峰”,2060年实现“碳中和”。因此将 转化为高附加值化学品成为科学家研究的重要课题。
转化为高附加值化学品成为科学家研究的重要课题。
Ⅰ、工业上在Cu—ZnO催化下利用 ,发生如下反应①来生产甲醇,同时伴有反应②发生。
,发生如下反应①来生产甲醇,同时伴有反应②发生。
①
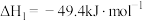
②

(1)已知:
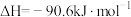 ,则
,则
_______ 。
(2)向密闭容器中加入 和
和 合成
合成 。已知反应①的正反应速率可表示为
。已知反应①的正反应速率可表示为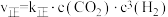 ,逆反应速率可表示为
,逆反应速率可表示为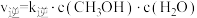 ,其中
,其中 、
、 为速率常数。下图甲中能够代表
为速率常数。下图甲中能够代表 的曲线为
的曲线为_______ (填 、
、 、
、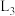 或
或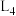 )。
)。

(3)不同条件下,按照 投料,
投料, 的平衡转化率如图乙所示。压强
的平衡转化率如图乙所示。压强 、
、 、
、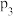 由大到小的顺序是
由大到小的顺序是_______ 。压强为 时,温度高于570℃之后,随着温度升高
时,温度高于570℃之后,随着温度升高 平衡转化率增大的原因是
平衡转化率增大的原因是_______ 。
Ⅱ、2022年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回答下列问题:在一定温度下,向体积固定的密闭容器中加入足量的 和1mol
和1mol ,起始压强为0.2MPa时,发生下列反应生成水煤气:
,起始压强为0.2MPa时,发生下列反应生成水煤气:
①
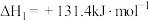
②

(4)下列说法不正确的是_______;
(5)反应平衡时, 的转化率为50%,CO的物质的量为0.1mol。此时,整个体系
的转化率为50%,CO的物质的量为0.1mol。此时,整个体系_______ (填“吸收”或“放出”)热量,反应①的平衡常数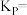
_______ (以分压表示,分压=总压×物质的量分数)。
 转化为高附加值化学品成为科学家研究的重要课题。
转化为高附加值化学品成为科学家研究的重要课题。Ⅰ、工业上在Cu—ZnO催化下利用
 ,发生如下反应①来生产甲醇,同时伴有反应②发生。
,发生如下反应①来生产甲醇,同时伴有反应②发生。①

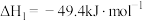
②


(1)已知:

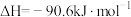 ,则
,则
(2)向密闭容器中加入
 和
和 合成
合成 。已知反应①的正反应速率可表示为
。已知反应①的正反应速率可表示为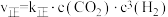 ,逆反应速率可表示为
,逆反应速率可表示为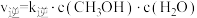 ,其中
,其中 、
、 为速率常数。下图甲中能够代表
为速率常数。下图甲中能够代表 的曲线为
的曲线为 、
、 、
、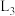 或
或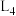 )。
)。
(3)不同条件下,按照
 投料,
投料, 的平衡转化率如图乙所示。压强
的平衡转化率如图乙所示。压强 、
、 、
、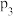 由大到小的顺序是
由大到小的顺序是 时,温度高于570℃之后,随着温度升高
时,温度高于570℃之后,随着温度升高 平衡转化率增大的原因是
平衡转化率增大的原因是Ⅱ、2022年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回答下列问题:在一定温度下,向体积固定的密闭容器中加入足量的
 和1mol
和1mol ,起始压强为0.2MPa时,发生下列反应生成水煤气:
,起始压强为0.2MPa时,发生下列反应生成水煤气:①

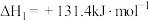
②


(4)下列说法不正确的是_______;
| A.平衡时向容器中充入惰性气体,反应①平衡逆向移动,反应②平衡不移动 |
| B.混合气体的密度保持不变时,说明反应体系已达到平衡 |
C.平衡时 的体积分数可能等于 的体积分数可能等于 |
| D.将炭块粉碎,可加快反应速率 |
 的转化率为50%,CO的物质的量为0.1mol。此时,整个体系
的转化率为50%,CO的物质的量为0.1mol。此时,整个体系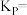
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】化学反应原理在科研和生产中有广泛应用。
(1)用生物质热解气(主要成分为CO、CH4、H2)将SO2在一定条件下还原为单质硫进行烟气脱硫。已知:
①C(s)+O2(g)=CO2(g) △H1=-393.5 kJ·mol-1
②CO2(g)+C(s)=2CO(g) △H2= + 172.5 kJ·mol-1
③S(s)+O2(g)=SO2(g) △H3=- 296.0 kJ·mol-1
CO将SO2还原为单质硫的热化学方程式为________________________ 。
(2)CO可用于合成甲醇,一定温度下,向体积为2 L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g) CH3OH(g),5分钟后达到平衡测得各组分物质的量如下:
CH3OH(g),5分钟后达到平衡测得各组分物质的量如下:
①反应达到平衡时,CO的转化率为_______ ,5分钟内用H2表示的速率为________
②该反应的平衡常数K=__________ 。
③恒温恒容条件下,可以说明反应已达到平衡状态的是__________ (填标号)。
A.v正(CO)=2v逆(H2) B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.CO、H2的浓度之比为1:2
E.单位时间内,每生成1mol H2消耗2mol CH3OH
④若将容器体积压缩到1L,则达到新平衡时c(H2)的取值范围是_____________ 。
⑤若保持容器体积不变,再充入0.6 mol CO 和0.4 mol CH3OH,此时v正__________ v逆(填“ >” < ”或“= ”)。
(1)用生物质热解气(主要成分为CO、CH4、H2)将SO2在一定条件下还原为单质硫进行烟气脱硫。已知:
①C(s)+O2(g)=CO2(g) △H1=-393.5 kJ·mol-1
②CO2(g)+C(s)=2CO(g) △H2= + 172.5 kJ·mol-1
③S(s)+O2(g)=SO2(g) △H3=- 296.0 kJ·mol-1
CO将SO2还原为单质硫的热化学方程式为
(2)CO可用于合成甲醇,一定温度下,向体积为2 L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g)
 CH3OH(g),5分钟后达到平衡测得各组分物质的量如下:
CH3OH(g),5分钟后达到平衡测得各组分物质的量如下:| 物质 | CO | H2 | CH3OH |
| 物质的量(mol) | 1.8 | 2.0 | 1.2 |
①反应达到平衡时,CO的转化率为
②该反应的平衡常数K=
③恒温恒容条件下,可以说明反应已达到平衡状态的是
A.v正(CO)=2v逆(H2) B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.CO、H2的浓度之比为1:2
E.单位时间内,每生成1mol H2消耗2mol CH3OH
④若将容器体积压缩到1L,则达到新平衡时c(H2)的取值范围是
⑤若保持容器体积不变,再充入0.6 mol CO 和0.4 mol CH3OH,此时v正
您最近一年使用:0次



