丙烯酰氯可用于合成一种神经肌肉阻断剂药物,某小组设计以下实验制备丙烯酰氯。
实验(一)制备三氯化磷 的沸点为76℃,
的沸点为76℃, 遇水蒸气剧烈反应;
遇水蒸气剧烈反应;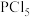 的熔点为148℃。
的熔点为148℃。
② 与
与 反应生成
反应生成 。
。
(1)B装置盛装的试剂为_______ ;E装置的作用除吸收尾气外,还有________ 的作用。
(2)A装置中发生反应的离子方程式为___________ ;
(3)为了提高产品纯度,宜采取的操作是___________ ;
(4)分离产品的方法是___________ 。
实验(二)制备丙烯酰氯( )
)
反应原理:
在干燥的三颈烧瓶中加入67.8 (1.0
(1.0 )丙烯酸,29
)丙烯酸,29 (0.333
(0.333 )三氯化磷,装置如图所示。缓慢加热回流,冷却至60~70℃,搅拌15min,室温放置2h,分离出上层液体,并对其进行减压蒸馏,得到无色液体59.8g。
)三氯化磷,装置如图所示。缓慢加热回流,冷却至60~70℃,搅拌15min,室温放置2h,分离出上层液体,并对其进行减压蒸馏,得到无色液体59.8g。___________ ,仪器A的进水口为___________ (填“a”或“b”)。
(6)本实验产率约为___________ (保留小数点后一位)。
实验(一)制备三氯化磷
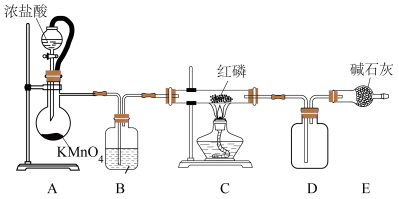
 的沸点为76℃,
的沸点为76℃, 遇水蒸气剧烈反应;
遇水蒸气剧烈反应;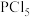 的熔点为148℃。
的熔点为148℃。②
 与
与 反应生成
反应生成 。
。(1)B装置盛装的试剂为
(2)A装置中发生反应的离子方程式为
(3)为了提高产品纯度,宜采取的操作是
(4)分离产品的方法是
实验(二)制备丙烯酰氯(
 )
)反应原理:

在干燥的三颈烧瓶中加入67.8
 (1.0
(1.0 )丙烯酸,29
)丙烯酸,29 (0.333
(0.333 )三氯化磷,装置如图所示。缓慢加热回流,冷却至60~70℃,搅拌15min,室温放置2h,分离出上层液体,并对其进行减压蒸馏,得到无色液体59.8g。
)三氯化磷,装置如图所示。缓慢加热回流,冷却至60~70℃,搅拌15min,室温放置2h,分离出上层液体,并对其进行减压蒸馏,得到无色液体59.8g。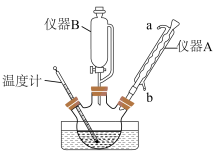
(6)本实验产率约为
更新时间:2023-12-16 19:48:20
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】某工厂采用如下步骤从海水中提取镁:
①把贝壳制成石灰乳;
②在引入的海水中加入石灰乳,沉降,过滤,洗涤;
③将沉淀物与盐酸反应,蒸发结晶,过滤,得到含结晶水的晶体;
④将所得晶体在一定条件下加热得到无水氯化镁;
⑤电解熔融氯化镁,得到金属镁。
回答下列问题:
(1)Ca(OH)2所含元素中,质量分数最高的元素为_____ (填元素符号),该元素在地壳中的含量居于第_____ 位。
(2)写出沉淀物中的Mg(OH)2与盐酸反应的离子方程式:_____ ,该反应的基本反应类型为_____ 。
(3)氯化镁溶液在空气中直接加热得到的最终产物为MgO,发生反应的化学方程式为①MgCl2+2H2O Mg(OH)2↓+2HCl;②Mg(OH)2
Mg(OH)2↓+2HCl;②Mg(OH)2 MgO+H2O。反应①利用了盐酸的
MgO+H2O。反应①利用了盐酸的____ (填“酸性”、“还原性”、“氧化性”或“挥发性”),在反应②中,每生成0.4gMgO,此时消耗MgCl2的物质的量为____ mol。
(4)已知海水中镁的含量为1.28g•L-1,每生产1.00t镁,至少需要引入____ L海水(不考虑生产过程中质量的损失)。
①把贝壳制成石灰乳;
②在引入的海水中加入石灰乳,沉降,过滤,洗涤;
③将沉淀物与盐酸反应,蒸发结晶,过滤,得到含结晶水的晶体;
④将所得晶体在一定条件下加热得到无水氯化镁;
⑤电解熔融氯化镁,得到金属镁。
回答下列问题:
(1)Ca(OH)2所含元素中,质量分数最高的元素为
(2)写出沉淀物中的Mg(OH)2与盐酸反应的离子方程式:
(3)氯化镁溶液在空气中直接加热得到的最终产物为MgO,发生反应的化学方程式为①MgCl2+2H2O
 Mg(OH)2↓+2HCl;②Mg(OH)2
Mg(OH)2↓+2HCl;②Mg(OH)2 MgO+H2O。反应①利用了盐酸的
MgO+H2O。反应①利用了盐酸的(4)已知海水中镁的含量为1.28g•L-1,每生产1.00t镁,至少需要引入
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】如图为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题
(1)①、②、③、④分别是_______ 、_______ 、_______ 、_______ (用元素符号表示)。
(2)画出⑤的原子结构示意图:_______ 。
(3)画出与⑧同族的下一周期元素的原子结构示意图:_______ 。
(4)⑥的单质与氢氧化钠溶液反应的化学方程式:_______ 。
(5)向500mLNaOH溶液中投入10.8gAl,二者恰好完全反应,产生H2(标况下)的体积为_______ L,参加反应的NaOH溶液的物质的量浓度为_______ mol/L。(忽略反应前后溶液体积的变化)。
(6)写出①的三种核素:_______ 、_______ 、_______ 。
(7)①、③、④元素中的两种元素可形成10个电子的分子,它们是_______ 、_______ 。(写出两个)
| 周期 | IA | 0 | |||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | …… | ② | ③ | ④ | |||||
| 3 | ⑤ | …… | ⑥ | ⑦ | ⑧ | ||||
(2)画出⑤的原子结构示意图:
(3)画出与⑧同族的下一周期元素的原子结构示意图:
(4)⑥的单质与氢氧化钠溶液反应的化学方程式:
(5)向500mLNaOH溶液中投入10.8gAl,二者恰好完全反应,产生H2(标况下)的体积为
(6)写出①的三种核素:
(7)①、③、④元素中的两种元素可形成10个电子的分子,它们是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为________________ mol.L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______________(填字母)。
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol.L-1的稀盐酸。
①该学生需要量取_______________ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面________
b定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水________
(4)①假设该同学成功配制了0.400mol.L-1的盐酸,他又用该盐酸中和含0.4gNaOH的NaOH溶液,则该同学需取_______________ mL盐酸。
②假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是_______________ 。(填字母)
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:1.19g.cm-3 HCl的质量分数:36.5% |
(1)该浓盐酸中HCl的物质的量浓度为
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_______________(填字母)。
| A.溶液中HCl的物质的量 | B.溶液的物质的量浓度 |
| C.溶液中Cl-的数目 | D.溶液的密度 |
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol.L-1的稀盐酸。
①该学生需要量取
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面
b定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
(4)①假设该同学成功配制了0.400mol.L-1的盐酸,他又用该盐酸中和含0.4gNaOH的NaOH溶液,则该同学需取
②假设该同学用新配制的盐酸中和含0.4 g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】硫酸锰(MnSO4·H2O)是一种粉色晶体,易溶于水,不溶于乙醇,是重要的微量元素肥料之一,可促进多种经济作物生长从而增加其产量。甲、乙两组同学拟制取硫酸锰并探究其性质。
(1)甲组同学拟制备MnSO4·H2O。
首先称取5.0gMnO2于200mL烧杯中,加入12.00mL6.00mol/L硫酸和6.00mLH2O。然后再称取8.0g草酸晶体[H2C2O4·2H2O],将溶液稍加热后,在搅拌下缓慢向烧杯中分批加入草酸晶体粉末。待充分反应后过滤得到浅粉色溶液,将溶液蒸发浓缩,加入适量乙醇冷却结晶,干燥后得MnSO4·H2O。
①实验中配制100mL6.00mol/L硫酸时,需要的仪器有量筒、烧杯、玻璃棒、胶头滴管和____________ 。
②在上述过程中,若MnO2的转化率为97.44%,则最终得到MnSO4·H2O晶体的质量为________ g。
(2)乙组同学拟研究硫酸锰的高温分解产物,用下图装置测量生成的Mn3O4、SO2、SO3及水蒸气。

①装置正确的连接顺序为_________________ (按气流方向,填装置序号)。
②实验自始至终均需通入N2,其目的是______________ 。
③若起始时,在装置Ⅱ中加入MnSO4·H2O50.7g,充分反应后,测得装置Ⅲ增重6.4g,则MnSO4·H2O分解的化学方程式为________________________ 。
(1)甲组同学拟制备MnSO4·H2O。
首先称取5.0gMnO2于200mL烧杯中,加入12.00mL6.00mol/L硫酸和6.00mLH2O。然后再称取8.0g草酸晶体[H2C2O4·2H2O],将溶液稍加热后,在搅拌下缓慢向烧杯中分批加入草酸晶体粉末。待充分反应后过滤得到浅粉色溶液,将溶液蒸发浓缩,加入适量乙醇冷却结晶,干燥后得MnSO4·H2O。
①实验中配制100mL6.00mol/L硫酸时,需要的仪器有量筒、烧杯、玻璃棒、胶头滴管和
②在上述过程中,若MnO2的转化率为97.44%,则最终得到MnSO4·H2O晶体的质量为
(2)乙组同学拟研究硫酸锰的高温分解产物,用下图装置测量生成的Mn3O4、SO2、SO3及水蒸气。

①装置正确的连接顺序为
②实验自始至终均需通入N2,其目的是
③若起始时,在装置Ⅱ中加入MnSO4·H2O50.7g,充分反应后,测得装置Ⅲ增重6.4g,则MnSO4·H2O分解的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】钴蓝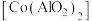 是一种重要的蓝色颜料。利用含钴废料(主要成分为
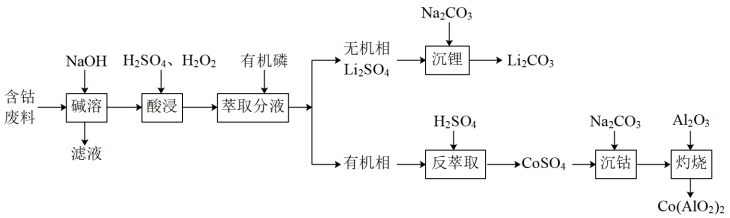
是一种重要的蓝色颜料。利用含钴废料(主要成分为 ,还含有少量的铝箔)制备钴蓝的一种工艺流程如图:
,还含有少量的铝箔)制备钴蓝的一种工艺流程如图:
已知: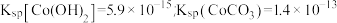
请回答以下问题:
(1)Co元素位于元素周期表第_______ 周期第_______ 族
(2)写出“酸浸”步骤中 发生反应的化学方程式
发生反应的化学方程式_______ ;在实际生产中,“酸浸”不用盐酸的原因是_______
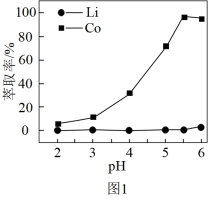
(3)已知钴、锂在有机磷萃取剂中的萃取率与pH的关系如图1所示,则有机磷萃取的最佳pH为_______
(4)根据图2判断,“沉锂”步骤中获取 的操作依次是
的操作依次是_______ 、_______ 、洗涤、干燥

(5)若 溶液中
溶液中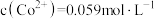 ,为防止沉钴过程中产生
,为防止沉钴过程中产生 沉淀,需控制溶液的pH不高于
沉淀,需控制溶液的pH不高于_______ (保留一位小数)
(6)写出灼烧过程中主要反应的化学方程式_______
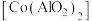 是一种重要的蓝色颜料。利用含钴废料(主要成分为
是一种重要的蓝色颜料。利用含钴废料(主要成分为 ,还含有少量的铝箔)制备钴蓝的一种工艺流程如图:
,还含有少量的铝箔)制备钴蓝的一种工艺流程如图:
已知:
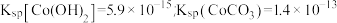
请回答以下问题:
(1)Co元素位于元素周期表第
(2)写出“酸浸”步骤中
 发生反应的化学方程式
发生反应的化学方程式(3)已知钴、锂在有机磷萃取剂中的萃取率与pH的关系如图1所示,则有机磷萃取的最佳pH为

(4)根据图2判断,“沉锂”步骤中获取
 的操作依次是
的操作依次是
(5)若
 溶液中
溶液中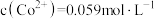 ,为防止沉钴过程中产生
,为防止沉钴过程中产生 沉淀,需控制溶液的pH不高于
沉淀,需控制溶液的pH不高于(6)写出灼烧过程中主要反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】 在中性或碱性溶液中稳定,在酸性溶液中不稳定。由S和
在中性或碱性溶液中稳定,在酸性溶液中不稳定。由S和 溶液制备硫代硫酸钠的反应为
溶液制备硫代硫酸钠的反应为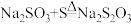 。实验室常用的制备方法是向
。实验室常用的制备方法是向 和
和 的混合溶液中通入
的混合溶液中通入 ,制备
,制备 晶体的实验步骤如下:
晶体的实验步骤如下:
①将含有煤粉的工业硫化钠提纯得到硫化的晶体( )。
)。
②按图安装制备硫代硫酸钠的装置,并检查装置的气密性。

③称取提纯后的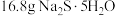 ,
,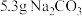 ,放入250mL锥形瓶中,加入150mL蒸馏水使其溶解。
,放入250mL锥形瓶中,加入150mL蒸馏水使其溶解。
④打开分液漏斗,使70%浓硫酸慢慢滴下。打开螺旋夹,使反应产生的气体均匀地通入 、
、 的混合溶液中,并用电磁搅拌器搅拌。随着气体的通入,逐渐有大量浅黄色固体析出。继续通入
的混合溶液中,并用电磁搅拌器搅拌。随着气体的通入,逐渐有大量浅黄色固体析出。继续通入 气体,浅黄色固体逐渐减少,反应进行约1h,控制锥形瓶中混合溶液的pH不小于7。
气体,浅黄色固体逐渐减少,反应进行约1h,控制锥形瓶中混合溶液的pH不小于7。
⑤过滤锥形瓶中的混合溶液,蒸发浓缩滤液至有晶体析出,停止蒸发,冷却,析出 晶体,过滤、洗涤、干燥,称量得到27.9g产品。
晶体,过滤、洗涤、干燥,称量得到27.9g产品。
回答下列问题:
(1)将含有煤粉的工业硫化钠提纯得到 的操作如下,正确的顺序是
的操作如下,正确的顺序是________ (填字母)。
A.趁热过滤 B.加热溶解 C.过滤、洗涤,干燥 D.冷却结晶
(2)实验室称量硫化钠晶体和 的质量需要使用的主要仪器有镊子、药匙、砝码、称量瓶和
的质量需要使用的主要仪器有镊子、药匙、砝码、称量瓶和_____ 。
(3)向锥形瓶中通入 气体时,若观察到锥形瓶中出现倒吸现象,可以
气体时,若观察到锥形瓶中出现倒吸现象,可以___________ (填操作)防止倒吸。锥形瓶中小磁铁的作用是______________________________ 。
(4) 与
与 反应析出浅黄色固体的化学方程式为
反应析出浅黄色固体的化学方程式为___________________ ;能说明锥形瓶中溶液与 气体发生放热反应的依据是
气体发生放热反应的依据是_________________________ ;控制锥形瓶中混合溶液的pH不小于7的原因是____________ 。
(5)硫代硫酸钠晶体( )的产率为
)的产率为__________ 。
 在中性或碱性溶液中稳定,在酸性溶液中不稳定。由S和
在中性或碱性溶液中稳定,在酸性溶液中不稳定。由S和 溶液制备硫代硫酸钠的反应为
溶液制备硫代硫酸钠的反应为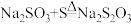 。实验室常用的制备方法是向
。实验室常用的制备方法是向 和
和 的混合溶液中通入
的混合溶液中通入 ,制备
,制备 晶体的实验步骤如下:
晶体的实验步骤如下:①将含有煤粉的工业硫化钠提纯得到硫化的晶体(
 )。
)。②按图安装制备硫代硫酸钠的装置,并检查装置的气密性。

③称取提纯后的
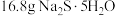 ,
,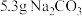 ,放入250mL锥形瓶中,加入150mL蒸馏水使其溶解。
,放入250mL锥形瓶中,加入150mL蒸馏水使其溶解。④打开分液漏斗,使70%浓硫酸慢慢滴下。打开螺旋夹,使反应产生的气体均匀地通入
 、
、 的混合溶液中,并用电磁搅拌器搅拌。随着气体的通入,逐渐有大量浅黄色固体析出。继续通入
的混合溶液中,并用电磁搅拌器搅拌。随着气体的通入,逐渐有大量浅黄色固体析出。继续通入 气体,浅黄色固体逐渐减少,反应进行约1h,控制锥形瓶中混合溶液的pH不小于7。
气体,浅黄色固体逐渐减少,反应进行约1h,控制锥形瓶中混合溶液的pH不小于7。⑤过滤锥形瓶中的混合溶液,蒸发浓缩滤液至有晶体析出,停止蒸发,冷却,析出
 晶体,过滤、洗涤、干燥,称量得到27.9g产品。
晶体,过滤、洗涤、干燥,称量得到27.9g产品。回答下列问题:
(1)将含有煤粉的工业硫化钠提纯得到
 的操作如下,正确的顺序是
的操作如下,正确的顺序是A.趁热过滤 B.加热溶解 C.过滤、洗涤,干燥 D.冷却结晶
(2)实验室称量硫化钠晶体和
 的质量需要使用的主要仪器有镊子、药匙、砝码、称量瓶和
的质量需要使用的主要仪器有镊子、药匙、砝码、称量瓶和(3)向锥形瓶中通入
 气体时,若观察到锥形瓶中出现倒吸现象,可以
气体时,若观察到锥形瓶中出现倒吸现象,可以(4)
 与
与 反应析出浅黄色固体的化学方程式为
反应析出浅黄色固体的化学方程式为 气体发生放热反应的依据是
气体发生放热反应的依据是(5)硫代硫酸钠晶体(
 )的产率为
)的产率为
您最近一年使用:0次



