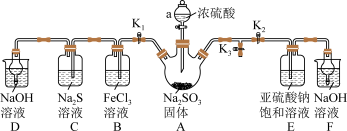
请回答下列问题:(实验前已除去装置中的空气)
(1)关闭K2、K3,打开K1,装置B中发生反应的离子方程式为
(2)装置D和F的作用是
(3)实验前,装置E中所用蒸馏水需经煮沸后迅速冷却,关闭K1、K3,打开K2,一段时间后装置E中有Na2S2O5晶体析出,装置E中发生反应的化学方程式为
(4)设计实验验证Na2S2O5晶体在空气中已被氧化,所需试剂为
(5)从化合价的角度分析Na2S2O5是否具有氧化性,可以利用
(6)实验前,装置E中所用蒸馏水需经煮沸后迅速冷却,目的是
相似题推荐
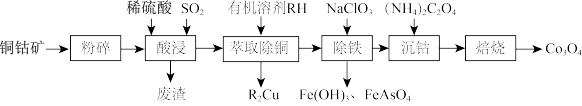
已知:①酸浸液中阳离子为Fe2+、Cu2+、Co2+、H+
②萃取铜的过程可表示为Cu2+(aq)+RH(有机物)=R2Cu(有机物)+2H+(aq)
③Ksp[Fe(OH)3]=2.8×10-39,Ksp(FeAsO4)=6.8×10-19
(1)Cu在周期表中的位置为
(2)酸浸液中钴以CoSO4形式存在,生成CoSO4的化学方程式为
(3)在除铁过程中,溶液中的AsO
 转化为FeAsO4沉淀,该反应的离子方程式为
转化为FeAsO4沉淀,该反应的离子方程式为 的浓度为
的浓度为(4)焙烧过程中,若空气与CoC2O4接触不充分,废气中会含有
 和
和 )并将其资源化的工艺有多种,其中一种工艺如图所示:
)并将其资源化的工艺有多种,其中一种工艺如图所示: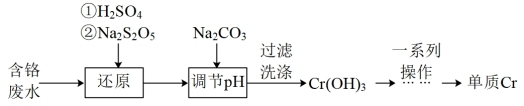
已知:Cr(OH)3受热易分解。
回答下列问题:
(1)
 中Cr元素的化合价为
中Cr元素的化合价为(2)加入H2SO4酸化的目的是将
 转变为
转变为 ,不选用稀HCl酸化的原因可能
,不选用稀HCl酸化的原因可能(3)焦亚硫酸钠(Na2S2O5)的投加量对Cr(VI)含量的影响如图所示。焦亚硫酸钠的最佳投加量为
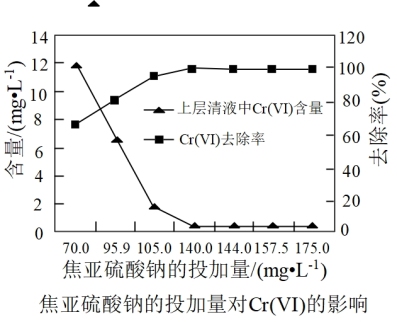
(4)“一系列操作”包含
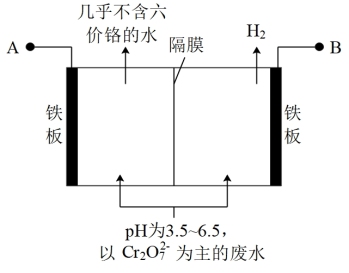
(5)工业上也常用电解法处理酸性含铬废水。用铁板作电极,在耐酸电解槽中盛放酸性含
 的废水,原理如图所示。则与B相连的铁板为电解池的
的废水,原理如图所示。则与B相连的铁板为电解池的{已如Ksp[Fe(OH)3]=2.8×10-39,Ksp[Cr(OH)3]=5.6×10-31}
【推荐3】工业上用低品铜矿(主要含CuS、FeO等)制备氯化亚铜(CuCl)的一种工艺流程如图:
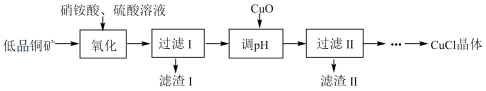
已知:①CuCl微溶于水,不溶于乙醇,露置于潮湿的空气中易被氧化。
②“氧化”时,NO 中N元素主要被还原为最低价态,少部分被还原为NO。
中N元素主要被还原为最低价态,少部分被还原为NO。
(1)①“氧化”阶段的温度需控制在65℃,其适宜的加热方式为
②该步骤中FeO被NH4NO3氧化,其主要反应的离子方程式:
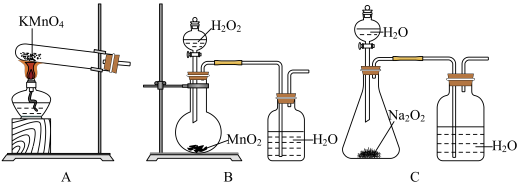
(2)在实验室进行实验时,“氧化”阶段反应可在如图所示装置中进行:
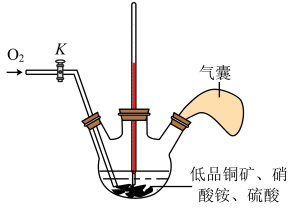
①实验开始时,温度计显示反应液温度低于室温,主要原因是
②通入氧气的目的是
③为便于观察和控制产生O2的速率,制备氧气的装置最好选用
(3)已知常温下CuCl在水溶液中Ksp=1.2×10-6,工艺流程最后一步析出CuCl晶体后的溶液中,如果c(Cl-)=4.0mol·L-1,则c(Cu+)=
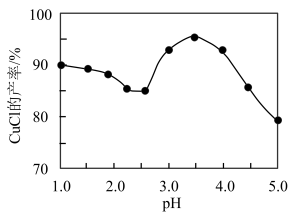
(4)已知pH对CuCl沉淀率的影响如图所示,请设计从“过滤II”所得的滤液中获取CuCl的实验方案:
| X | 宇宙中含量最丰富的元素 |
| Y | 植物生长所必需的三种营养元素中,电负性最大的 |
| Z | 原子最外层电子数是其电子层数的3倍 |
| Q | 其气态氢化物与其低价氧化物常温下能反应,生成该元素的单质 |
| T | 最高正价与最低负价代数和为6,其单质能与强碱溶液反应制消毒液 |
| W | 其+2价阳离子的价电子排布为3d9 |
(1)W元素位于周期表的第
(2)X与Z按原子个数比为1:1组合得到的一种物质甲,它能用于杀菌消毒,物质甲的电子式为
(3)元素Q的简单离子半径
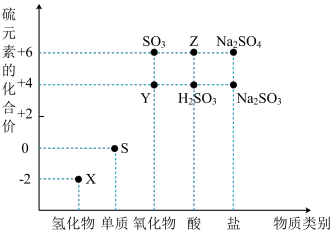
(1)S在周期表中的位置是
(2)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(3)Na2S2O3是重要的化工原料。从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
(4)已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则24 mL 0.05 mol·L-1的Na2SO3溶液与20 mL 0.02 mol·L-1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为
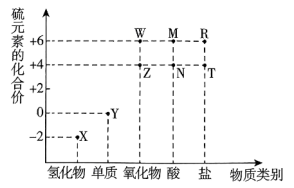
(1)T是一种由四种元素组成的钠盐,其电离方程式为
(2)Z是形成酸雨的主要物质之一,用化学式表示由Z形成酸雨的过程
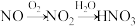 )。
)。(3)Fe2(SO4)3溶液脱除空气污染物X并再生的原理如图所示。

反应Ⅰ的离子方程式为
(4)海水提溴时,先用Cl2氧化海水中的
 ,热空气吹出Br2后用Z进行吸收,再通入Cl2氧化,最后蒸馏得到液溴。两次通入Cl2氧化的目的是
,热空气吹出Br2后用Z进行吸收,再通入Cl2氧化,最后蒸馏得到液溴。两次通入Cl2氧化的目的是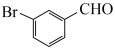 )是有机合成的重要中间体,低温下较稳定,高温易被氧化。兴趣小组同学利用如下装置制取间溴苯甲醛(加热及夹持装置略):
)是有机合成的重要中间体,低温下较稳定,高温易被氧化。兴趣小组同学利用如下装置制取间溴苯甲醛(加热及夹持装置略):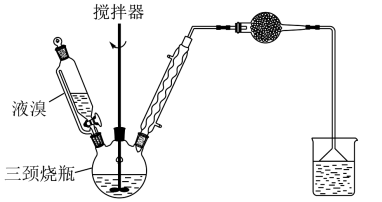
已知:有关数据见表(101kPa)
| 物质 | 溴分子 | 苯甲醛 | 1,2-二氯乙烷 | 间溴苯甲醛 | 无水 |
| 沸点/℃ | 58.8 | 179 | 83.5 | 229178 | |
| 溶解性 | 微溶于水 | 微溶于水 | 难溶于水 | 难溶于水 | 遇水水解 |
| 相对分子质量 | 160 | 106 | — | 185 | — |
步骤1:按照一定配比将5.3g苯甲醛、有机溶剂(1,2-二氯乙烷)和催化剂(无水
 )加入三颈烧瓶中充分混合,升温至60℃,缓慢滴加足量液溴,保温反应一段时间,冷却。
)加入三颈烧瓶中充分混合,升温至60℃,缓慢滴加足量液溴,保温反应一段时间,冷却。步骤2:将反应混合物缓慢加入一定量的稀盐酸中,搅拌、静置、分液。有机相用10%
 溶液洗涤后再水洗。
溶液洗涤后再水洗。步骤3:经洗涤的有机相加入适量无水
 固体,放置一段时间,过滤。
固体,放置一段时间,过滤。步骤4:减压蒸馏,收集122℃~124℃的馏分。
回答下列问题:
(1)步骤1反应化学方程式为
(2)冷凝管的主要作用是冷凝回流,其目的是
(3)烧杯内盛有的溶液是
 ,其作用是
,其作用是(4)步骤2中使用10%的
 溶液洗涤有机相,是为了除去溶于有机相的
溶液洗涤有机相,是为了除去溶于有机相的(5)步骤4中采用减压蒸馏的目的是
(6)若实验得到3.7g间溴苯甲醛,则间溴苯甲醛产率为
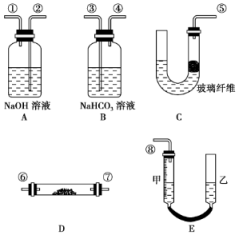
上图中量气装置E是由甲、乙两根玻璃管组成,它们用橡皮管连通,并装入适量水。甲管有刻度(0~50 mL),供量气用;乙管可上下移动,以调节液面高低。
实验室可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水。上述装置的连接顺序是⑤③④⑥⑦②①⑧(提示:B装置用来除去制得的CO2中的HCl)
试回答:
(1)写出装置D中的化学反应方程式
(2)C装置用来制取CO2,写出此装置中的化学反应方程式:
(3)装置A的作用是
(4)为了较准确地测量氧气的体积,除了必须检查整个装置的气密性之外,在读取反应前后甲管中液面的读数,求其差值的过程中,应注意
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管液面相平
(1)ClO2的制备(已知:SO2+2NaClO3+H2SO4═2ClO2+2NaHSO4。)
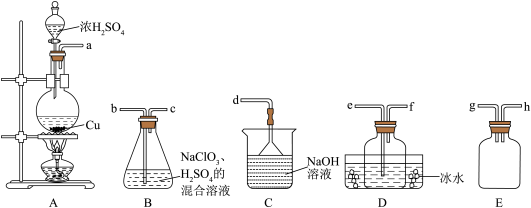
①整套装置正确的链接顺序为(填A~E)A→
②装置D的作用是
(2)ClO2与Na2S的反应
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入如图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究Ⅰ中反应的产物。

| 操作步骤 | 实验现象 | 结论 |
| 取少量Ⅰ中溶液于试管甲中,滴加品红溶液和盐酸 | 品红溶液始终不褪色 | ①无 |
| 另取少量Ⅰ中溶液于试管乙中,加入Ba(OH)2溶液,振荡 | ② | 有 生成 生成 |
| ③继续在试管乙中滴加Ba(OH)2溶液至过量,静置,取上层清液于试管丙中, | 有白色沉淀生成 | 有Cl-生成 |
④ClO2与Na2S反应的离子方程式为
(1)要说明Na2SO3具有氧化性,应选用的试剂是
(2)要说明Na2SO3具有还原性,应选用的试剂是
Ⅱ、某亚硫酸钠试剂已被部分氧化。为了确定它的纯度,要进行如下实验:
①称取样品 a g;
②将样品溶解;
③在溶液中加入稍过量的盐酸酸化的BaCl2溶液;
④将沉淀过滤,洗涤、干燥后称重,质量为b g。
试回答:
(3)BaCl2溶液要用盐酸酸化的原因是
(4)BaCl2溶液要稍过量的原因是
(5)判断沉淀是否洗尽的方法是
(6)Na2SO3样品纯度的计算式是
III、现有混有少量SO2杂质的CO2气体,请选用适当的实验装置,收集纯净干燥的CO2气体。
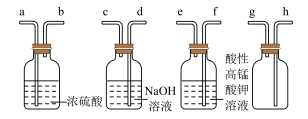
(7)①要达到实验目的,按气流从左到右,各接口连接顺序正确的是
A.dcabh B.feabh C.feabg
②本实验除去SO2的原理是利用SO2的

实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2 mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中离子。
Ⅶ.实验结束后,打开弹簧夹K1~K4,再通入一段时间N2,然后拆卸,洗涤,整理仪器。
(1)过程Ⅰ的目的是
(2)棉花中浸润的溶液为
(3)C中发生反应的化学方程式为
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是
| 过程Ⅳ中B溶液中含有的离子 | 过程Ⅵ中B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO |
| 乙 | 既有Fe3+又有Fe2+ | 有SO |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
(6)进行实验过程Ⅴ时,B中溶液颜色由黄色逐渐变为红棕色,停止通气,放置一段时间后溶液颜色变为浅绿色。
查阅资料:Fe2+(aq)+SO
 (aq)
(aq) FeSO3(s)(墨绿色)
FeSO3(s)(墨绿色)提出假设:FeCl3与SO2的反应经历了中间产物FeSO3,溶液的红棕色是FeSO3(墨绿色)与FeCl3(黄色)的混合色。
某同学设计如下实验,证实该假设成立:
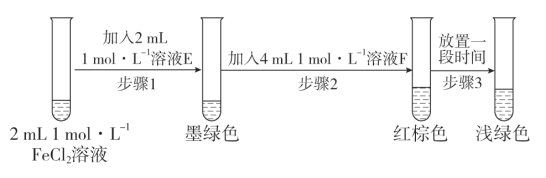
则溶液E和F分别为
Ⅰ.连二亚硫酸钠(Na2S2O4)。广泛应用于造纸等行业。利用NaBH4(H为-1价)溶液和Zn还原含硫物质均可制得Na2S2O4.实验室利用NaBH4碱性溶液制取Na2S2O4,实验装置如下图所示。
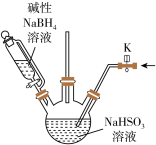
(1)实验前需打开K通入一段时间氮气,其目的是
(2)在10℃~35℃下,向盛有一定浓度的NaHSO3溶液容器中滴加NaBH4溶液,生成Na2S2O4和NaBO2.制备Na2S2O4的化学方程式为
Ⅱ.SO2、Na2SO3、Na2S2O5(焦亚硫酸钠)中都含有+4价的S。
(3)工业上常用SO2还原法制备粗碲:一定条件下,将SO2通入TeOSO4溶液中,反应一段时间后过滤、洗涤得到粗Te.反应中n(SO2):n(TeOSO4)=
(4)Na2SO3是实验室常用试剂。
①实验室用Na2SO3固体与浓硫酸制备SO2,该反应的化学方程式为
②在溴水中加入Na2SO3溶液反应的离子方程式为
(5)焦亚硫酸钠(Na2S2O5)空气法处理含氰废水的部分机理如下,其中[O]代表活性氧原子,具有强氧化性,发生如下反应
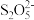 +H2O=2
+H2O=2 +2H+、
+2H+、 +O2=
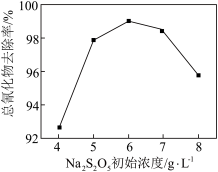
+O2= +[O]、CN-+[O]=CNO-。其他条件相同时,废水中氰化物去除率随Na2S2O5初始浓度的变化如图所示。当Na2S2O5初始浓度大于6g/L时,总氰化物去除率下降的原因可能是
+[O]、CN-+[O]=CNO-。其他条件相同时,废水中氰化物去除率随Na2S2O5初始浓度的变化如图所示。当Na2S2O5初始浓度大于6g/L时,总氰化物去除率下降的原因可能是