按要求回答下列问题:
(1)下列物质中属于强电解质的是______ (填标号,下同),非电解质是______ ,能导电的是______ 。
① ②
② ③氨水④液态
③氨水④液态 ⑤乙醇⑥
⑤乙醇⑥ ⑦
⑦ ⑧
⑧
(2)若 时,醋酸的电离常数
时,醋酸的电离常数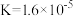 ,则该温度下
,则该温度下 醋酸溶液中
醋酸溶液中 约为
约为______  。
。
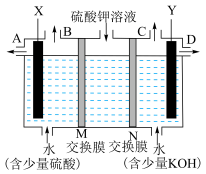
(3)用如图装置电解硫酸钾溶液,可获得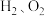 、硫酸和氢氧化钾溶液。电解过程中
、硫酸和氢氧化钾溶液。电解过程中 电极与电源的极
电极与电源的极______ 相连, 电极周围溶液
电极周围溶液 值
值______ (填“增大”、“减小”或“不变”),M、 交换膜中是阳离子交换膜的是
交换膜中是阳离子交换膜的是______ (填“M”或“N”)。
(4)现有反应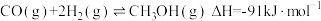 已知该反应中相关的化学键键能数据如下:
已知该反应中相关的化学键键能数据如下:
则气态 中
中 的键能为
的键能为______ 
(1)下列物质中属于强电解质的是
①
 ②
② ③氨水④液态
③氨水④液态 ⑤乙醇⑥
⑤乙醇⑥ ⑦
⑦ ⑧
⑧
(2)若
 时,醋酸的电离常数
时,醋酸的电离常数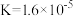 ,则该温度下
,则该温度下 醋酸溶液中
醋酸溶液中 约为
约为 。
。(3)用如图装置电解硫酸钾溶液,可获得
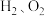 、硫酸和氢氧化钾溶液。电解过程中
、硫酸和氢氧化钾溶液。电解过程中 电极与电源的极
电极与电源的极 电极周围溶液
电极周围溶液 值
值 交换膜中是阳离子交换膜的是
交换膜中是阳离子交换膜的是
(4)现有反应
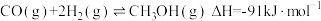 已知该反应中相关的化学键键能数据如下:
已知该反应中相关的化学键键能数据如下:| 化学键 | H—H | C—O | H—O | C—H |
 | 436 | 343 | 465 | 413 |
 中
中 的键能为
的键能为
更新时间:2023-12-21 11:19:08
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】已知下列十种物质:①液态HCl ;②FeCl3溶液; ③盐酸 ;④NH4Cl晶体 ;⑤蔗糖溶液; ⑥铜; ⑦碳酸钙; ⑧淀粉溶液 ;⑨熔融NaOH; ⑩CO2.根据上述提供的物质,回答下列问题:
(1)能够导电的是_______ ,属于强电解质的是_______ ,属于非电解质的是_______ 。(填序号)
(2)如图1是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,则E1_______ (填“增大”、“减小”或“不变”,下同),ΔH_______ 。请写出NO2和CO反应的热化学方程式:_______ 。

(3)观察图a和图b,根据盖斯定律,写出△H1、△H2、△H3、△H4、△H5和△H6的关系。图a:_______ ;图b:_______ 。

(4)用CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:① H2O(l)=H2O(g) △H=+44 kJ/mol
② 2N2(g)+CO2(g)+2H2O(g)=CH4(g)+4NO(g) △H= +1160 kJ/mol
③ CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H= -574 kJ/mol
请写出CH4(g)与NO2(g)反应生成参与大气循环的气体和液态水的热化学方程式_______ 。
(1)能够导电的是
(2)如图1是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,则E1

(3)观察图a和图b,根据盖斯定律,写出△H1、△H2、△H3、△H4、△H5和△H6的关系。图a:

(4)用CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:① H2O(l)=H2O(g) △H=+44 kJ/mol
② 2N2(g)+CO2(g)+2H2O(g)=CH4(g)+4NO(g) △H= +1160 kJ/mol
③ CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H= -574 kJ/mol
请写出CH4(g)与NO2(g)反应生成参与大气循环的气体和液态水的热化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了( (乙醇)、
(乙醇)、 、
、 、
、 、
、 ,图中相连的物质均可归为一类,相交部分A、
,图中相连的物质均可归为一类,相交部分A、 、C、D为相应的分类标准代号。
、C、D为相应的分类标准代号。
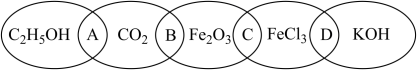
①相连的两种物质都是电解质的是___________ (填分类标准代号)。
② 中
中 的结构示意图是
的结构示意图是_______ 。
(2)分类方法应用广泛,属于同一类的物质具有相似性。
① 、
、 都属于酸性氧化物,
都属于酸性氧化物,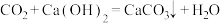 ,可得出
,可得出 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
②已知钾元素位于元素周期表中第四周期第ⅠA族,性质与钠相似,钾的原子序数为___________ 。钾单质与 反应的离子方程式为
反应的离子方程式为___________ 。
(3)某实验小组测定铁的氧化物 的化学式,已知该氧化物中铁元素只有+2和+3两种价态,实验步骤如图所示:
的化学式,已知该氧化物中铁元素只有+2和+3两种价态,实验步骤如图所示:
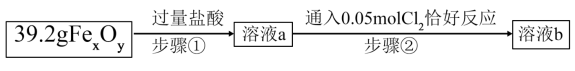
①为证明步骤②中 已反应完全,可选择下列的试剂有
已反应完全,可选择下列的试剂有_______ (填序号)。
A.铁氰化钾溶液 B.酸性 溶液
溶液
C. 溶液 D.
溶液 D. 溶液
溶液
②该氧化物的化学式为_______ 。
(1)如图为五个椭圆交叉构成的图案,其中五个椭圆内分别写了(
 (乙醇)、
(乙醇)、 、
、 、
、 、
、 ,图中相连的物质均可归为一类,相交部分A、
,图中相连的物质均可归为一类,相交部分A、 、C、D为相应的分类标准代号。
、C、D为相应的分类标准代号。
①相连的两种物质都是电解质的是
②
 中
中 的结构示意图是
的结构示意图是(2)分类方法应用广泛,属于同一类的物质具有相似性。
①
 、
、 都属于酸性氧化物,
都属于酸性氧化物,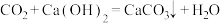 ,可得出
,可得出 与
与 反应的化学方程式为
反应的化学方程式为②已知钾元素位于元素周期表中第四周期第ⅠA族,性质与钠相似,钾的原子序数为
 反应的离子方程式为
反应的离子方程式为(3)某实验小组测定铁的氧化物
 的化学式,已知该氧化物中铁元素只有+2和+3两种价态,实验步骤如图所示:
的化学式,已知该氧化物中铁元素只有+2和+3两种价态,实验步骤如图所示:
①为证明步骤②中
 已反应完全,可选择下列的试剂有
已反应完全,可选择下列的试剂有A.铁氰化钾溶液 B.酸性
 溶液
溶液C.
 溶液 D.
溶液 D. 溶液
溶液②该氧化物的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】氯化钠是日常生活必需品和重要的化工原料。
(1)NaCl固体是否属于电解质?______ ,是否能导电?______ (填写“是”或“否”)。
(2)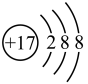 表示
表示______ 。
A.氯原子的结构示意图
B.氯离子的结构示意图
(3)实验室提纯粗盐时,将粗盐溶于水后,先除去泥沙等难溶性杂质,再除去Ca2+、Mg2+、SO 等可溶性杂质。
等可溶性杂质。
①写出NaCl溶于水时的电离方程式______ 。
②为了除去可溶性杂质,依次加入稍过量的BaCl2溶液、NaOH溶液和Na2CO3溶液,加热至70℃左右约2min,冷却后过滤,得到的沉淀有BaSO4、Mg(OH)2、CaCO3和______ 。
(4)“84消毒液”是常见的消毒剂,其有效成分是NaClO。
①Cl2和NaOH制备NaClO的离子方程式为_______ 。
如图是某品牌“84消毒液”的使用注意事项。
②注意事项4“易使有色衣物脱色”,是因为“84消毒液”具有______ 。
A.碱性 B.强氧化性
③注意事项6“不可与酸性物质同时使用”,例如,若将“84消毒液”与“洁厕灵”(含盐酸)同时使用会生成黄绿色有毒气体。写出反应的离子方程式_______ 。
(1)NaCl固体是否属于电解质?
(2)
 表示
表示A.氯原子的结构示意图
B.氯离子的结构示意图
(3)实验室提纯粗盐时,将粗盐溶于水后,先除去泥沙等难溶性杂质,再除去Ca2+、Mg2+、SO
 等可溶性杂质。
等可溶性杂质。①写出NaCl溶于水时的电离方程式
②为了除去可溶性杂质,依次加入稍过量的BaCl2溶液、NaOH溶液和Na2CO3溶液,加热至70℃左右约2min,冷却后过滤,得到的沉淀有BaSO4、Mg(OH)2、CaCO3和
(4)“84消毒液”是常见的消毒剂,其有效成分是NaClO。
①Cl2和NaOH制备NaClO的离子方程式为
如图是某品牌“84消毒液”的使用注意事项。
| 注意事项 1、外用消毒液,勿口服; 2、现用现配,使用时注意戴手套防护; 3、不适用于钢和铝制品的消毒; 4、易使有色衣物脱色; 5、避光、阴凉处保存; 6、不可与酸性物质同时使用. |
A.碱性 B.强氧化性
③注意事项6“不可与酸性物质同时使用”,例如,若将“84消毒液”与“洁厕灵”(含盐酸)同时使用会生成黄绿色有毒气体。写出反应的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】氨既是一种重要的化工产品,又是一种重要的化工原料。如图为合成氨以及氨氧化制硝酸的流程示意图。
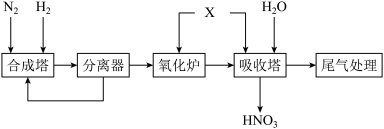
(1)合成塔中发生反应的化学方程式为_______ 。
(2)单质X的化学式是_______ 。 吸收塔中X的作用是_______ 。
(3)工业上为了储运浓硝酸,最好选择_______作为罐体材料。
(4)为避免硝酸生产尾气中的氮氧化物污染环境,工业上常用Na2CO3吸收尾气,发生的反应为:NO+NO2+Na2CO3 =2NaNO2+CO2、2NO2+Na2CO3=NaNO2+NaNO3+CO2,将标准状况下44.8L仅含NO和NO2混合气体的尾气通入Na2CO3溶液中,尾气被完全吸收,则消耗的Na2CO3的物质的量为_______ mol。
将拆开或形成1mol化学键所需要的能量称为键能(kJ·mol-1)。表中是一些共价键的键能:
(5)根据表中的数据判断工业合成氨的反应是_______ (填“吸热”或“放热”)反应;
(6)取一定量N2和H2放入一密闭容器中,在一定条件下进行反应,理论上生成2molNH3时放出或吸收的热量为QkJ,则Q=_______ 。

(1)合成塔中发生反应的化学方程式为
(2)单质X的化学式是
(3)工业上为了储运浓硝酸,最好选择_______作为罐体材料。
| A.铜 | B.铂 | C.铝 | D.镁 |
将拆开或形成1mol化学键所需要的能量称为键能(kJ·mol-1)。表中是一些共价键的键能:
| 共价键 | H-H | N≡N | N-H |
| 键能(kJ·mol-1) | 436 | 945 | 391 |
(6)取一定量N2和H2放入一密闭容器中,在一定条件下进行反应,理论上生成2molNH3时放出或吸收的热量为QkJ,则Q=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】请按要求填空:
(1)已知热化学方程式:SO2(g)+ O2(g)
O2(g)  SO3(g) ΔH=
SO3(g) ΔH= 98.32
98.32  ,在容器中充入2 mol SO2和1 mol O2,充分反应,最终放出的热量_______(填字母)。
,在容器中充入2 mol SO2和1 mol O2,充分反应,最终放出的热量_______(填字母)。
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
①2SO2(g)+O2(g) 2SO3(g) ΔH1=
2SO3(g) ΔH1= 197
197  ;
;
②H2O(g)=H2O(l) ΔH2= 44
44  ;
;
③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3= 545
545 
则SO3(g)与H2O(l)反应的热化学方程式是_______ 。
(3)已知下列两个热化学方程式:
H2(g)+ O2(g)=H2O(l) ΔH=
O2(g)=H2O(l) ΔH= 285.0
285.0 
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH= 2220.0
2220.0 
①实验测得H2和C3H8的混合气体共5 mol,完全燃烧生成液态水时放热6262.5 kJ,则混合气体中H2和C3H8的体积之比为_______ 。
②已知:H2O(l)=H2O(g) ΔH=+44.0 ,写出C3H8燃烧生成CO2和气态水的热化学方程式:
,写出C3H8燃烧生成CO2和气态水的热化学方程式:_______ 。
(4)已知:2CO(g)+O2(g)=2CO2(g) ΔH= 566
566  ①
①
Na2O2(s)+CO2(g)=Na2CO3(s)+ O2(g) ΔH=
O2(g) ΔH= 226
226  ②
②
则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为_______ 。
(5)已知H2(g)+Br2(l)=2HBr(g) ΔH= 72
72  ,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
则表中a=_______ 。
(1)已知热化学方程式:SO2(g)+
 O2(g)
O2(g)  SO3(g) ΔH=
SO3(g) ΔH= 98.32
98.32  ,在容器中充入2 mol SO2和1 mol O2,充分反应,最终放出的热量_______(填字母)。
,在容器中充入2 mol SO2和1 mol O2,充分反应,最终放出的热量_______(填字母)。| A.=196.64 kJ | B.=98.32 kJ | C.<196.64 kJ | D.>196.64 kJ |
(2)FeS2焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
①2SO2(g)+O2(g)
 2SO3(g) ΔH1=
2SO3(g) ΔH1= 197
197  ;
;②H2O(g)=H2O(l) ΔH2=
 44
44  ;
;③2SO2(g)+O2(g)+2H2O(g)=2H2SO4(l) ΔH3=
 545
545 
则SO3(g)与H2O(l)反应的热化学方程式是
(3)已知下列两个热化学方程式:
H2(g)+
 O2(g)=H2O(l) ΔH=
O2(g)=H2O(l) ΔH= 285.0
285.0 
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=
 2220.0
2220.0 
①实验测得H2和C3H8的混合气体共5 mol,完全燃烧生成液态水时放热6262.5 kJ,则混合气体中H2和C3H8的体积之比为
②已知:H2O(l)=H2O(g) ΔH=+44.0
 ,写出C3H8燃烧生成CO2和气态水的热化学方程式:
,写出C3H8燃烧生成CO2和气态水的热化学方程式:(4)已知:2CO(g)+O2(g)=2CO2(g) ΔH=
 566
566  ①
①Na2O2(s)+CO2(g)=Na2CO3(s)+
 O2(g) ΔH=
O2(g) ΔH= 226
226  ②
②则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为
(5)已知H2(g)+Br2(l)=2HBr(g) ΔH=
 72
72  ,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:
,蒸发1 mol Br2(l)需要吸收的能量为30 kJ,其他相关数据如下表:| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1 mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 200 | a |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】一氯甲烷广泛用作溶剂、提取剂、推进剂、制冷剂、甲基化试剂,用于生产农药、医药等。600K时, 和
和 作用生成
作用生成 ,
, 可继续反应生成
可继续反应生成 。反应原理如下:
。反应原理如下:
①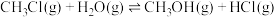

②
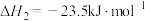
(1)已知反应①中相关化学键的键能数据如表:
则
___________  。
。
上述反应体系在一定条件下建立平衡后,下列说法正确的是___________ (填标号)。
A.升高温度反应①正向移动,反应②逆向移动
B.加入反应①的催化剂,可以降低反应的活化能及反应热
C.增大水蒸气浓度有利于提高 的产量
的产量
D.及时分离出 可以使反应①的正反应速率增大
可以使反应①的正反应速率增大
(2)对于反应②,反应速率与浓度之间存在如下关系: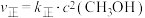 ,
,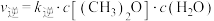 ,
, 、
、 为速率常数,只受温度影响,k和温度的关系为
为速率常数,只受温度影响,k和温度的关系为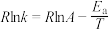 (
( 为活化能,k为速率常数,R、A为常数)。右图中两条直线分别表示
为活化能,k为速率常数,R、A为常数)。右图中两条直线分别表示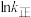 和
和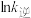 与
与 的关系,表示
的关系,表示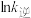 的是
的是___________ (填“a”或“b”),温度为 时,反应②的平衡常数K=
时,反应②的平衡常数K=___________ 。

(3)在恒温条件下,向2L恒容密闭容器中,充入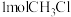 和
和 发生反应,甲醇的物质的量随时间变化如图所示:
发生反应,甲醇的物质的量随时间变化如图所示:
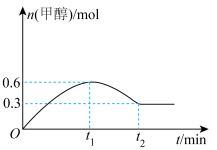
 时,水的体积分数为65%,则
时,水的体积分数为65%,则 的转化率为
的转化率为___________ ,反应①的平衡常数
___________ [对于反应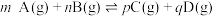 ,
,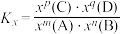 ,x为物质的量分数]。
,x为物质的量分数]。
(4)甲醇也可通过电化学方法由甲烷直接制得,装置如图所示:
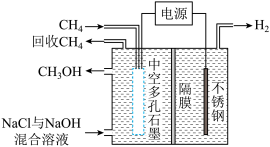
已知,电解生成甲醇的过程分3步:
①通电时,氯离子先转化成高活性的原子氯(Cl·);②Cl·与吸附在电极上的 反应生成HCl和
反应生成HCl和 ;③在碱性电解液中,
;③在碱性电解液中, 转化为目标产物
转化为目标产物 。当步骤①有2molCl·生成时,外电路中转移的电子数为
。当步骤①有2molCl·生成时,外电路中转移的电子数为___________ (用含 的代数式表示)。阴极的电极反应为
的代数式表示)。阴极的电极反应为___________ 。
 和
和 作用生成
作用生成 ,
, 可继续反应生成
可继续反应生成 。反应原理如下:
。反应原理如下:①
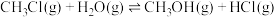

②

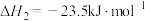
(1)已知反应①中相关化学键的键能数据如表:
| 化学键 | C-Cl | C-H | C-O | H-Cl | H-O |
键能 | 331 | 414 | 343 | 429 | 460 |

 。
。上述反应体系在一定条件下建立平衡后,下列说法正确的是
A.升高温度反应①正向移动,反应②逆向移动
B.加入反应①的催化剂,可以降低反应的活化能及反应热
C.增大水蒸气浓度有利于提高
 的产量
的产量D.及时分离出
 可以使反应①的正反应速率增大
可以使反应①的正反应速率增大(2)对于反应②,反应速率与浓度之间存在如下关系:
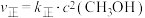 ,
,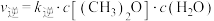 ,
, 、
、 为速率常数,只受温度影响,k和温度的关系为
为速率常数,只受温度影响,k和温度的关系为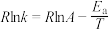 (
( 为活化能,k为速率常数,R、A为常数)。右图中两条直线分别表示
为活化能,k为速率常数,R、A为常数)。右图中两条直线分别表示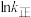 和
和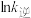 与
与 的关系,表示
的关系,表示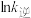 的是
的是 时,反应②的平衡常数K=
时,反应②的平衡常数K=
(3)在恒温条件下,向2L恒容密闭容器中,充入
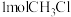 和
和 发生反应,甲醇的物质的量随时间变化如图所示:
发生反应,甲醇的物质的量随时间变化如图所示:
 时,水的体积分数为65%,则
时,水的体积分数为65%,则 的转化率为
的转化率为
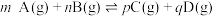 ,
,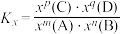 ,x为物质的量分数]。
,x为物质的量分数]。(4)甲醇也可通过电化学方法由甲烷直接制得,装置如图所示:

已知,电解生成甲醇的过程分3步:
①通电时,氯离子先转化成高活性的原子氯(Cl·);②Cl·与吸附在电极上的
 反应生成HCl和
反应生成HCl和 ;③在碱性电解液中,
;③在碱性电解液中, 转化为目标产物
转化为目标产物 。当步骤①有2molCl·生成时,外电路中转移的电子数为
。当步骤①有2molCl·生成时,外电路中转移的电子数为 的代数式表示)。阴极的电极反应为
的代数式表示)。阴极的电极反应为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】电化学原理在探究物质性质和实际生产中应用广泛,据此回答下列问题。

(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由装置甲知铬的金属活动性比铜_______ (填“强”或“弱”);由装置乙知常温下铬在浓硝酸中出现_______ 现象(填化学专业名词)。
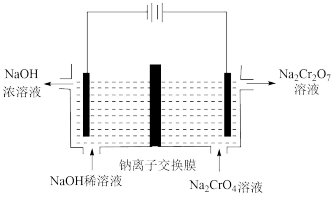
(2)已知存在反应:2 +2H+⇌
+2H+⇌ +H2O。用下图装置,以石墨作电极电解Na2CrO4溶液制备Na2Cr2O7的转化原理为
+H2O。用下图装置,以石墨作电极电解Na2CrO4溶液制备Na2Cr2O7的转化原理为_______ 。
(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(VI)转化为Cr(III)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和
的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和 发生反应,则阳极的电极反应式为
发生反应,则阳极的电极反应式为_______ 。阴极上 、H+、Fe3+都可能放电。若
、H+、Fe3+都可能放电。若 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为_______ ;若H+放电,则阴极区形成_______ 和Cr(OH)3沉淀。
②铁氧磁体法:在含Cr(VI)的废水中加入FeSO4,在pH<4时发生反应使Cr(VI)转化为Cr(III),调节溶液pH为6~8,使溶液中的Fe(II)、Fe(III)、Cr(III)析出组成相当于Fe(II)[Fe(III)x·Cr(III)2-x]O4(铁氧磁体)的沉淀,则铁氧磁体中x=_______ 。

(1)在如图装置中,观察到装置甲铜电极上产生大量的无色气体;而装置乙中铜电极上无气体产生,铬电极上产生大量红棕色气体。由装置甲知铬的金属活动性比铜
(2)已知存在反应:2
 +2H+⇌
+2H+⇌ +H2O。用下图装置,以石墨作电极电解Na2CrO4溶液制备Na2Cr2O7的转化原理为
+H2O。用下图装置,以石墨作电极电解Na2CrO4溶液制备Na2Cr2O7的转化原理为
(3)CrO3和K2Cr2O7均易溶于水,它们是工业废水造成铬污染的主要原因。要将Cr(VI)转化为Cr(III)常见的处理方法是电解法和铁氧磁体法。
①电解法:将含
 的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和
的废水通入电解槽内,用铁作阳极,在酸性环境中,加入适量的NaCl进行电解,使阳极产物和 发生反应,则阳极的电极反应式为
发生反应,则阳极的电极反应式为 、H+、Fe3+都可能放电。若
、H+、Fe3+都可能放电。若 放电,则阴极的电极反应式为
放电,则阴极的电极反应式为②铁氧磁体法:在含Cr(VI)的废水中加入FeSO4,在pH<4时发生反应使Cr(VI)转化为Cr(III),调节溶液pH为6~8,使溶液中的Fe(II)、Fe(III)、Cr(III)析出组成相当于Fe(II)[Fe(III)x·Cr(III)2-x]O4(铁氧磁体)的沉淀,则铁氧磁体中x=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
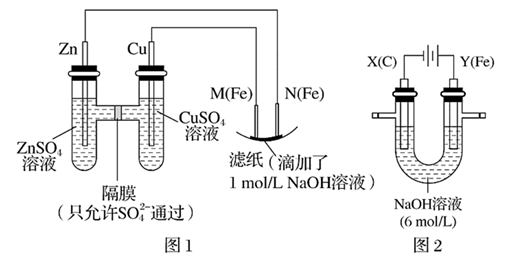
请回答:Ⅰ.用如图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,能替代Cu做电极的是___________(填字母序号)。
(2)M极发生反应的电极反应式为___________ ;
Ⅱ.用如图 所示装置进行第二组实验。实验过程中,两极均有气体产生,
所示装置进行第二组实验。实验过程中,两极均有气体产生, 极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(
极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(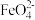 )在溶液中呈紫红色。
)在溶液中呈紫红色。
(3)电解过程中, 极区溶液的
极区溶液的
_____ (填“增大”、“减小”或“不变”);
(4)电解过程中, 极发生的电极反应为
极发生的电极反应为 和
和 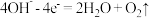 ,若在
,若在 极收集到
极收集到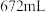 气体,在
气体,在 极收集到
极收集到 气体(均已折算为标准状况时气体体积),则
气体(均已折算为标准状况时气体体积),则 电极(铁电极)质量减少
电极(铁电极)质量减少___________ g。
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池总反应为: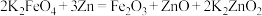 该电池正极的电极反应式为
该电池正极的电极反应式为___________ 。

请回答:Ⅰ.用如图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,能替代Cu做电极的是___________(填字母序号)。
| A.铝 | B.石墨 | C.镁 | D.铂 |
Ⅱ.用如图
 所示装置进行第二组实验。实验过程中,两极均有气体产生,
所示装置进行第二组实验。实验过程中,两极均有气体产生, 极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(
极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(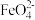 )在溶液中呈紫红色。
)在溶液中呈紫红色。(3)电解过程中,
 极区溶液的
极区溶液的
(4)电解过程中,
 极发生的电极反应为
极发生的电极反应为 和
和 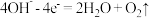 ,若在
,若在 极收集到
极收集到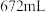 气体,在
气体,在 极收集到
极收集到 气体(均已折算为标准状况时气体体积),则
气体(均已折算为标准状况时气体体积),则 电极(铁电极)质量减少
电极(铁电极)质量减少(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池总反应为:
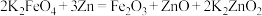 该电池正极的电极反应式为
该电池正极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】一种利用电化学方法同时脱除NO/SO2的工艺如图所示:
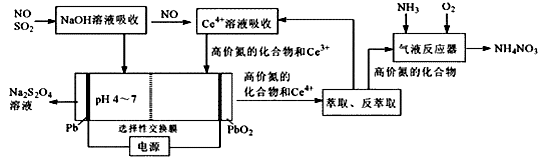
已知SO2水溶液中含硫微粒分布分数(Xi)与pH关系如图所示
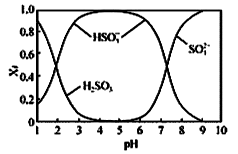
(1)NaOH溶液吸收SO2时,溶液的pH由9→6时,主要发生反应的离子方程式为________ 。
(2)含Ce4+的溶液吸收NO,若高价氮中的NO2、N2O3、NO2-、NO3-各1mol,则消耗0.5mol·L-1的含Ce4+溶液的体积为________ L;其中NO转化NO3-的离子方程式为________ 。
(3)电解槽中,阴极电极反应式主要为________ ,阳极电极反应式为________ 。
(4)在“气液反应器”中高价氮中的N2O3化合为NH4NO3的化学方程式为________ 。

已知SO2水溶液中含硫微粒分布分数(Xi)与pH关系如图所示

(1)NaOH溶液吸收SO2时,溶液的pH由9→6时,主要发生反应的离子方程式为
(2)含Ce4+的溶液吸收NO,若高价氮中的NO2、N2O3、NO2-、NO3-各1mol,则消耗0.5mol·L-1的含Ce4+溶液的体积为
(3)电解槽中,阴极电极反应式主要为
(4)在“气液反应器”中高价氮中的N2O3化合为NH4NO3的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】制备锂离子电池的正极材料的前体 的一种流程如下:
的一种流程如下:

资料:ⅰ.磷灰石的主要成分是
ⅱ. 可溶于水,
可溶于水, 微溶于水
微溶于水
ⅲ.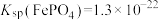
ⅳ.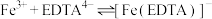
(1)制备
①用 溶液、
溶液、 溶液分步浸取磷灰石生成HF、
溶液分步浸取磷灰石生成HF、 和
和 ,主要反应是
,主要反应是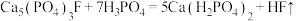 和
和______ 。
②其他条件不变时,若仅用 溶液酸浸,浸取的速率低于用
溶液酸浸,浸取的速率低于用 、
、 分步浸取法,原因是
分步浸取法,原因是______ 。
(2)制备
将 、
、 、
、 混合并调节溶液的pH制备
混合并调节溶液的pH制备 。
。
①酸性条件下,生成 的离子方程式是
的离子方程式是______ 。
②含磷各微粒的物质的量分数与pH的关系如图。
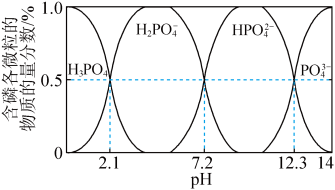
pH=1时,溶液中的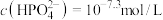 ,则
,则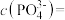
______ mol/L。
再加入 晶体、
晶体、 溶液使溶液中的
溶液使溶液中的 ,不考虑溶液体积的变化,通过计算说明此时能否产生
,不考虑溶液体积的变化,通过计算说明此时能否产生 沉淀
沉淀______ 。
③ 的纯度及颗粒大小会影响其性能,沉淀速率过快容易团聚。
的纯度及颗粒大小会影响其性能,沉淀速率过快容易团聚。
ⅰ.研究表明,沉淀时可加入含 的溶液,
的溶液, 的作用是
的作用是________________________ 。
ⅱ.其他条件不变时,工业上选择pH=2而不是更高的pH制备 ,可能的原因是
,可能的原因是____ (答出2点)。
 的一种流程如下:
的一种流程如下:
资料:ⅰ.磷灰石的主要成分是

ⅱ.
 可溶于水,
可溶于水, 微溶于水
微溶于水ⅲ.
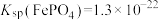
ⅳ.
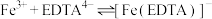
(1)制备

①用
 溶液、
溶液、 溶液分步浸取磷灰石生成HF、
溶液分步浸取磷灰石生成HF、 和
和 ,主要反应是
,主要反应是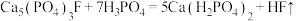 和
和②其他条件不变时,若仅用
 溶液酸浸,浸取的速率低于用
溶液酸浸,浸取的速率低于用 、
、 分步浸取法,原因是
分步浸取法,原因是(2)制备

将
 、
、 、
、 混合并调节溶液的pH制备
混合并调节溶液的pH制备 。
。①酸性条件下,生成
 的离子方程式是
的离子方程式是②含磷各微粒的物质的量分数与pH的关系如图。

pH=1时,溶液中的
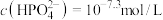 ,则
,则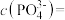
再加入
 晶体、
晶体、 溶液使溶液中的
溶液使溶液中的 ,不考虑溶液体积的变化,通过计算说明此时能否产生
,不考虑溶液体积的变化,通过计算说明此时能否产生 沉淀
沉淀③
 的纯度及颗粒大小会影响其性能,沉淀速率过快容易团聚。
的纯度及颗粒大小会影响其性能,沉淀速率过快容易团聚。ⅰ.研究表明,沉淀时可加入含
 的溶液,
的溶液, 的作用是
的作用是ⅱ.其他条件不变时,工业上选择pH=2而不是更高的pH制备
 ,可能的原因是
,可能的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氮是空气中含量最多的元素,在自然界中存在十分广泛,在生物体内亦有较大作用,是组成氨基酸的基本元素之一。请回答下列问题。
(1)用CO可将汽车尾气中的NO还原为N2,反应为2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH=-akJ·mol-1,K=m。已知:N2(g)+O2(g)
N2(g)+2CO2(g) ΔH=-akJ·mol-1,K=m。已知:N2(g)+O2(g) 2NO(g) ΔH1=+bkJ·mol-1,K1=n,则CO(g)+
2NO(g) ΔH1=+bkJ·mol-1,K1=n,则CO(g)+ O2(g)
O2(g) CO2(g) ΔH2=
CO2(g) ΔH2=____ kJ·mol-1(用含a、b的代数式表示),K2=____ (用含m、n的代数式表示)。
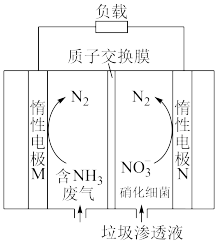
(2)“绿水青山就是金山银山”。现利用如图所示装置对工业废气、垃圾渗透液进行综合治理并实现发电。M极是____ 极,正极的电极反应式为____ 。
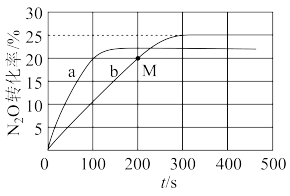
(3)N2O可以被CO还原:N2O(g)+CO(g) N2(g)+CO2(g)。在体积均为1L的恒容密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1molN2O、0.4molCO和相同的催化剂。实验测得A、B中N2O的转化率随时间的变化关系如图所示。A中N2O的转化率随时间的变化关系是图中的b曲线,M点:v正
N2(g)+CO2(g)。在体积均为1L的恒容密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1molN2O、0.4molCO和相同的催化剂。实验测得A、B中N2O的转化率随时间的变化关系如图所示。A中N2O的转化率随时间的变化关系是图中的b曲线,M点:v正____ v逆(填“>”“<”或“=”),A中反应的平衡常数为____ (用分数表示),平衡常数:B____ A(填“大于”“小于”或“等于”)。
(4)实验室中可用NaOH溶液吸收多余的NO2:2NO2+2NaOH=NaNO3+NaNO2+H2O。常温下,用含0.14molNaOH的水溶液吸收NO2,恰好完全反应得1L溶液,测得该溶液的pH=8,则HNO2的电离常数为____ 。
(1)用CO可将汽车尾气中的NO还原为N2,反应为2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH=-akJ·mol-1,K=m。已知:N2(g)+O2(g)
N2(g)+2CO2(g) ΔH=-akJ·mol-1,K=m。已知:N2(g)+O2(g) 2NO(g) ΔH1=+bkJ·mol-1,K1=n,则CO(g)+
2NO(g) ΔH1=+bkJ·mol-1,K1=n,则CO(g)+ O2(g)
O2(g) CO2(g) ΔH2=
CO2(g) ΔH2=(2)“绿水青山就是金山银山”。现利用如图所示装置对工业废气、垃圾渗透液进行综合治理并实现发电。M极是

(3)N2O可以被CO还原:N2O(g)+CO(g)
 N2(g)+CO2(g)。在体积均为1L的恒容密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1molN2O、0.4molCO和相同的催化剂。实验测得A、B中N2O的转化率随时间的变化关系如图所示。A中N2O的转化率随时间的变化关系是图中的b曲线,M点:v正
N2(g)+CO2(g)。在体积均为1L的恒容密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1molN2O、0.4molCO和相同的催化剂。实验测得A、B中N2O的转化率随时间的变化关系如图所示。A中N2O的转化率随时间的变化关系是图中的b曲线,M点:v正
(4)实验室中可用NaOH溶液吸收多余的NO2:2NO2+2NaOH=NaNO3+NaNO2+H2O。常温下,用含0.14molNaOH的水溶液吸收NO2,恰好完全反应得1L溶液,测得该溶液的pH=8,则HNO2的电离常数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】电离平衡常数和电离度(电离度是指已电离的电解质分子数占原来总分子数的百分比)均可衡量弱电解质的电离,下表是常温下几种弱酸的电离平衡常数( )和弱碱的电离平衡常数(
)和弱碱的电离平衡常数( ),回答下列问题∶
),回答下列问题∶
(1) 的水溶液呈
的水溶液呈______ (填“酸性”、“中性”或“碱性”),理由是______ 。
(2)现测得溶解了 的某盐酸的pH=4,则该溶液中
的某盐酸的pH=4,则该溶液中 的电离度约为
的电离度约为______ 。
(3)常温下,浓度相同的三种溶液NaF、 、
、 ,pH由大到小的顺序是
,pH由大到小的顺序是______ 。
(4)将过量 通入
通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为______ 。
 )和弱碱的电离平衡常数(
)和弱碱的电离平衡常数( ),回答下列问题∶
),回答下列问题∶| 弱酸或弱碱 | HF |  |  |  |  |
| 电离平衡常数 | 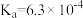 | 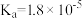 | 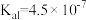 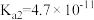 |  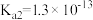 |  |
 的水溶液呈
的水溶液呈(2)现测得溶解了
 的某盐酸的pH=4,则该溶液中
的某盐酸的pH=4,则该溶液中 的电离度约为
的电离度约为(3)常温下,浓度相同的三种溶液NaF、
 、
、 ,pH由大到小的顺序是
,pH由大到小的顺序是(4)将过量
 通入
通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为
您最近一年使用:0次



