以菱镁矿(主要成分为MgCO3,含少量SiO2、Fe2O3和Al2O3)为原料制备高纯镁砂的工艺流程如下:

已知浸出时产生的废渣中有SiO2、 和
和 。下列说法错误的是
。下列说法错误的是

已知浸出时产生的废渣中有SiO2、
 和
和 。下列说法错误的是
。下列说法错误的是| A.流程中可循环使用的物质有NH3、NH4Cl |
| B.浸出和沉镁的操作均不应在较高温度下进行 |
C.浸出镁的离子反应为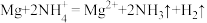 |
D.分离Mg2+与Al3+、Fe3+是利用了它们氢氧化物 的不同 的不同 |
23-24高三上·黑龙江齐齐哈尔·期中 查看更多[2]
更新时间:2023-12-05 11:03:42
|
相似题推荐
【推荐1】工业上利用锌焙砂(主要含ZnO、 ,还含有少量FeO、CuO等)湿法制取金属锌的流程如图所示。下列说法不正确的是
,还含有少量FeO、CuO等)湿法制取金属锌的流程如图所示。下列说法不正确的是

 ,还含有少量FeO、CuO等)湿法制取金属锌的流程如图所示。下列说法不正确的是
,还含有少量FeO、CuO等)湿法制取金属锌的流程如图所示。下列说法不正确的是
| A.酸浸时的硫酸可以用盐酸代替 |
B.加入X的目的是调节溶液的pH,X可以是ZnO或 |
| C.沉淀2的主要成分是ZnS和CuS |
| D.为加快反应速率,净化Ⅰ和Ⅱ均应在较高的温度下进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某混合物可能含有Al、Fe、CuO、 ,为探究该混合物成分,某兴趣小组设计如图分析方案。下列分析错误的是
,为探究该混合物成分,某兴趣小组设计如图分析方案。下列分析错误的是

 ,为探究该混合物成分,某兴趣小组设计如图分析方案。下列分析错误的是
,为探究该混合物成分,某兴趣小组设计如图分析方案。下列分析错误的是
A.已知 ,则混合物中一定含有Al ,则混合物中一定含有Al |
| B.向溶液N中加入足量盐酸可得到无色溶液 |
| C.固体P一定是纯净物 |
D.蓝绿色溶液中含有的阳离子为 、 、 、 、 和 和 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列化学用语对事实的表述不正确 的是
A.由Na和Cl形成离子键的过程: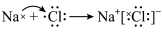 |
| B.Na2S做沉淀剂可处理含Hg2+的工业污水:Hg2++S2-=HgS↓ |
| C.CH3COOH溶液与NaOH溶液反应放出热量H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1 |
| D.闪锌矿(ZnS)经CuSO4溶液作用转化为铜蓝(CuS):ZnS+Cu2+=CuS+Zn2+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用0.100 mol/LAgNO3溶液滴定50.00 mL 0.0500 mol/LNaCl溶液的滴定曲线如图所示,图中c点坐标为(25,4.8)。则下列有关描述错误的是


| A.根据数据计算可知Ksp(AgCl)的数量级为10-10 |
| B.c点之前是AgC1沉淀的生成过程,c点之后是AgCl溶解平衡的移动过程 |
| C.相同实验条件下,若改为0.0500 mol/LNaBr溶液,反应终点c向b方向移动 |
| D.相同实验条件下,若改为0.0400 mol/LNaCl溶液,反应终点c移到a |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验操作中,对应的现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 常温下pH=2的高碘酸(HIO4)溶液与pH=12的NaOH溶液等体积混合 | 所得溶液显酸性 | 高碘酸是弱酸 |
| B | 用pH试纸分别测定等浓度的NaClO和NaHCO3溶液的pH | pH:NaClO>NaHCO3 | 酸性H2CO3>HClO |
| C | 测定0.1mol/LCH3COONa溶液的pH | pH=10 | CH3COOH为强电解质 |
| D | 向2mL1mol·L-1的NaOH溶液中滴加5滴1mol·L-1MgCl2溶液,再滴加5滴1mol·L-1的FeCl3溶液 | 先产生白色沉淀后又产生红褐色沉淀 | 溶度积常数: Mg(OH)2>Fe(OH)3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】某化学兴趣小组利用KBr废液制备溴单质,其流程如图所示(“氧化1”时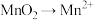 )。下列说法正确的是
)。下列说法正确的是
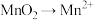 )。下列说法正确的是
)。下列说法正确的是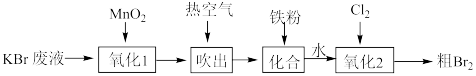
| A.“吹出”时涉及氧化还原反应 |
| B.可用乙醇从溴水中萃取溴 |
C.“氧化1”时若1 mol 发生反应,则转移4 mol电子 发生反应,则转移4 mol电子 |
D.“氧化2”时发生反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在气体分析中,常用 的盐酸溶液吸收并定量测定CO的含量。某工艺通过如图流程制备氯化亚铜固体(已知
的盐酸溶液吸收并定量测定CO的含量。某工艺通过如图流程制备氯化亚铜固体(已知 容易被氧化):
容易被氧化):

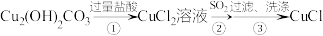
下列说法正确的是
 的盐酸溶液吸收并定量测定CO的含量。某工艺通过如图流程制备氯化亚铜固体(已知
的盐酸溶液吸收并定量测定CO的含量。某工艺通过如图流程制备氯化亚铜固体(已知 容易被氧化):
容易被氧化):
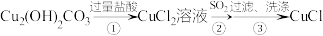
下列说法正确的是
A.步骤①中不可用稀硫酸代替稀盐酸,步骤②中 作为氧化剂 作为氧化剂 |
B.步骤③中用 水溶液洗涤更有效,若洗涤液不含 水溶液洗涤更有效,若洗涤液不含 ,则沉淀已洗净 ,则沉淀已洗净 |
C. 晶胞结构如图所示,每个氯离子周围与之距离最近的氯离子数目为4 晶胞结构如图所示,每个氯离子周围与之距离最近的氯离子数目为4 |
D.若 晶胞的参数为 晶胞的参数为 ,则晶胞的密度 ,则晶胞的密度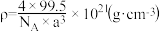 |
您最近一年使用:0次


 是为了使铁溶解生成
是为了使铁溶解生成
 是为了将部分
是为了将部分 是为了防止空气中的
是为了防止空气中的 氧化
氧化 、
、 、极少量
、极少量 等]为原料制取
等]为原料制取 晶体,其部分工艺流程如图:
晶体,其部分工艺流程如图:



