氯及其化合物在生产生活中应用广泛,试回答:
(1)如图是一组探究氯气性质的装置。
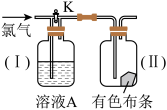
现关闭活塞K,若有色布条是干燥的,溶液A为浓硫酸,则有色布条___________ (填现象,下同)。现打开K,溶液A为氢氧化钠溶液,通入的氯气是湿润的,布条是干燥的,则有色布条___________ 。
(2)下图为氯元素的“价类二维图”的部分信息。请回答下列问题:
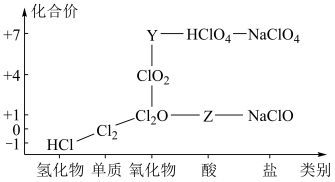
根据图中信息写出Y、Z的化学式:___________ 、___________ 。
(3) 越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
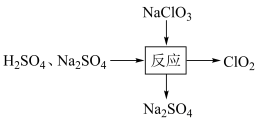
写出该反应的化学方程式并用单线桥表示电子转移的方向和数目:___________ ,该反应的还原剂为___________ 。
(1)如图是一组探究氯气性质的装置。

现关闭活塞K,若有色布条是干燥的,溶液A为浓硫酸,则有色布条
(2)下图为氯元素的“价类二维图”的部分信息。请回答下列问题:

根据图中信息写出Y、Z的化学式:
(3)
 越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
越来越多地取代以次氯酸盐为有效成分的漂白剂和消毒剂。其制取方法有多种,如图是其中的一种制取方法:
写出该反应的化学方程式并用单线桥表示电子转移的方向和数目:
更新时间:2023-12-30 21:04:02
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】用双线桥表示下列反应的电子转移情况:
(1)Fe2O3 + 3CO=2Fe + 3CO2_______
(2)2KMnO4+16HCl=2MnCl2 + 2KCl+5Cl2↑+8H2O_______
(1)Fe2O3 + 3CO=2Fe + 3CO2
(2)2KMnO4+16HCl=2MnCl2 + 2KCl+5Cl2↑+8H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(Ⅰ)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2.
已知该反应中H2O2只发生如下过程:H2O2―→O2.
①该反应中的还原剂是____________ .
②该反应中,发生还原反应的过程是____________ →____________ .
③写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目_______
④如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为____________
(Ⅱ)已知实验室利用KMnO4溶液和浓盐酸反应制取Cl2,请回答下列问题:
①配平此化学方程式:
____ KMnO4+____ HCl(浓)— ____ KCl+____ MnCl2+____ Cl2↑+____ H2O
②把此化学方程式改写成离子方程式:________
③被氧化的HCl 与未被氧化的HCl物质的量之比为____________
已知该反应中H2O2只发生如下过程:H2O2―→O2.
①该反应中的还原剂是
②该反应中,发生还原反应的过程是
③写出该反应的化学方程式,并用单线桥标出电子转移的方向和数目
④如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为
(Ⅱ)已知实验室利用KMnO4溶液和浓盐酸反应制取Cl2,请回答下列问题:
①配平此化学方程式:
②把此化学方程式改写成离子方程式:
③被氧化的HCl 与未被氧化的HCl物质的量之比为
您最近一年使用:0次
【推荐3】工业废水中含有的重铬酸根( )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++ +14H+=6Fe3++2Cr3++7H2O,回答下列问题:
+14H+=6Fe3++2Cr3++7H2O,回答下列问题:
(1)氧化性:
___________ Fe3+(填“>”或“<”)。
(2)用“单线桥”标出电子转移的方向和数目___________
6Fe2++ +14H+=6Fe3++2Cr3++7H2O。
+14H+=6Fe3++2Cr3++7H2O。
(3)每处理含0.5 mol 的废水,需消耗绿矾
的废水,需消耗绿矾___________ g (已知:FeSO4·7H2O的摩尔质量为278 g/mol)。
 )有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++
)有毒,必须处理达标后才能排放。工业上常用绿矾(FeSO4·7H2O)做处理剂,反应的离子方程式如下:6Fe2++ +14H+=6Fe3++2Cr3++7H2O,回答下列问题:
+14H+=6Fe3++2Cr3++7H2O,回答下列问题:(1)氧化性:

(2)用“单线桥”标出电子转移的方向和数目
6Fe2++
 +14H+=6Fe3++2Cr3++7H2O。
+14H+=6Fe3++2Cr3++7H2O。(3)每处理含0.5 mol
 的废水,需消耗绿矾
的废水,需消耗绿矾
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某漂粉精说明书如下:
(1)从主要成分看,可知生产漂粉精的原料是氯气和石灰乳,请写出制漂粉精的化学方程式:_______ ,漂粉精中有效成分为_______ 。
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:_______ ,并进一步写出制备“84消毒液”的化学方程式_______ 。
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?_______ 。
| 使用说明书 主要成分:次氯酸钙、氯化钙 用途用量:取漂粉精2-3克,水100克,配成溶液,将禽流感病人用具浸泡其中5-10分钟,如需要可延长时间,提高浓度。 注意事项:密封保存于阴凉处,随配随用,有腐蚀性,少与手接触。 |
(2)生活中常有的漂白剂还有“84消毒液”,制备“84消毒液”的反应物是通过氯碱工业制得,请写出电解饱和食盐水的化学方程式:
(3)为什么家庭中的漂白剂使用漂粉精,而不使用氯水?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图为氯及其化合物的“价—类”二维图。
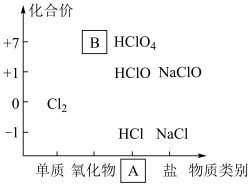
(1)缺失的类别 为
为___________ 、物质 为
为___________ (填化学式)。
(2) 在
在 中安静燃烧
中安静燃烧_______________________________ (化学方程式)。
(3) 溶于水
溶于水____________________________ (离子方程式)。
(4)工业制备漂白粉__________________________________ (化学方程式)。

(1)缺失的类别
 为
为 为
为(2)
 在
在 中安静燃烧
中安静燃烧(3)
 溶于水
溶于水(4)工业制备漂白粉
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,图为氯元素的“价类二维图”的部分信息。请回答下列问题:
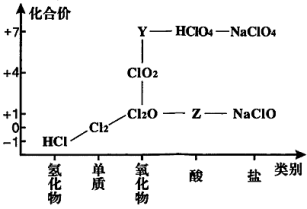
(1)根据图中信息写出Y、Z的化学式_______ 、_______ 。
(2)已知高氯酸(HClO4)是强酸,写出高氯酸与氢氧化钠反应的离子方程式_______ 。
(3)氯气既有氧化性又有还原性,结合图示说明理由_______ 
(4)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式_______ ,该反应中盐酸表现_______ (填字母)。
A.酸性 B.氧化性 C.还原性
(5)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为NaClO+2HCl═NaCl+Cl2↑+H2O,下列有关该反应说法不正确 的是_______ 。
A.n(氧化剂)∶n(还原剂)=1∶1 B.n(氧化剂)∶n(还原剂)=1∶2
C.氧化性:NaClO>Cl2 D.Cl2既是氧化产物又是还原产物
(6)某游泳池常用来NaClO抑制藻类生长,工作人员一次错用H2O2消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了O2和NaCl,写出相应的化学方程式_______ 。

(1)根据图中信息写出Y、Z的化学式
(2)已知高氯酸(HClO4)是强酸,写出高氯酸与氢氧化钠反应的离子方程式
(3)氯气既有氧化性又有还原性,结合图示说明理由

(4)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式
A.酸性 B.氧化性 C.还原性
(5)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为NaClO+2HCl═NaCl+Cl2↑+H2O,下列有关该反应说法
A.n(氧化剂)∶n(还原剂)=1∶1 B.n(氧化剂)∶n(还原剂)=1∶2
C.氧化性:NaClO>Cl2 D.Cl2既是氧化产物又是还原产物
(6)某游泳池常用来NaClO抑制藻类生长,工作人员一次错用H2O2消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了O2和NaCl,写出相应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。

回答下列问题:
(1)X在水中的电离方程式为_______ 。
(2)Y可用于实验室制O2,其焰色试验为紫色,则Y的化学式为_______ ;Y在400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种是含氧酸盐,则生成这两种盐的物质的量之比是_______ 。
(3)NaClO2具有很强的氧化性,常用作消毒剂,其消毒效率是Z的_______ 倍(还原产物都为Cl-,消毒效率以单位物质的量得到的电子数表示)。
(4)Cl2O熔点-116℃,沸点2℃,容易与水反应生成次氯酸,与空气混合容易爆炸。Cl2O可用潮湿的Z与Na2CO3反应制取,同时生成NaHCO3,反应中Z既体现氧化性,又体现还原性,该反应的化学方程式为________ ,适宜的收集方法是_______ 。

回答下列问题:
(1)X在水中的电离方程式为
(2)Y可用于实验室制O2,其焰色试验为紫色,则Y的化学式为
(3)NaClO2具有很强的氧化性,常用作消毒剂,其消毒效率是Z的
(4)Cl2O熔点-116℃,沸点2℃,容易与水反应生成次氯酸,与空气混合容易爆炸。Cl2O可用潮湿的Z与Na2CO3反应制取,同时生成NaHCO3,反应中Z既体现氧化性,又体现还原性,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】水是生命之源,水在工业、农业和日常生活中均发挥着重要作用。
(1)下列关于水的说法,正确的是_________。
(2)为增强水的导电性,通常向纯水中加入适量的NaOH(NaOH不参加反应)。
①某电解水实验开始时,向180g纯水中溶解了4gNaOH。此时溶液中Na+和水分子的个数比是___________ 。
②当实验进行到一段时间,两个石墨电极共收集到的气体质量为3.6g。计算此时被电解的水的物质的量是____________ 。
(3)目前,很多自来水厂用氯气杀菌、消毒。仔细观察下图的微观反应过程,写出该化学反应方程式___________ 。
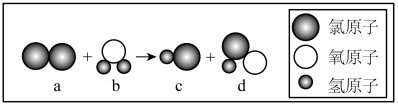
(1)下列关于水的说法,正确的是_________。
| A.2mol水的摩尔质量是36g/mol | B.18g水中含有10个电子 |
| C.1mol水中含2mol氢 | D.一个水分子的质量约是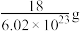 |
①某电解水实验开始时,向180g纯水中溶解了4gNaOH。此时溶液中Na+和水分子的个数比是
②当实验进行到一段时间,两个石墨电极共收集到的气体质量为3.6g。计算此时被电解的水的物质的量是
(3)目前,很多自来水厂用氯气杀菌、消毒。仔细观察下图的微观反应过程,写出该化学反应方程式

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图是依据一定的分类标准,对某些物质与水反应情况进行分类的分类图。请根据你所学的知识,按要求填空:

(1)根据物质与水反应的情况,分成A、B组的分类依据是___ 。
(2)A组中的CaO常用作食品包装袋中的干燥剂,CaO所属类别为___ (填序号)。
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
(3)D组中的气体水溶液呈弱碱性,用电离方程式表示其水溶液呈弱碱性的原因:__ 。
(4)F组中与水反应,氧化剂与还原剂的数量之比为1∶1的物质是__ 。(填化学式)。
(5)写出水既做氧化剂又做还原剂的化学方程式___ 。

(1)根据物质与水反应的情况,分成A、B组的分类依据是
(2)A组中的CaO常用作食品包装袋中的干燥剂,CaO所属类别为
①金属氧化物 ②酸性氧化物 ③碱性氧化物 ④两性氧化物
(3)D组中的气体水溶液呈弱碱性,用电离方程式表示其水溶液呈弱碱性的原因:
(4)F组中与水反应,氧化剂与还原剂的数量之比为1∶1的物质是
(5)写出水既做氧化剂又做还原剂的化学方程式
您最近一年使用:0次



