NaCl是一种化工原料,可以制备多种物质,如下图所示。

请根据以上转化关系填写下列空白。
(1)写出反应①的离子方程式:___________ ,该反应中氧化产物与还原产物的质量比为___________ 。
(2)反应②可用于制取漂白粉,写出化学反应方程式并用双线桥法标出电子转移的方向和数目:___________ ;漂白粉需要密封保存,其原因是___________ (用化学方程式表示)
(3)反应③是侯氏制碱法的核心反应,写出化学反应方程式:___________ ;侯氏制碱法将___________ 和___________ 联合起来,也称联合制碱法。

请根据以上转化关系填写下列空白。
(1)写出反应①的离子方程式:
(2)反应②可用于制取漂白粉,写出化学反应方程式并用双线桥法标出电子转移的方向和数目:
(3)反应③是侯氏制碱法的核心反应,写出化学反应方程式:
更新时间:2024-01-01 08:30:19
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】为有效控制汽车尾气造成的空气污染,目前,汽车尾气系统中均安装了催化转化器。在催化转化器中,汽车尾气中的 和
和 在催化剂作用下发生反应,生成可参与大气循环的无毒气体。
在催化剂作用下发生反应,生成可参与大气循环的无毒气体。
(1)该反应的化学方程式为___________________________ ,其中氧化剂是__________________ (填化学式,下同),氧化产物是_________ 。
(2)上述反应中,若处理 ,则消耗
,则消耗 的体积为
的体积为_________  (标准状况)。
(标准状况)。
(3)下列措施有利于控制城市空气污染的是_________(填序号)。
(4)利用 催化还原氮氧化物(
催化还原氮氧化物( 技术)是目前应用广泛的脱硝技术,
技术)是目前应用广泛的脱硝技术, 技术涉及的主要反应是:
技术涉及的主要反应是:
①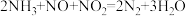
②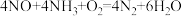
若反应①中消耗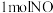 ,则转移电子的物质的量为
,则转移电子的物质的量为_________  ,反应②中
,反应②中 被
被_________ (填“氧化”或“还原”),若反应①和反应②中所得 物质的量相等,则两个反应转移的电子数之比为
物质的量相等,则两个反应转移的电子数之比为_________ 。
 和
和 在催化剂作用下发生反应,生成可参与大气循环的无毒气体。
在催化剂作用下发生反应,生成可参与大气循环的无毒气体。(1)该反应的化学方程式为
(2)上述反应中,若处理
 ,则消耗
,则消耗 的体积为
的体积为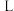 (标准状况)。
(标准状况)。(3)下列措施有利于控制城市空气污染的是_________(填序号)。
| A.推广电动汽车 | B.开发和使用氢能 | C.加快煤炭开采和使用 |
 催化还原氮氧化物(
催化还原氮氧化物( 技术)是目前应用广泛的脱硝技术,
技术)是目前应用广泛的脱硝技术, 技术涉及的主要反应是:
技术涉及的主要反应是:①
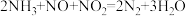
②
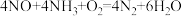
若反应①中消耗
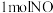 ,则转移电子的物质的量为
,则转移电子的物质的量为 ,反应②中
,反应②中 被
被 物质的量相等,则两个反应转移的电子数之比为
物质的量相等,则两个反应转移的电子数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:
____ Na2SO3+____ KIO3+____ H2SO4===____ Na2SO4+____ K2SO4+____ I2+____ H2O
(1)配平上面的氧化还原方程式。
(2)若反应中有5 mol电子转移,则生成的碘单质是________ mol。
(1)配平上面的氧化还原方程式。
(2)若反应中有5 mol电子转移,则生成的碘单质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】2012年10月29日,超强飓风“桑迪”登陆美国东海岸,给人们的生命财产造成巨大损失。灾区人们的饮水必须用漂白粉等药品消毒后才能饮用,以防止传染病发生。
(1)试用化学方程式表示工业制取漂白粉的过程______________________________ ;
(2)已知浓盐酸和漂白粉中的成分之一次氯酸钙能发生如下反应:
Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质气体是( )
① CO2 ② HCl ③ H2O ④ O2
A.①②③ B.②③④ C.②③ D.①④
(3)若用KMnO4氧化盐酸。其反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
该反应中,氧化剂是____ ,1 mol氧化剂在反应中_______ (填“得到”或“失去”)______ mol电子。当有1mol KMnO4恰好和盐酸全部完全反应,反应后溶液的体积为2L,则所得溶液中Cl—的物质的量浓度为_______ ,此时产生的Cl 2在标准状况下的体积为_______ ,被氧化的HCl的物质的量为________ 。
(1)试用化学方程式表示工业制取漂白粉的过程
(2)已知浓盐酸和漂白粉中的成分之一次氯酸钙能发生如下反应:
Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质气体是
① CO2 ② HCl ③ H2O ④ O2
A.①②③ B.②③④ C.②③ D.①④
(3)若用KMnO4氧化盐酸。其反应方程式如下:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
该反应中,氧化剂是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题
(1)消毒液中的有效成分是_______ ,制备 消毒液的反应的化学方程式为
消毒液的反应的化学方程式为_______ 。它的消毒原理是_______ (用化学方程式表示)。由以上反应证明 是弱酸,酸性比碳酸
是弱酸,酸性比碳酸_______ 。
(2)将 和
和 的混合物加入足量的水中充分反应后,生成标准状况下的气体
的混合物加入足量的水中充分反应后,生成标准状况下的气体 ,所得溶液的体积为
,所得溶液的体积为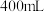 。试计算:
。试计算:
①原混合物中 的质量为
的质量为_______  。
。
②所得溶液的物质的量浓度为_______  。
。
(1)消毒液中的有效成分是
 消毒液的反应的化学方程式为
消毒液的反应的化学方程式为 是弱酸,酸性比碳酸
是弱酸,酸性比碳酸(2)将
 和
和 的混合物加入足量的水中充分反应后,生成标准状况下的气体
的混合物加入足量的水中充分反应后,生成标准状况下的气体 ,所得溶液的体积为
,所得溶液的体积为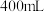 。试计算:
。试计算:①原混合物中
 的质量为
的质量为 。
。②所得溶液的物质的量浓度为
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】我们生活中处处都与化学有密切关系。
(1)洪灾过后,饮用水可用漂白粉消毒。工业上将氯气通入石灰乳 [Ca(OH)2]中制取漂白粉,反应的化学方程式为____________ 。
(2)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要化合物。电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式__________________ ;如何检验FeCl3腐蚀铜后的溶液是否含Fe3+__________ 。
(3)在用二氧化氯进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+生成ClO2-和MnO2的离子方程式为___________ 。
(1)洪灾过后,饮用水可用漂白粉消毒。工业上将氯气通入石灰乳 [Ca(OH)2]中制取漂白粉,反应的化学方程式为
(2)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸盐为重要化合物。电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。请写出FeCl3溶液与铜反应的离子方程式
(3)在用二氧化氯进行水处理时,ClO2除了杀菌消毒外,还能除去水中的Fe2+和Mn2+。用ClO2氧化除去Mn2+生成ClO2-和MnO2的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性。其中含氯消毒剂在生产生活中有着广泛的用途。
(1)①写出实验室中制取氯气的化学方程式_______ ;实验室用排_______ 的方法除去混在氯气的氯化氢杂质,用_______ 除去混在里面的水蒸气;
②写出次氯酸分解的化学反应方程式_______ ;新制氯水中含有的分子为_______ ;新制氯水含有多种离子,除OH-外,还有_______ ;
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO 是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。
①用离子方程式表示“84”消毒液的制备:_______ ;
②某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与ClO 的离子个数比为1∶3,请配平该反应的:
的离子个数比为1∶3,请配平该反应的:___ 。_______Cl2+ _______OH- = _______Cl-+1ClO-+3ClO +____H2O;
+____H2O;
(1)①写出实验室中制取氯气的化学方程式
②写出次氯酸分解的化学反应方程式
(2)常温下,氯气与烧碱溶液反应得“84”消毒液,NaClO 是“84”消毒液的有效成分,在此次抗击新冠病毒中发挥了重要作用。
①用离子方程式表示“84”消毒液的制备:
②某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与ClO
 的离子个数比为1∶3,请配平该反应的:
的离子个数比为1∶3,请配平该反应的: +____H2O;
+____H2O;
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】短周期主族元素A、B、C、D、E,F在元素周期表中的位置如图所示。试回答下列问题:
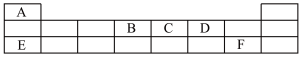
(l)E的某种氧化物可以做制氧剂,请书写所涉及的化学反应方程式:__ 、___ 。
(2)F在周期表中的位置为__ ,其下一周期元素的原子结构示意图为__ ,写出其单质与EDA溶液反应的离子方程式__ 。
(3)写出化合物EABD3在水溶液中的电离方程式__ ,其溶液可与足量的澄清石灰水反应,则反应的离子方程式为__ 。

(l)E的某种氧化物可以做制氧剂,请书写所涉及的化学反应方程式:
(2)F在周期表中的位置为
(3)写出化合物EABD3在水溶液中的电离方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入足量的氯气,二者恰好完全反应。生成Cl-、ClO-、ClO3-三种含氯元素的离子,其中ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示。
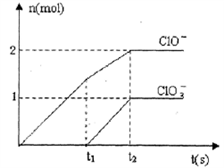
(1)t1时,开始有ClO3-生成的原因是___________________________ 。
(2)t2时,Ca(OH)2与Cl2发生反应的总的化学方程式为___________________________ 。
(3)该石灰乳中含有Ca(OH)2的物质的量是_________ mol。

(1)t1时,开始有ClO3-生成的原因是
(2)t2时,Ca(OH)2与Cl2发生反应的总的化学方程式为
(3)该石灰乳中含有Ca(OH)2的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】超酸是一类比纯硫酸更强的酸,在石油重整中用作高效催化剂。某实验小组对超酸HSbF6的制备及性质进行了探究。由三氯化锑(SbCl3)制备HSbF6的反应如下: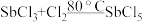 、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
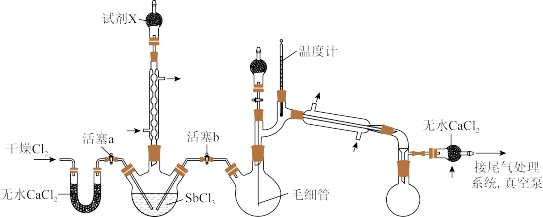
相关性质如表:
回答下列问题:
(1)实验小组在由SbCl5制备HSbF6时,没有选择玻璃仪器,其原因为_______ (写化学反应方程式)。
(2)为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为_______ 。
(3)实验小组在探究实验中发现蜡烛可以溶解于HSbF6中,同时放出氢气。已知烷烃分子中碳氢键的活性大小顺序为:甲基(—CH3)<亚甲基(—CH2—)<次甲基(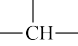 )。写出2-甲基丙烷与HSbF6反应的离子方程式
)。写出2-甲基丙烷与HSbF6反应的离子方程式_______ 。
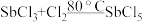 、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
、SbCl5+6HF=HSbF6+5HCl。制备SbCl5的初始实验装置如图(毛细管连通大气,减压时可吸入极少量空气,防止液体暴沸;夹持、加热及搅拌装置略):
相关性质如表:
| 物质 | 熔点 | 沸点 | 性质 |
| SbCl3 | 73.4℃ | 220.3℃ | 极易水解 |
| SbCl5 | 3.5℃ | 140℃分解79℃/2.9kPa | 极易水解 |
回答下列问题:
(1)实验小组在由SbCl5制备HSbF6时,没有选择玻璃仪器,其原因为
(2)为更好地理解超酸的强酸性,实验小组查阅相关资料了解到:弱酸在强酸性溶剂中表现出碱的性质,如冰醋酸与纯硫酸之间的化学反应方程式为CH3COOH+H2SO4=[CH3C(OH)2]+[HSO4]-。以此类推,H2SO4与HSbF6之间的化学反应方程式为
(3)实验小组在探究实验中发现蜡烛可以溶解于HSbF6中,同时放出氢气。已知烷烃分子中碳氢键的活性大小顺序为:甲基(—CH3)<亚甲基(—CH2—)<次甲基(
 )。写出2-甲基丙烷与HSbF6反应的离子方程式
)。写出2-甲基丙烷与HSbF6反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】工业上利用电解饱和食盐水可制得重要化工产品。
(1)反应化学方程式为:___ 。
(2)电解饱和食盐水时,___ 极区附近溶液pH变大。
(3)取阴极区溶液作系列实验,下列结论中错误的是___ 。(填字母)
A.滴加石蕊试剂,溶液呈红色
B.滴加氯化镁溶液,有白色沉淀产生
C.加入石灰石,有气泡产生
D.先加足量硝酸,再滴加硝酸银溶液,若产生沉淀说明溶液中含有氯离子
(4)电解饱和食盐水一段时间后,想要让溶液恢复电解前的状态,应往溶液中加入(或通入)一定量的___ (填字母)。
A.NaCl固体 B.NaCl溶液 C.HCl气体 D.盐酸
(1)反应化学方程式为:
(2)电解饱和食盐水时,
(3)取阴极区溶液作系列实验,下列结论中错误的是
A.滴加石蕊试剂,溶液呈红色
B.滴加氯化镁溶液,有白色沉淀产生
C.加入石灰石,有气泡产生
D.先加足量硝酸,再滴加硝酸银溶液,若产生沉淀说明溶液中含有氯离子
(4)电解饱和食盐水一段时间后,想要让溶液恢复电解前的状态,应往溶液中加入(或通入)一定量的
A.NaCl固体 B.NaCl溶液 C.HCl气体 D.盐酸
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氯及其合氯化合物
人体中钠的主要来源为食盐、酱油、腌制食品、烟熏食品、咸味食品等。氧化钠,也称苛性钠、烧藏、火马、是一种无机化合物,化学式为NaOH,用途非常广泛。烧碱是一种重要的化工原料,工业烧碱中可能含有少量NaCl。
(1)海水晒盐的原理是_____。
(2)电解饱和的食盐水,先要精制盐水,以除去 、Ca2+,可依次加入的溶液是_____。
、Ca2+,可依次加入的溶液是_____。
(3)电解饱和食盐水溶液,下列叙述中,正确的是_____。
(4)下列氯化物中,可以由金属和氯气反应得到的是_____。
(5)下列关于氯气和氯水的叙述正确的是_____。
(6)电解饱和食盐水的化学方程式:_____ 。
(7)工业上用_____ 和_____ (写化学式)作为原料来制取漂粉精,反应的化学方程式为_____ ,漂粉精长期在空气中,会使其失效,主要化学方程式_____ ;_____ ,故其应_____ 保存。
人体中钠的主要来源为食盐、酱油、腌制食品、烟熏食品、咸味食品等。氧化钠,也称苛性钠、烧藏、火马、是一种无机化合物,化学式为NaOH,用途非常广泛。烧碱是一种重要的化工原料,工业烧碱中可能含有少量NaCl。
(1)海水晒盐的原理是_____。
| A.利用热蒸发浓缩海水达到饱和并进一步结晶 |
| B.用过降温降低食盐的溶解度使食盐析出 |
| C.利用加入沉淀剂的方法使食盐沉淀析出 |
| D.利用泥沙使海水到达饱和,然后利用日光使海盐析出 |
 、Ca2+,可依次加入的溶液是_____。
、Ca2+,可依次加入的溶液是_____。| A.Na2CO3、BaCl2、NaOH、HCl |
| B.BaCl2、NaOH、Na2CO3、HCl |
| C.BaCl2、Na2CO3、HCl、NaOH |
| D.Na2CO3、BaCl2、HCl、NaOH |
| A.电解时在阳极得到氯气,在阴极得到金属钠 |
| B.在阳极附近的溶液中滴入淀粉碘化钾溶液,溶液呈蓝色 |
| C.若在阴极收集气体,能使带火星的木条燃。 |
| D.在阴极的物质只有氢气 |
| A.CuCl | B.FeCl2 | C.FeCl3 | D.HCl |
| A.因氯气有强氧化性,所以氯气本身可用于杀菌、消毒、漂白 |
| B.氯水中起漂白用的是次氯酸 |
| C.氯水长期放置颜色无明显变化 |
| D.光照水有气泡冒出,该气体是氯气 |
(7)工业上用
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在下图所示的物质转化关系中,A是海水中含量最丰富的盐,B是常见的无色液体,G的水溶液是一种常用的漂白剂,F是地壳中含量最多的金属元素。(反应中生成的水和部分反应条件未列出)

(1)画出A中阴离子的结构示意图_________ 。
(2)反应②在点燃条件下的现象是_________ 。
(3)H转化为F的氢氧化物最好选择的试剂是_________ 。
(4)反应③的离子方程式为_________ 。
(5)反应④的离子方程式为_________ 。

(1)画出A中阴离子的结构示意图
(2)反应②在点燃条件下的现象是
(3)H转化为F的氢氧化物最好选择的试剂是
(4)反应③的离子方程式为
(5)反应④的离子方程式为
您最近一年使用:0次



