钠及其化合物在生活和生产中有重要用途。
(1) 因外观和食盐相似,有咸味,容易使人误食中毒。已知
因外观和食盐相似,有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: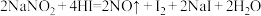 。请回答:
。请回答:
①上述反应中,氧化产物是___________ (填化学式),其中HI在反应中体现出的性质为___________ (填字母)。
A.酸性 B.氧化性 C.碱性 D.还原性
②某厂废液中含有3%~6%的 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是
的是___________ (填字母)。
A.NaClO B. C.
C. D.
D.
(2) 是实验室常用的试剂,也常作呼吸面具和潜水艇里的供氧剂。
是实验室常用的试剂,也常作呼吸面具和潜水艇里的供氧剂。
①写出 与
与 反应的化学方程式
反应的化学方程式___________ 。
②将二氧化碳和水蒸气组成的混合气体8.0g通过足量的 粉末,完全吸收后固体质量增重3.2g,则该混合气体中水蒸气的质量为
粉末,完全吸收后固体质量增重3.2g,则该混合气体中水蒸气的质量为___________ 。
③将一定量的 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,完全反应后,溶液中上述离子数目几乎不变的是
,完全反应后,溶液中上述离子数目几乎不变的是___________ (填离子符号)。
(3) 是实验室中常用的物质。侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。
是实验室中常用的物质。侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。
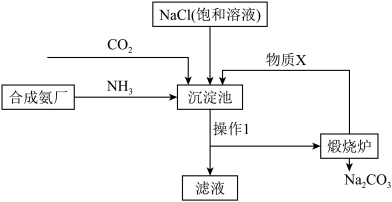
①上述流程中,物质X是___________ (填化学式)。
②写出沉淀池的化学反应方程式___________ 。
③下列关于侯德榜“联合制碱法”说法错误的是___________ (填字母)。
A.上述流程中滤液中可分离得到一种氮肥
B.上述流程应在饱和NaCl溶液中先通 ,再通
,再通
C.沉淀池中析出晶体利用了相同条件下物质溶解度的差异
D.该工艺的碳原子利用率理论上为100%
(1)
 因外观和食盐相似,有咸味,容易使人误食中毒。已知
因外观和食盐相似,有咸味,容易使人误食中毒。已知 能发生如下反应:
能发生如下反应: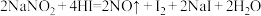 。请回答:
。请回答:①上述反应中,氧化产物是
A.酸性 B.氧化性 C.碱性 D.还原性
②某厂废液中含有3%~6%的
 ,直接排放会造成污染,下列试剂能使
,直接排放会造成污染,下列试剂能使 转化为不引起二次污染的
转化为不引起二次污染的 的是
的是A.NaClO B.
 C.
C. D.
D.
(2)
 是实验室常用的试剂,也常作呼吸面具和潜水艇里的供氧剂。
是实验室常用的试剂,也常作呼吸面具和潜水艇里的供氧剂。①写出
 与
与 反应的化学方程式
反应的化学方程式②将二氧化碳和水蒸气组成的混合气体8.0g通过足量的
 粉末,完全吸收后固体质量增重3.2g,则该混合气体中水蒸气的质量为
粉末,完全吸收后固体质量增重3.2g,则该混合气体中水蒸气的质量为③将一定量的
 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,完全反应后,溶液中上述离子数目几乎不变的是
,完全反应后,溶液中上述离子数目几乎不变的是(3)
 是实验室中常用的物质。侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。
是实验室中常用的物质。侯德榜“联合制碱法”将制碱技术发展到一个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。
①上述流程中,物质X是
②写出沉淀池的化学反应方程式
③下列关于侯德榜“联合制碱法”说法错误的是
A.上述流程中滤液中可分离得到一种氮肥
B.上述流程应在饱和NaCl溶液中先通
 ,再通
,再通
C.沉淀池中析出晶体利用了相同条件下物质溶解度的差异
D.该工艺的碳原子利用率理论上为100%
更新时间:2024-01-11 21:20:52
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】工业烟道气中含有的二氧化硫和氮氧化物是大气主要污染物,脱硫脱氮是环境治理的热点问题。回答下列问题:
(1)配平利用KMnO4脱除二氧化硫的离子方程式:_______ 。
□ +□SO2+□H2O⇌□
+□SO2+□H2O⇌□ +□_______+□_______
+□_______+□_______
加入CaCO3可以提高SO2去除率,原因是_______ 。
(2)CaSO3与Na2SO4混合浆液可用于脱除NO2,反应过程为:
I.CaSO3(s)+ (aq)⇌CaSO4(s)+
(aq)⇌CaSO4(s)+ (aq)
(aq)
II. (aq)+2NO2(g)+H2O(l)⇌
(aq)+2NO2(g)+H2O(l)⇌ (aq)+2
(aq)+2 (aq)+2H+(aq)
(aq)+2H+(aq)
浆液中CaSO3质量一定时,Na2SO4的质量与NO2的去除率变化趋势如图所示。
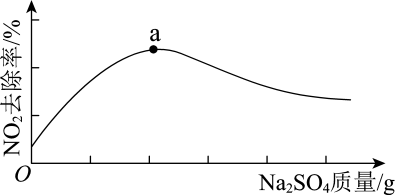
a点后NO2去除率降低的原因是_______ 。
(1)配平利用KMnO4脱除二氧化硫的离子方程式:
□
 +□SO2+□H2O⇌□
+□SO2+□H2O⇌□ +□_______+□_______
+□_______+□_______加入CaCO3可以提高SO2去除率,原因是
(2)CaSO3与Na2SO4混合浆液可用于脱除NO2,反应过程为:
I.CaSO3(s)+
 (aq)⇌CaSO4(s)+
(aq)⇌CaSO4(s)+ (aq)
(aq)II.
 (aq)+2NO2(g)+H2O(l)⇌
(aq)+2NO2(g)+H2O(l)⇌ (aq)+2
(aq)+2 (aq)+2H+(aq)
(aq)+2H+(aq)浆液中CaSO3质量一定时,Na2SO4的质量与NO2的去除率变化趋势如图所示。

a点后NO2去除率降低的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】干电池是日常生活中常用的电池,原料为Zn和MnO2。某工厂用软锰矿(含MnO2约70%及杂质Al2O3)和闪锌矿(含ZnS约80%及少量FeS杂质)共同生产。流程如下:

已知:①A是ZnSO4、MnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。
②Ⅳ中反应的方程式为:MnSO4+ZnSO4+2H2O MnO2+Zn+2H2SO4。
MnO2+Zn+2H2SO4。
(1)混合物A中,属于还原产物的是______ (填化学式)。
(2)加入X的作用是_____________________ 。已知溶液中各离子开始沉淀的pH如表所示,则加入X后,溶液pH应调整到_____ (填字母)。
A.4.5 B.8.0 C.6.5 D.9.0
步骤Ⅱ加热的原因是____________________ 。适宜作为X加入步骤Ⅱ的物质为______ (填字母)。
A.MnCO3 B.Zn2(OH)2CO3 C.NaOH D.KOH
(3)生产过程中除矿石外,还有哪些原料需要购买?____________ (填化学式)。
(4)若要从步骤Ⅳ的过滤中得到芒硝晶体(Na2SO4·10H2O),则需要进行的实验操作有________ 、________ 、过滤、洗涤、干燥等。

已知:①A是ZnSO4、MnSO4、Fe2(SO4)3、Al2(SO4)3的混合液。
②Ⅳ中反应的方程式为:MnSO4+ZnSO4+2H2O
 MnO2+Zn+2H2SO4。
MnO2+Zn+2H2SO4。(1)混合物A中,属于还原产物的是
(2)加入X的作用是
A.4.5 B.8.0 C.6.5 D.9.0
| 离子 | 开始沉淀pH | 完全沉淀pH |
| Fe3+ | 2.3 | 3.2 |
| Al3+ | 4.2 | 5.4 |
| Zn2+ | 7.2 | 8.0 |
| Mn2+ | 8.3 | 9.8 |
步骤Ⅱ加热的原因是
A.MnCO3 B.Zn2(OH)2CO3 C.NaOH D.KOH
(3)生产过程中除矿石外,还有哪些原料需要购买?
(4)若要从步骤Ⅳ的过滤中得到芒硝晶体(Na2SO4·10H2O),则需要进行的实验操作有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】实验探究 、
、 的性质。
的性质。
已知: 可与
可与 溶液反应生成蓝色沉淀。
溶液反应生成蓝色沉淀。
(1)分别取一定量硫酸铁、氯化亚铁固体,均配制成 溶液。配制
溶液。配制 溶液时需加入少量铁屑,目的是
溶液时需加入少量铁屑,目的是_______ 。
(2)甲组同学取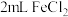 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为_______ 。
(3)乙组同学认为甲组实验不够严谨,该组同学用煮沸冷却后的水配制溶液,向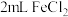 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是_____ 。
(4)丙组同学取 溶液,加入足量
溶液,加入足量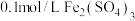 溶液混合后,滴加淀粉溶液,出现蓝色,该现象说明氧化性:
溶液混合后,滴加淀粉溶液,出现蓝色,该现象说明氧化性:
_______  (填“>”或“<”);另取
(填“>”或“<”);另取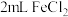 溶液,加入几小块锌片,实验现象为
溶液,加入几小块锌片,实验现象为_______ ,说明 具有
具有_______ 。(填“氧化性”或“还原性”)。
(5)丁组同学为探究维生素C是否可将 转化为
转化为 ,设计了如下实验。
,设计了如下实验。
其他组同学认为:根据该实验现象不能得出“维生素C可将 转化为
转化为 ”的结论,原因是
”的结论,原因是_______ ;认为可另外设计实验验证结论是否正确:取a溶液少许,滴加_______ ,若出现_______ ,则结论正确。
 、
、 的性质。
的性质。已知:
 可与
可与 溶液反应生成蓝色沉淀。
溶液反应生成蓝色沉淀。(1)分别取一定量硫酸铁、氯化亚铁固体,均配制成
 溶液。配制
溶液。配制 溶液时需加入少量铁屑,目的是
溶液时需加入少量铁屑,目的是(2)甲组同学取
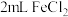 溶液,加入几滴氯水,再加入1滴
溶液,加入几滴氯水,再加入1滴 溶液,溶液变红,说明
溶液,溶液变红,说明 可将
可将 氧化。
氧化。 溶液与氯水反应的离子方程式为
溶液与氯水反应的离子方程式为(3)乙组同学认为甲组实验不够严谨,该组同学用煮沸冷却后的水配制溶液,向
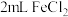 溶液中先加入
溶液中先加入 煤油,再于液面下依次加入几滴氯水和1滴
煤油,再于液面下依次加入几滴氯水和1滴 溶液,溶液变红,煤油的作用是
溶液,溶液变红,煤油的作用是(4)丙组同学取
 溶液,加入足量
溶液,加入足量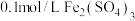 溶液混合后,滴加淀粉溶液,出现蓝色,该现象说明氧化性:
溶液混合后,滴加淀粉溶液,出现蓝色,该现象说明氧化性:
 (填“>”或“<”);另取
(填“>”或“<”);另取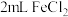 溶液,加入几小块锌片,实验现象为
溶液,加入几小块锌片,实验现象为 具有
具有(5)丁组同学为探究维生素C是否可将
 转化为
转化为 ,设计了如下实验。
,设计了如下实验。| 实验操作 | 实验现象 | 得出结论 |
取一定量 溶液于试管中,加入维生素C片,振荡溶解得到溶液a.取a溶液少许,滴加酸性 溶液于试管中,加入维生素C片,振荡溶解得到溶液a.取a溶液少许,滴加酸性 溶液。 溶液。 | 紫色褪去 | 维生素C可将 转化为 转化为 |
 转化为
转化为 ”的结论,原因是
”的结论,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】在潜水艇中可用过氧化钠作为供氧剂。请选择适当的化学试剂和实验用品,用下图中的实验装置(C中盛放的是过氧化钠)进行实验,证明过氧化钠可作供氧剂。

(1)B中盛有饱和NaHCO3溶液,其作用是___________ 。
(2)写出过氧化钠与二氧化碳反应的化学方程式___________ 。
(3)D中盛放的试剂是___________ ,其目的是___________ 。
(4)试管F中收集到的气体是___________ ,如何验证?___________ 。

(1)B中盛有饱和NaHCO3溶液,其作用是
(2)写出过氧化钠与二氧化碳反应的化学方程式
(3)D中盛放的试剂是
(4)试管F中收集到的气体是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】如图表示中学化学中常见物质的转化关系(部分条件已略去)。其中A属于正盐,B、C、E是常见的气体,C能使湿润的红色石蕊试纸变蓝,D是一种淡黄色固体。

回答下列问题:
(1)A物质的化学式是___________ ,A中存在的化学键有___________ 。
(2)C的电子式是___________ ,在上述①~④反应中属于氧化还原反应的是___________ (填编号)。
(3)写出B和D反应生成E的化学方程式,并用单线桥法表示电子的转移:___________ 。
(4)请写出反应④的化学方程式:___________ ,写出该反应在工业上的用途:___________ 。

回答下列问题:
(1)A物质的化学式是
(2)C的电子式是
(3)写出B和D反应生成E的化学方程式,并用单线桥法表示电子的转移:
(4)请写出反应④的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】盐X受热分解后的产物与其它几种常见物质有如图所示的转化关系(部分物质已略去)。常温下,A、C都是无色气体,F是红棕色气体,B为无色液体,H为淡黄色固体,I为紫红色固体单质。

请回答下列问题:
(1)A的化学式为___________ ,B的结构式为 ___________ ,H中含有的化学键为___________ 。
(2)写出C→E的化学方程式___________ 。
(3)写出G→D的离子方程式___________ 。
(4)若X受热分解后产生的A和C物质的量相等,则X的化学式为___________ 。

请回答下列问题:
(1)A的化学式为
(2)写出C→E的化学方程式
(3)写出G→D的离子方程式
(4)若X受热分解后产生的A和C物质的量相等,则X的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,而且其中的X、Y、Z的焰色试验均为黄色,而W为无色无味可使澄清石灰水变浑浊的气体,这四种化合物具有如图的转化关系(部分反应物、产物及反应条件已略去)。请回答:

(1)W的电子式是_______ ;
(2)X与Y在溶液中反应的离子方程式是_______ ;
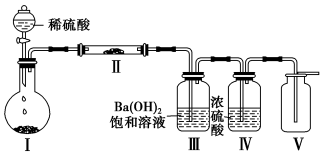
(3)X含有的四种元素之间(选其中二种、三种或四种元素)可组成多种化合物,现选用其中某些化合物装于如图装置Ⅰ、Ⅱ,利用图中的装置(夹持固定装置已略去)进行实验,若最终装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体单质。若此时装置Ⅱ中反应过程中共转移4 mol电子,则此时产生的无色气体单质为_______ mol;装置Ⅲ中发生反应的化学方程式是_______ 。

(1)W的电子式是
(2)X与Y在溶液中反应的离子方程式是
(3)X含有的四种元素之间(选其中二种、三种或四种元素)可组成多种化合物,现选用其中某些化合物装于如图装置Ⅰ、Ⅱ,利用图中的装置(夹持固定装置已略去)进行实验,若最终装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体单质。若此时装置Ⅱ中反应过程中共转移4 mol电子,则此时产生的无色气体单质为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,某同学进行CO2 与Na2O2反应的探究实验,回答下列问题。
(1)用下图装置制备纯净的CO2

①丙装置的名称是___________ ,乙、丙装置中盛装的试剂分别是___________ 、___________ 。
②若CO2中混有HCl,则HCl 与Na2O2反应的 化学方程式为___________ 。
(2)按照下面的装置图进行实验(夹持装置略)。

先组装仪器,然后___________ ,再用注射器1 抽取100 mL纯净的CO2,将其连接在K1处,注射器2 的活塞推到底后连接在K2处,具支U形管中装入足量的Na2O2粉末与玻璃珠。
(3)实验结束后,当注射器1 的活塞推到底时,测得注射器2 中气体体积为65 mL,则CO2的转化率是___________ 。
(1)用下图装置制备纯净的CO2

①丙装置的名称是
②若CO2中混有HCl,则HCl 与Na2O2反应的 化学方程式为
(2)按照下面的装置图进行实验(夹持装置略)。

先组装仪器,然后
(3)实验结束后,当注射器1 的活塞推到底时,测得注射器2 中气体体积为65 mL,则CO2的转化率是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】下表为元素周期表的一部分,回答有关问题:
(1)请写出硅元素在周期表中的位置___________ 。
(2)元素③的原子结构示意图为___________ 。
(3)元素①、④形成的四原子分子的电子式为___________ 。
(4)元素⑨的一种核素,其中子数为20,该核素符号为___________ 。
(5)元素④、⑤、⑥、⑧的离子半径由大到小的顺序是___________ 。(填离子符号)
(6)能比较元素⑦和⑧非金属性强弱的实验事实是___________ (填字母序号)。
A.最简单气态氢化物的酸性⑧强于⑦
B.⑦的最简单气态氢化物沸点为-60℃高于⑧的最简单气态氢化物沸点-85℃
C.在⑦的氢化物 的水溶液中通少量⑧的单质
的水溶液中通少量⑧的单质 气体可置换出单质Q
气体可置换出单质Q
(7)①将 含
含 、
、 、
、 的混合气体通过足量由④和⑤构成的淡黄色固体化合物,充分反应后气体体积变为
的混合气体通过足量由④和⑤构成的淡黄色固体化合物,充分反应后气体体积变为 ,则原气体中,
,则原气体中, 的体积为
的体积为___________ 。
②若将该淡黄色固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子含量几乎不变的有
,反应完毕后,溶液中上述离子含量几乎不变的有___________ 。(填离子符号)
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 四 | ⑨ | ⑩ |
(2)元素③的原子结构示意图为
(3)元素①、④形成的四原子分子的电子式为
(4)元素⑨的一种核素,其中子数为20,该核素符号为
(5)元素④、⑤、⑥、⑧的离子半径由大到小的顺序是
(6)能比较元素⑦和⑧非金属性强弱的实验事实是
A.最简单气态氢化物的酸性⑧强于⑦
B.⑦的最简单气态氢化物沸点为-60℃高于⑧的最简单气态氢化物沸点-85℃
C.在⑦的氢化物
 的水溶液中通少量⑧的单质
的水溶液中通少量⑧的单质 气体可置换出单质Q
气体可置换出单质Q(7)①将
 含
含 、
、 、
、 的混合气体通过足量由④和⑤构成的淡黄色固体化合物,充分反应后气体体积变为
的混合气体通过足量由④和⑤构成的淡黄色固体化合物,充分反应后气体体积变为 ,则原气体中,
,则原气体中, 的体积为
的体积为②若将该淡黄色固体投入到含有下列离子的溶液中:
 、
、 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子含量几乎不变的有
,反应完毕后,溶液中上述离子含量几乎不变的有
您最近一年使用:0次



