氢能是清洁能源之一,工业制取氢气涉及的重要反应之一是:
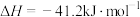
已知:①
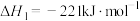
②
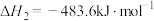
③

下列叙述正确的是

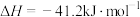
已知:①

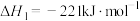
②

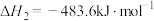
③


下列叙述正确的是
A. 的燃烧热为 的燃烧热为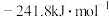 |
B. 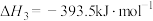 |
| C.12gC(s)不完全燃烧全部生成CO(g)时放出热量为221kJ |
D. 平衡常数表达式为 平衡常数表达式为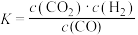 |
2024·陕西商洛·一模 查看更多[3]
(已下线)专题05 化学反应与能量-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)河南省焦作市博爱县第一中学2023-2024学年高三下学期开学化学试题2024届陕西省商洛市高三上学期尖子生学情诊断考试理综试题
更新时间:2024-01-08 21:56:54
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列热化学方程式或离子方程式中,正确的是:
| A.甲烷的标准燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1 |
B.500℃、30MPa下,将0.5mol N2和1.5molH2置 于密闭的窗口中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: △H=-38.6kJ·mol-1 △H=-38.6kJ·mol-1 |
C.氯化镁溶液与氨水反应: |
| D.钢铁腐蚀时可能发生的正极反应:2H2O+ O2+ 4e-=4OH一 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法或表示方法中正确的是
| A.氢气的燃烧热为285.8kJ/mol,即:2H2(g)+O2(g)=2H2O(l)ΔH=-285.8kJ/mol |
| B.已知:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的反应热ΔH=2×(-57.3)kJ/mol |
| C.等质量的硫蒸气和硫粉分别完全燃烧,前者放出的热量多 |
| D.由于红磷转化为白磷是放热反应,则红磷比白磷更稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列有关热化学方程式的叙述,正确的是
| A.若2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1,则1mol碳完全燃烧放出的热量大于110.5kJ |
| B.若CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-812.3kJ/mol,则甲烷的燃烧热为812.3kJ/mol |
C.若2NO2(g) N2O4(g) ΔH=56.9kJ·mol-1,则2molNO2(g)置于密闭容器中充分反应吸收热量为56.9kJ N2O4(g) ΔH=56.9kJ·mol-1,则2molNO2(g)置于密闭容器中充分反应吸收热量为56.9kJ |
| D.若H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-1,含1 mol CH3COOH的溶液与含1molNaOH的溶液混合,放出热量为57.3kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】将1L0.1mol/L的BaCl2溶液与足量稀硫酸充分反应放出放出akJ热量;将1L0.5mol/LHCl溶液与足量CH3COONa溶液充分反应放出bkJ热量(不考虑醋酸钠水解);将0.5L1mol/LH2SO4溶液与足量(CH3COO)2Ba(可溶性强电解质)溶液反应放出的热量为
| A.(4b-10a)kJ | B.(5a+2b)kJ | C.(5a-2b)kJ | D.(10a+4b)kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】反应
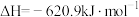 分三步进行,各步的相对能量变化如图I、II、III所示:
分三步进行,各步的相对能量变化如图I、II、III所示:不正确 的是

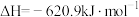 分三步进行,各步的相对能量变化如图I、II、III所示:
分三步进行,各步的相对能量变化如图I、II、III所示: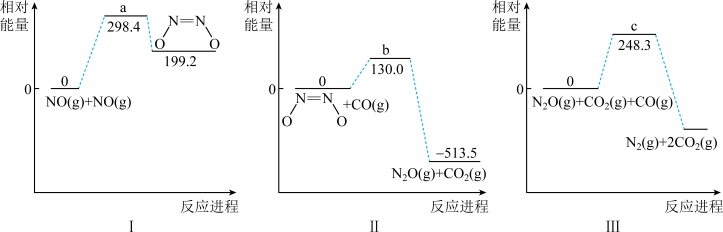
| A.三步分反应中决定总反应速率的是反应I |
B.I、II两步的总反应为 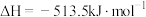 |
| C.根据图像无法判断过渡状态a、b、c的稳定性相对高低 |
D.反应III逆反应的活化能 (逆) (逆) |
您最近一年使用:0次
【推荐3】下列说法或表示法正确的是
| A.等量的白磷蒸气和白磷固体分别完全燃烧,后者放出热量多 |
| B.由C(s,石墨)=C(s,金刚石) ΔH=+1.19 kJ·mol-1可知,金刚石比石墨稳定 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l) ΔH=-285.8 kJ·mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】氢气用于烟气的脱氮、脱硫的反应:4H2(g)+2NO(g)+SO2(g) N2(g)+S(l)+4H2O(g) ΔH<0。下列有关说法正确的是
N2(g)+S(l)+4H2O(g) ΔH<0。下列有关说法正确的是
 N2(g)+S(l)+4H2O(g) ΔH<0。下列有关说法正确的是
N2(g)+S(l)+4H2O(g) ΔH<0。下列有关说法正确的是| A.当v(H2)=v(H2O)时,达到平衡 |
| B.升高温度,化学平衡正向移动 |
| C.使用高效催化剂可提高NO的平衡转化率 |
D.化学平衡常数学平表达式为K= |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知反应 ,在某温度下的平衡常数为400。此温度下,在密闭容器中加入
,在某温度下的平衡常数为400。此温度下,在密闭容器中加入 ,反应进行到某时刻测得各组分的浓度如下:
,反应进行到某时刻测得各组分的浓度如下:
下列叙述中正确的是
 ,在某温度下的平衡常数为400。此温度下,在密闭容器中加入
,在某温度下的平衡常数为400。此温度下,在密闭容器中加入 ,反应进行到某时刻测得各组分的浓度如下:
,反应进行到某时刻测得各组分的浓度如下:物质 |
|
|
|
浓度 |
|
|
|

A.该反应的平衡常数表达式为  |
B.该时刻正、逆反应速率的大小: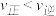 |
C.平衡时 |
D.若加入 后,经 后,经 反应达到平衡,该时间内反应速率 反应达到平衡,该时间内反应速率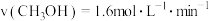 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】将一定量纯净的氨基甲酸铵固体置于恒容的密闭真空容器中,在恒定温度下使其达到分解平衡:NH2COONH4(s)  2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
下列说法正确的是
 2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:
2NH3(g)+CO2(g),实验测得不同温度下的平衡数据列于下表:| 温度/℃ | 15 | 20 | 25 | 30 | 35 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/ 10-3mol·L-1 | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A.该反应在低温下可以自发进行 |
| B.当体系中气体的平均相对分子质量不变时,说明该反应达到了平衡状态 |
| C.恒温条件下,向容器中再充入2mol NH3和1molCO2,平衡向左移动,平衡后,NH3的浓度减小 |
| D.15℃时,该反应的平衡常数约为2.05×10-9 |
您最近一年使用:0次