下列实验的现象与对应结论均正确的是

| A.A | B.B | C.C | D.D |
2014·河南郑州·一模 查看更多[1]
(已下线)2013-2014河南省中原名校高三高考仿真模拟统一考试理综化学试卷
更新时间:2014-06-12 22:46:54
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏伽德罗常数的值,下列有关叙述正确的是
| A.标准状况下,22.4LHF中含有的分子数为NA |
| B.常温常压下,硝酸与铜反应得到NO2、N2O4共23g,则铜失去的电子数为0.5NA |
| C.标准状况下,8.96L平均相对分子质量为3.5的H2与D2含有的中子数为0.3NA |
| D.0.1L18mol/L浓硫酸与足量金属铜在加热条件下充分反应,生成0.9NA个SO2分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】用如图所示装置完成相应实验(a、b、c中分别盛有试剂1、2、3),能达到实验目的的是
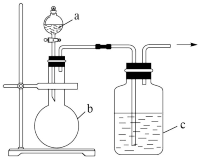

| 选项 | 试剂1 | 试剂2 | 试剂3 | 实验目的 |
| A | 浓氨水 | CaO | 浓硫酸 | 制取干燥的NH3 |
| B | 浓硫酸 | Cu片 | 浓硫酸 | 制取干燥的SO2 |
| C | 浓盐酸 | KMnO4 | 饱和NaCl溶液 | 制取Cl2并除去HCl |
| D | 浓硝酸 | Fe片 | H2O | 制取干燥的NO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】表示下列反应的方程式正确的是
A.铁粉与水蒸气共热,生成可燃性气体: |
B.过量的铁粉和氯气反应: |
C.向 浊液中加入 浊液中加入 溶液,生成红褐色沉淀: 溶液,生成红褐色沉淀: |
D.向 溶液中滴加 溶液中滴加 溶液,溶液由浅绿色变为黄色: 溶液,溶液由浅绿色变为黄色: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】由下列实验操作及现象,可得出相应正确结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 常温下,分别测定浓度均为1mol/L的 溶液和NaCl溶液的pH 溶液和NaCl溶液的pH | pH均等于7 | 常温下,这两种溶液中水的电离程度相等 |
| B | 将红热的铁粉与水蒸气反应后的固体溶于过量稀硫酸中,再滴入几滴KSCN溶液 | 溶液未变红 | 铁粉与水蒸气反应生成 |
| C | 常温下,将Fe、Cu与浓硝酸组成原电池 | 电流计指针偏转 | Fe金属活动性强于Cu |
| D | 将0.1mol/L  溶液滴入到2ml 0.1mol/L 溶液滴入到2ml 0.1mol/L  溶液中至不再有沉淀产生,再滴加几滴0.1mol/L 溶液中至不再有沉淀产生,再滴加几滴0.1mol/L  溶液 溶液 | 先有白色沉淀生成,后变为黑色沉淀 |  (ZnS)> (ZnS)> (CuS) (CuS) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列事实或现象不能用元素周期律解释的是
| A.相同温度时,等物质的量浓度的硫酸的pH小于高氯酸 |
| B.醛基的碳氧双键中,氧原子带部分单位的负电荷 |
| C.相同条件下,Mg与水的反应不如Na与水的反应剧烈 |
| D.向KBr溶液中滴加氯水,再加四氯化碳,溶液分层,下层为橙色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】根据表1信息,判断以下叙述正确的
表1 部分短周期元素的原子半径及主要化合价
表1 部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A.M与T形成的化合物具有两性 | B.氢化物的沸点为:H2T<H2R |
| C.L2+与R2-的核外电子数相等 | D.元素的金属性强弱程度为:L<Q |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】实验室验证钠能与二氧化碳发生反应,并确定其产物的装置如图所示(已知:PdC12溶液遇CO能产生黑色的Pd),下列说法错误的是


| A.装置①的仪器还可以制取H2、NH3等气体 |
| B.装置⑤中石灰水变浑浊后,再点燃酒精灯 |
| C.装置②③中分别盛装饱和Na2CO3溶液、浓H2SO4 |
| D.装置⑥中有黑色沉淀,发生的反应是PdC12+CO+H2O=Pd↓+CO2+2HCl |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】为了确定SbCl3、SbCl5、SnCl4是否为离子晶体,可以进行下列实验,其中合理、可靠的是
| A.观察常温下的状态,SbCl5是黄色液体,SnCl4为无色液体。结论:SbCl5和SnCl4都是离子晶体 |
| B.测定SbCl3、SbCl5、SnCl4的熔点依次为73.5 ℃、2.8 ℃、-33 ℃。结论:SbCl3、SbCl5、SnCl4都不是离子晶体 |
| C.将SbCl3、SbCl5、SnCl4溶解于水中,滴入HNO3酸化的AgNO3溶液,产生白色沉淀。结论:SbCl3、SbCl5、SnCl4都是离子晶体 |
| D.测定SbCl3、SbCl5、SnCl4的水溶液的导电性,发现它们都可以导电。结论:SbCl3、SbCl5、SnCl4都是离子晶体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某氮肥样品可能含有NH4HCO3、NH4C1、NH4NO3中的一种或几种。称取该样品1.000克,溶于水配成100mL溶液。将溶液分成两等份依次完成如下实验:
①向一份溶液中加入10mL 0.2mol•L-1的盐酸与之充分反应,可收集到标准状况下的CO2气体44.8mL(设产生的CO2全部逸出)。
②向另一份溶液中加入足量的6mol•L-1氢氧化钠溶液,加热,产生的气体(设产生的NH3全部逸出)至少需要25mL 0.15mol•L-1的硫酸才能被完全反应。
下列说法正确的是
①向一份溶液中加入10mL 0.2mol•L-1的盐酸与之充分反应,可收集到标准状况下的CO2气体44.8mL(设产生的CO2全部逸出)。
②向另一份溶液中加入足量的6mol•L-1氢氧化钠溶液,加热,产生的气体(设产生的NH3全部逸出)至少需要25mL 0.15mol•L-1的硫酸才能被完全反应。
下列说法正确的是
| A.1.000 g样品中一定含有NH4HCO3 0.316克 |
| B.向①反应所得的溶液中加入硝酸酸化的硝酸银溶液,若有白色沉淀生成,说明原样品中一定含有NH4C1 |
| C.原样品的含氮量为21% |
| D.无需另外再设计实验验证,就能确定原样品中是否含有NH4Cl |
您最近一年使用:0次






