电化学在生活中的应用广泛,请根据电化学原理回答下列问题:
(1)将锌片、铜片置于稀硫酸中并以导线连接起来组成原电池,可以获得电流,则Zn电极上发生的电极反应式为___________ 。
(2)如图所示是甲烷燃料电池的原理示意图:___________ 。
②电池工作一段时间后,电解质溶液的pH___________ (填“增大”、“减小”或“不变”)。
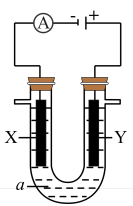
(3)按图所示装置,以石墨为电极电解氯化钠溶液,同时在两边各滴入几滴酚酞溶液,则电解时在X极附近观察到的现象是___________ ,若将X电极材料换为Cu,则X电极上的电极反应式将___________ (填“发生变化”或“不变”)。
(1)将锌片、铜片置于稀硫酸中并以导线连接起来组成原电池,可以获得电流,则Zn电极上发生的电极反应式为
(2)如图所示是甲烷燃料电池的原理示意图:
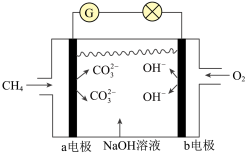
②电池工作一段时间后,电解质溶液的pH
(3)按图所示装置,以石墨为电极电解氯化钠溶液,同时在两边各滴入几滴酚酞溶液,则电解时在X极附近观察到的现象是
更新时间:2024-01-12 17:14:31
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】 具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备
具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备 ,采用的装置如图B所示,以
,采用的装置如图B所示,以 辅助的
辅助的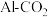 电池(如图A)为电源进行电解。
电池(如图A)为电源进行电解。
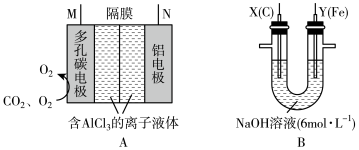
(1) 的电子式为
的电子式为___________ 。
(2)图A中正极反应式为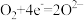 、
、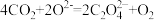 ,则该电池的总反应方程式为
,则该电池的总反应方程式为___________ 。
(3)图A中N极名称是___________ (填“正极”或“负极”),M极与图B___________ (填“X”或“Y”)极相连。
(4)电解过程中,图BX极区溶液的pH___________ (填“增大”“减小”或“不变”)。
(5)图B中两极均有气体产生,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况下的气体体积),则Y电极质量减小___________ g。
 具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备
具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备 ,采用的装置如图B所示,以
,采用的装置如图B所示,以 辅助的
辅助的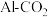 电池(如图A)为电源进行电解。
电池(如图A)为电源进行电解。
(1)
 的电子式为
的电子式为(2)图A中正极反应式为
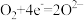 、
、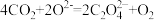 ,则该电池的总反应方程式为
,则该电池的总反应方程式为(3)图A中N极名称是
(4)电解过程中,图BX极区溶液的pH
(5)图B中两极均有气体产生,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况下的气体体积),则Y电极质量减小
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】电化学知识给人类的生活和工业生产带来极大的方便。回答下列问题:
(1)新型Na-CO2电池工作原理为:4Na+3CO2 2Na2CO3+C,原电池以熔融的Na2CO3为电解质,正极的电极反应式为
2Na2CO3+C,原电池以熔融的Na2CO3为电解质,正极的电极反应式为_______ 。
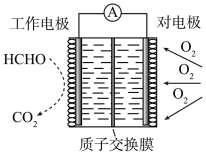
(2)一种检测空气中甲醛含量的电化学传感器的工作原理如图所示,工作电极的电极反应式为_______ ,工作时对电极附近电解质溶液的pH_______ (填“增大”“减小”或“不变”),当进入传感器反应的甲醛为9 g时,有_______ mol H+移向_______ (填“工作电极”或“对电极”)。
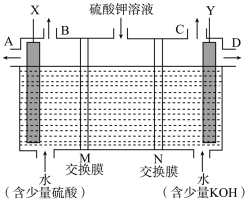
(3)用如图装置电解硫酸钾溶液,可获得H2、O2、硫酸和氢氧化钾溶液。X电极与电源的_______ 极相连,H2从_______ 口导出(填“B”或“C”),M、N交换膜中属于阳离子交换膜的是_______ 。
(1)新型Na-CO2电池工作原理为:4Na+3CO2
 2Na2CO3+C,原电池以熔融的Na2CO3为电解质,正极的电极反应式为
2Na2CO3+C,原电池以熔融的Na2CO3为电解质,正极的电极反应式为(2)一种检测空气中甲醛含量的电化学传感器的工作原理如图所示,工作电极的电极反应式为

(3)用如图装置电解硫酸钾溶液,可获得H2、O2、硫酸和氢氧化钾溶液。X电极与电源的

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】Ⅰ.一定温度下在某定容容器中发生反应:2A(g)+3B(g)=2C(g),开始时,A的浓度为2mol·L-1,B的浓度为4mol·L-1,2min后,A的浓度减少0.8mol·L-1,则:
(1)v(B)=_______ ,v(C)=_______ 。
(2)在2min末,C的浓度是_______ ,B的浓度是_______ 。
Ⅱ.如图所示的原电池装置中:

(1)_______ (填“铜”或“锌”)作负极。
(2)正极的电极反应式为_______ 。
(3)电子的流向_______ 。
(4)若铜电极上产生了标准状况下11.2L气体,则Zn电极会减轻_______ g。
(1)v(B)=
(2)在2min末,C的浓度是
Ⅱ.如图所示的原电池装置中:

(1)
(2)正极的电极反应式为
(3)电子的流向
(4)若铜电极上产生了标准状况下11.2L气体,则Zn电极会减轻
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】我国提出争取在2030年前实现碳达峰,2060年前实现碳中和,这对于改变环境、实现绿色发展至关重要。因此,研发CO2利用技术、降低空气中CO2含量成为化学科学家研究的热点。回答下列问题:
(1)利用工业废气中的CO2可制取甲醇,其反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0。为探究用CO2生产燃料CH3OH的反应原理,现进行如下实验:在T℃时,向2L恒容密闭容器中充入1molCO2和3molH2,进行上述反应,10min时反应达到平衡,0~10min内,H2的反应速率为0.09mol•L-1•min-1。该温度下的平衡常数K=
CH3OH(g)+H2O(g) △H<0。为探究用CO2生产燃料CH3OH的反应原理,现进行如下实验:在T℃时,向2L恒容密闭容器中充入1molCO2和3molH2,进行上述反应,10min时反应达到平衡,0~10min内,H2的反应速率为0.09mol•L-1•min-1。该温度下的平衡常数K=______ (保留三位有效数字)。
(2)电化学法将CO2转化为甲酸。科学家近年发明了一种新型Zn-CO2水介质电池。如图1所示,电极分别为金属铈和选择性催化材料,放电时,CO2被转化为储氢物质甲酸。注:双极隔膜为一层阳离子交换膜和一层阴离子交换膜复合而成,中间为水,作为电解质溶液中H+和OH-的来源。
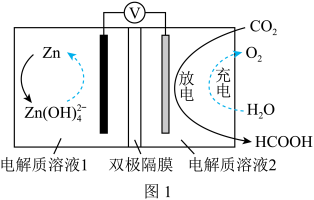
①放电时,正极电极反应式为______ 。
②与Zn极室相连的离子交换膜为______ 。
(3)热化学法将CO2转化为甲醇。CO2催化加氢主要反应有:
反应I.CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.4kJ•mol-1
CH3OH(g)+H2O(g) △H1=-49.4kJ•mol-1
反应Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.2kJ•mol-1
CO(g)+H2O(g) △H2=+41.2kJ•mol-1
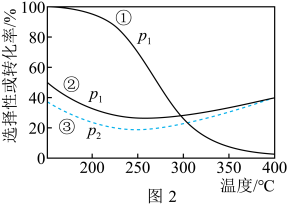
压强分别为p1、p2时,将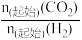 =1:3的混合气体置于密闭容器中反应,不同温度下平衡时体系中CO2转化率和CH3OH(或CO)选择性如图2所示。
=1:3的混合气体置于密闭容器中反应,不同温度下平衡时体系中CO2转化率和CH3OH(或CO)选择性如图2所示。
已知:CH3OH(或CO)的选择性=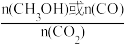 ×100%
×100%
①曲线①代表的是______ 的选择性曲线(填“CH3OH”或“CO”)。
②p1______ p2(选填“=”、“>”或“<”)。
③温度高于250℃,曲线②或曲线③上升的原因是______ 。
(1)利用工业废气中的CO2可制取甲醇,其反应为CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H<0。为探究用CO2生产燃料CH3OH的反应原理,现进行如下实验:在T℃时,向2L恒容密闭容器中充入1molCO2和3molH2,进行上述反应,10min时反应达到平衡,0~10min内,H2的反应速率为0.09mol•L-1•min-1。该温度下的平衡常数K=
CH3OH(g)+H2O(g) △H<0。为探究用CO2生产燃料CH3OH的反应原理,现进行如下实验:在T℃时,向2L恒容密闭容器中充入1molCO2和3molH2,进行上述反应,10min时反应达到平衡,0~10min内,H2的反应速率为0.09mol•L-1•min-1。该温度下的平衡常数K=(2)电化学法将CO2转化为甲酸。科学家近年发明了一种新型Zn-CO2水介质电池。如图1所示,电极分别为金属铈和选择性催化材料,放电时,CO2被转化为储氢物质甲酸。注:双极隔膜为一层阳离子交换膜和一层阴离子交换膜复合而成,中间为水,作为电解质溶液中H+和OH-的来源。

①放电时,正极电极反应式为
②与Zn极室相连的离子交换膜为
(3)热化学法将CO2转化为甲醇。CO2催化加氢主要反应有:
反应I.CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.4kJ•mol-1
CH3OH(g)+H2O(g) △H1=-49.4kJ•mol-1反应Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.2kJ•mol-1
CO(g)+H2O(g) △H2=+41.2kJ•mol-1压强分别为p1、p2时,将
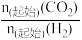 =1:3的混合气体置于密闭容器中反应,不同温度下平衡时体系中CO2转化率和CH3OH(或CO)选择性如图2所示。
=1:3的混合气体置于密闭容器中反应,不同温度下平衡时体系中CO2转化率和CH3OH(或CO)选择性如图2所示。
已知:CH3OH(或CO)的选择性=
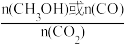 ×100%
×100%①曲线①代表的是
②p1
③温度高于250℃,曲线②或曲线③上升的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】回答下列问题:
(1)向某体积固定的密闭容器中加入0.3mol A、0.1mol C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:

①若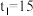 ,则
,则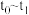 内反应速率
内反应速率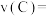
_______ ,A的转化率为_______ ;
②写出反应的化学方程式:_______ ;
(2)工业上可以通过 (g)与
(g)与 (g)反应制备
(g)反应制备 (g):
(g):
 。
。
在一体积固定的密闭容器中投入一定量的CO和 进行上述反应。下列叙述中能说明上述反应达到平衡状态的是_______。
进行上述反应。下列叙述中能说明上述反应达到平衡状态的是_______。
(3)向恒容密闭容器中充入一定量 和
和 ,在不同催化剂作用下合成甲醇,反应进行相同时间后(均未达到化学平衡状态),
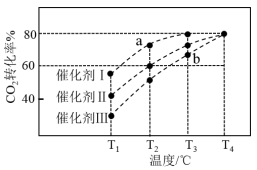
,在不同催化剂作用下合成甲醇,反应进行相同时间后(均未达到化学平衡状态), 的转化率随反应温度的变化如图所示。其中a点
的转化率随反应温度的变化如图所示。其中a点 的转化率高于b点的原因是
的转化率高于b点的原因是_______ 。
(4)燃料电池是一种高效、环境友好的供电装置,如图为 燃料电池的工作原理示意图,a、b均为惰性电极。
燃料电池的工作原理示意图,a、b均为惰性电极。

①使用时,空气从_______ 口通入(填“A”或“B”);
②a极的电极反应为:_______ 。
(1)向某体积固定的密闭容器中加入0.3mol A、0.1mol C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:

①若
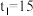 ,则
,则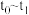 内反应速率
内反应速率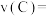
②写出反应的化学方程式:
(2)工业上可以通过
 (g)与
(g)与 (g)反应制备
(g)反应制备 (g):
(g):
 。
。在一体积固定的密闭容器中投入一定量的CO和
 进行上述反应。下列叙述中能说明上述反应达到平衡状态的是_______。
进行上述反应。下列叙述中能说明上述反应达到平衡状态的是_______。A.反应中CO与 的物质的量之比为1:1 的物质的量之比为1:1 | B.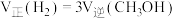 |
| C.混合气体的压强不随时间的变化而变化 | D.混合气体的密度不再改变 |
 和
和 ,在不同催化剂作用下合成甲醇,反应进行相同时间后(均未达到化学平衡状态),
,在不同催化剂作用下合成甲醇,反应进行相同时间后(均未达到化学平衡状态), 的转化率随反应温度的变化如图所示。其中a点
的转化率随反应温度的变化如图所示。其中a点 的转化率高于b点的原因是
的转化率高于b点的原因是
(4)燃料电池是一种高效、环境友好的供电装置,如图为
 燃料电池的工作原理示意图,a、b均为惰性电极。
燃料电池的工作原理示意图,a、b均为惰性电极。
①使用时,空气从
②a极的电极反应为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】SCR和NSR技术可有效降低柴油发动机在空气过量条件下的NOx排放。
(1)SCR(选择性催化还原)工作原理:
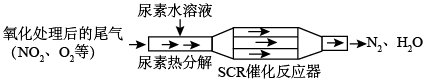
尿素[CO(NH2)2]水溶液热分解为NH3和CO2,请写出CO2的电子式___________ 。
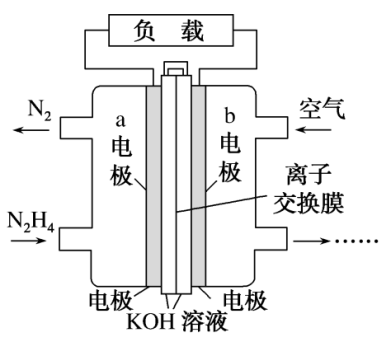
(2)肼(N2H4)可以用作燃料电池的原料。肼的结构式为___________ ;一种以液态肼为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。a电极是电极的___________ 极(填“正”或“负”),a电极的电极反应式为___________ 。
(3)已知:N2(g)+O2(g)=2NO(g)△H1=+180.5kJ·mol-1
C(s)+O2(g)=CO2(g)△H2=-393.5kJ·mol-1
2C(s)+O2(g)=2CO(g)△H3=-221.0kJ·mol-1
若某反应的平衡常数表达式为K=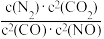 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式___________ 。
(4)已知植物光合作用发生的反应如下:6CO2(g)+6H2O(l)⇌C6H12O6(s)+6O2(g)△H=+669.62kJ/mol,该反应达到化学平衡后,若改变下列条件,CO2转化率增大的是___________ 。
a.增大CO2的浓度b.取走一半C6H12O6c.加入催化剂d.适当升高温度
(5)N2O5的分解反应2N2O5(g)⇌4NO2(g)+O2(g),由实验测得在67℃时N2O5的浓度随时间的变化如下:
计算在0~2min时段,化学反应速率v(NO2)=___________ mol∙L-1∙min-1。
(1)SCR(选择性催化还原)工作原理:

尿素[CO(NH2)2]水溶液热分解为NH3和CO2,请写出CO2的电子式
(2)肼(N2H4)可以用作燃料电池的原料。肼的结构式为

(3)已知:N2(g)+O2(g)=2NO(g)△H1=+180.5kJ·mol-1
C(s)+O2(g)=CO2(g)△H2=-393.5kJ·mol-1
2C(s)+O2(g)=2CO(g)△H3=-221.0kJ·mol-1
若某反应的平衡常数表达式为K=
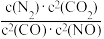 ,请写出此反应的热化学方程式
,请写出此反应的热化学方程式(4)已知植物光合作用发生的反应如下:6CO2(g)+6H2O(l)⇌C6H12O6(s)+6O2(g)△H=+669.62kJ/mol,该反应达到化学平衡后,若改变下列条件,CO2转化率增大的是
a.增大CO2的浓度b.取走一半C6H12O6c.加入催化剂d.适当升高温度
(5)N2O5的分解反应2N2O5(g)⇌4NO2(g)+O2(g),由实验测得在67℃时N2O5的浓度随时间的变化如下:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| C(N2O5)/(mol·L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
计算在0~2min时段,化学反应速率v(NO2)=
您最近一年使用:0次
【推荐1】CO2是导致温室效应的主要物质。CO2加氢合成甲醇可为实现“碳达峰”“碳中和”提供技术支持。回答下列问题:
(1)在25℃、101kPa下,1g液态甲醇燃烧生成CO2和液态水时放出22.5kJ热量,则该反应的热化学方程式为_______ 、
(2)在一定容积的密闭容器中,进行化学反应: ,其化学平衡常数K与温度t的关系如下表所示:
,其化学平衡常数K与温度t的关系如下表所示:
①该反应为_______ (填“吸热”或“放热”)反应。
②提高H2的平衡转化率的措施是_______ 。(写出两条)
(3)在一定温度下,将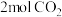 和
和 充入2L的恒容密闭容器中,发生反应
充入2L的恒容密闭容器中,发生反应 ,达到平衡时,测得混合气体中
,达到平衡时,测得混合气体中 的物质的量分数为25%,则该反应中CO2的转化率为
的物质的量分数为25%,则该反应中CO2的转化率为_______ (保留小数点后一位小数),化学平衡常数为_______ 。
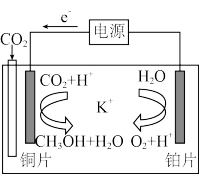
(4)如图所示,利用一种钾盐水溶液作电解质溶液,CO2电催化还原为甲醇。在阴极上的电极反应式为_______ 。
(1)在25℃、101kPa下,1g液态甲醇燃烧生成CO2和液态水时放出22.5kJ热量,则该反应的热化学方程式为
(2)在一定容积的密闭容器中,进行化学反应:
 ,其化学平衡常数K与温度t的关系如下表所示:
,其化学平衡常数K与温度t的关系如下表所示:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
②提高H2的平衡转化率的措施是
(3)在一定温度下,将
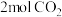 和
和 充入2L的恒容密闭容器中,发生反应
充入2L的恒容密闭容器中,发生反应 ,达到平衡时,测得混合气体中
,达到平衡时,测得混合气体中 的物质的量分数为25%,则该反应中CO2的转化率为
的物质的量分数为25%,则该反应中CO2的转化率为(4)如图所示,利用一种钾盐水溶液作电解质溶液,CO2电催化还原为甲醇。在阴极上的电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】航天员呼吸产生的CO2用下列反应处理,可实现其合理利用。反应Ⅰ:CO2(g)+4H2(g)⇌CH4(g)+2H2O(g)
(1)已知H2(g)、CH4(g)的燃烧热分别为A kJ/mol、B kJ/mol,H2O(l)=H2O(g)△H=+C kJ/mol。计算反应Ⅰ的△H=_______ kJ/mol。
(2)将原料气按n(CO2)∶n(H2)=1:4置于密闭容器中发生反应Ⅰ,测得H2O(g)的物质的量分数与温度的关系如图所示(虚线表示平衡曲线)。
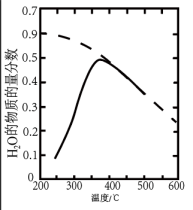
①温度过高或过低均不利于该反应的进行,原因是________ 。
②200℃达到平衡时体系的总压强为p,该反应平衡常数Kp的计算式为____ 。(不必化简。用平衡分压代替平衡浓度计算)
(3)一种新的利用方案是Ⅱ:反应:CO2(g)+2H2(g)⇌C(s)+2H2O(g)△H
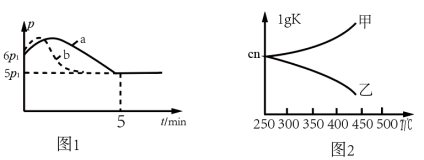
①向体积为2 L且带气压计的恒容密闭容器中通入0.08 mol H2和0.04 mol CO2发生反应Ⅱ。若反应起始和平衡时温度相同(均为250℃),测得反应过程中压强(P)随时间(t)的变化如图1曲线a所示,则△H___ 0(填“>”“<”或“不确定”)
②若其它条件相同,仅改变某一条件时,测得其压强(P)随时间(t)的变化如图1曲线b所示,则改变的条件是_______ 。
③图2是甲、乙两同学描绘上述反应平衡常数的对数值(lgK)与温度的变化关系,其中正确的曲线是_______ (填“甲”或“乙”),m值为______ 。
④反应Ⅱ必须在高温下才能启动,原因是______________ 。
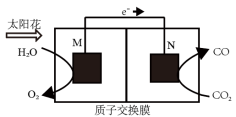
(4)科学家还研究了处理CO2(g)另外的方法,利用下图所示装置可以将CO2转化为气体燃料CO。该装置工作时,N电极的电极反应式为______________ 。
(1)已知H2(g)、CH4(g)的燃烧热分别为A kJ/mol、B kJ/mol,H2O(l)=H2O(g)△H=+C kJ/mol。计算反应Ⅰ的△H=
(2)将原料气按n(CO2)∶n(H2)=1:4置于密闭容器中发生反应Ⅰ,测得H2O(g)的物质的量分数与温度的关系如图所示(虚线表示平衡曲线)。

①温度过高或过低均不利于该反应的进行,原因是
②200℃达到平衡时体系的总压强为p,该反应平衡常数Kp的计算式为
(3)一种新的利用方案是Ⅱ:反应:CO2(g)+2H2(g)⇌C(s)+2H2O(g)△H
①向体积为2 L且带气压计的恒容密闭容器中通入0.08 mol H2和0.04 mol CO2发生反应Ⅱ。若反应起始和平衡时温度相同(均为250℃),测得反应过程中压强(P)随时间(t)的变化如图1曲线a所示,则△H
②若其它条件相同,仅改变某一条件时,测得其压强(P)随时间(t)的变化如图1曲线b所示,则改变的条件是
③图2是甲、乙两同学描绘上述反应平衡常数的对数值(lgK)与温度的变化关系,其中正确的曲线是

④反应Ⅱ必须在高温下才能启动,原因是
(4)科学家还研究了处理CO2(g)另外的方法,利用下图所示装置可以将CO2转化为气体燃料CO。该装置工作时,N电极的电极反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】已知甲酸的酸性强于醋酸。
(1)醋酸铵溶液呈中性,则甲酸铵溶液的pH____ 7(填“>”、“<”或“=”);若HCOONH4、NH4HSO4、NH4Cl三种溶液中的c(NH4+)相同,则c(HCOONH4)、c(NH4Cl)、c(NH4HSO4)的由大到小的顺序是_____________________________________ 。
(2)常温下0.01 mol·L-1的氨水中 ,该溶液的pH为
,该溶液的pH为_________ 。向0.01 mol·L-1的甲酸溶液中逐滴加入0.01 mol·L-1的氨水,该过程中的离子浓度关系不可能为__________ 。
A.c(HCOO-)>c(H+)>c(NH4+)>c(OH-) B.c(HCOO-)> c(NH4+)> c(H+) >c(OH-)
C.c(HCOO-)= c(NH4+) > c(H+) =c(OH-) D.c(HCOO-)> c(NH4+)>c(OH-)> c(H+)
E.c(NH4+)>c(HCOO-)> c(OH-)>c(H+)
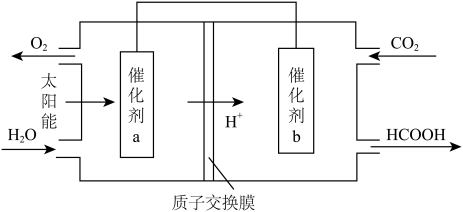
(3)如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。催化剂a附近的pH_______ (填“增大”、“不变”或“减小”),催化剂b表面发生的电极反应式为___________________ 。
(4)常温下,0.02 mol·L-1的HCOONa溶液pH=8,则常温下HCOOH的电离常数Ka约为_____________ 。
(1)醋酸铵溶液呈中性,则甲酸铵溶液的pH
(2)常温下0.01 mol·L-1的氨水中
 ,该溶液的pH为
,该溶液的pH为A.c(HCOO-)>c(H+)>c(NH4+)>c(OH-) B.c(HCOO-)> c(NH4+)> c(H+) >c(OH-)
C.c(HCOO-)= c(NH4+) > c(H+) =c(OH-) D.c(HCOO-)> c(NH4+)>c(OH-)> c(H+)
E.c(NH4+)>c(HCOO-)> c(OH-)>c(H+)
(3)如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。催化剂a附近的pH

(4)常温下,0.02 mol·L-1的HCOONa溶液pH=8,则常温下HCOOH的电离常数Ka约为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】Ⅰ.甲醇燃料电池是符合绿色化学理念的新型燃料电池,如图是以甲醇燃料电池(甲池)为电源的电解装置。已知:A、B、C、D、E、F都是惰性电极,丙中为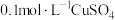 溶液(假设反应前后溶液体积不变),当向甲池通入物质a和b时,D极附近呈红色。
溶液(假设反应前后溶液体积不变),当向甲池通入物质a和b时,D极附近呈红色。___________ 。
(2)乙装置中D电极方程式为___________ 。
(3)丙装置中总反应的离子方程式为___________ 。
(4)当乙装置中C电极收集到224mL(标况)气体时,丙中溶液的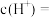
___________ mol。
Ⅱ.二氧化氯(ClO2)是一种高效、广谱、安全、会与碱反应的杀菌、消毒剂。利用食盐水制取ClO2的工业流程如下图所示: 的装置。写出阳极产生
的装置。写出阳极产生 的电极反应式:
的电极反应式:___________ 。电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为___________ mol。
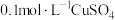 溶液(假设反应前后溶液体积不变),当向甲池通入物质a和b时,D极附近呈红色。
溶液(假设反应前后溶液体积不变),当向甲池通入物质a和b时,D极附近呈红色。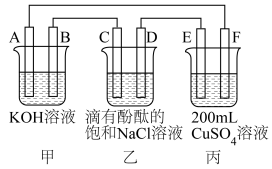
(2)乙装置中D电极方程式为
(3)丙装置中总反应的离子方程式为
(4)当乙装置中C电极收集到224mL(标况)气体时,丙中溶液的
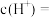
Ⅱ.二氧化氯(ClO2)是一种高效、广谱、安全、会与碱反应的杀菌、消毒剂。利用食盐水制取ClO2的工业流程如下图所示:
 的装置。写出阳极产生
的装置。写出阳极产生 的电极反应式:
的电极反应式: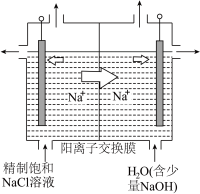
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
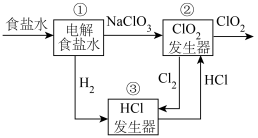
【推荐2】氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱和氯的含氧酸盐等系列化工产品。下图是离子交换膜法电解食盐水的示意图,图中的离子交换膜只允许阳离子通过。
完成下列填空:
(1)写出电解饱和食盐水的离子方程式:_________________ 。
(2)离子交换膜的作用为__________ 、_________________ 。
(3)精制饱和食盐水从图中___ (选填“a”、“b”、“c”或“d”)位置补充,氢氧化钠溶液从图中______ 位置流出。
(4)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3•H2O。已知:
a.常温下,醋酸和NH3•H2O的电离平衡常数均为1.74×10﹣5;
b.CH3COOH+NaHCO3═CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈_____ 性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈_____ 性,NH4HCO3溶液中物质的量浓度最大的离子是_____ (填化学式)。

完成下列填空:
(1)写出电解饱和食盐水的离子方程式:
(2)离子交换膜的作用为
(3)精制饱和食盐水从图中
(4)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3•H2O。已知:
a.常温下,醋酸和NH3•H2O的电离平衡常数均为1.74×10﹣5;
b.CH3COOH+NaHCO3═CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
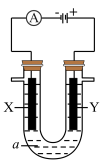
【推荐3】电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,在 X极附近观察到的现象是:________________ 。
(2)Y电极上的电极反应式是_________ ,检验该电极反应产物的方法是:______________ 。
(3)如果用电解方法精炼粗铜(粗铜中含有杂质锌和银),电解液a选用CuSO4溶液,则Y 电极的材料是____ ,电极反应式是_________________ 。
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,在 X极附近观察到的现象是:
(2)Y电极上的电极反应式是
(3)如果用电解方法精炼粗铜(粗铜中含有杂质锌和银),电解液a选用CuSO4溶液,则Y 电极的材料是
您最近一年使用:0次



