某工厂的工业废水中含有大量的 、较多量的
、较多量的 和
和 ,为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀
,为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀 、NaOH溶液)
、NaOH溶液)

(1)若废水是由 、
、 和
和 组成的混合溶液,其中
组成的混合溶液,其中 ,
, ,
, ,(溶液中
,(溶液中 和
和 浓度忽略不计),则
浓度忽略不计),则 为
为________  。
。
(2)试剂①是________ 。
(3)固体E的成分是________ (填化学式),操作c名称为________ 。
(4)若取2mL溶液D加入试管中,然后向其中滴加氢氧化钠溶液,可观察到的现象是________ ,此过程中涉及氧化还原反应的化学方程式是________ 。
(5)回收的 经一系列变化后可制得一种新型绿色净水剂高铁酸钠
经一系列变化后可制得一种新型绿色净水剂高铁酸钠 ,主要用于饮用水处理。其中一种制备原理如下,请配平该反应的离子方程式:
,主要用于饮用水处理。其中一种制备原理如下,请配平该反应的离子方程式:_____
________ ________
________ ________
________ ________
________ ________
________ ________
________ ,
,
当有 生成时,转移电子的数目约为
生成时,转移电子的数目约为________ 个。
 、较多量的
、较多量的 和
和 ,为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀
,为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据下列流程图,完成回收硫酸亚铁和铜的实验方案。(可供选择的试剂为铁粉、稀 、NaOH溶液)
、NaOH溶液)
(1)若废水是由
 、
、 和
和 组成的混合溶液,其中
组成的混合溶液,其中 ,
, ,
, ,(溶液中
,(溶液中 和
和 浓度忽略不计),则
浓度忽略不计),则 为
为 。
。(2)试剂①是
(3)固体E的成分是
(4)若取2mL溶液D加入试管中,然后向其中滴加氢氧化钠溶液,可观察到的现象是
(5)回收的
 经一系列变化后可制得一种新型绿色净水剂高铁酸钠
经一系列变化后可制得一种新型绿色净水剂高铁酸钠 ,主要用于饮用水处理。其中一种制备原理如下,请配平该反应的离子方程式:
,主要用于饮用水处理。其中一种制备原理如下,请配平该反应的离子方程式:________
 ________
________ ________
________ ________
________ ________
________ ________
________ ,
,当有
 生成时,转移电子的数目约为
生成时,转移电子的数目约为
更新时间:2024-02-03 21:19:21
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
【推荐1】锂离子电池是目前具有最高比能量的二次电池。LiFePO4可极大地改善电池体系的安全性能,且具有资源丰富、循环寿命长、环境友好等特点,是锂离子电池正极材料的理想选择。生产LiFePO4的一种工艺流程如图:

在步骤IV中生成了LiFePO4、CO2和H2O(g),则氧化剂与还原剂的物质的量之比为_______ 。

在步骤IV中生成了LiFePO4、CO2和H2O(g),则氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】亚氯酸钠( )主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
)主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下 )受热易分解;
)受热易分解;
②高浓度的 易爆炸。
易爆炸。
(1) 与
与 ,因有强氧化性而用作常用消毒剂,消毒时均被还原为
,因有强氧化性而用作常用消毒剂,消毒时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的_____ 倍(保留小数点后一位)。
(2)反应1涉及的反应方程式为: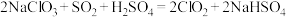 反应中生成的氧化产物与还原产物的个数比为
反应中生成的氧化产物与还原产物的个数比为_____ ;“反应1”需要鼓入空气,空气的作用是_____ 。
(3)“反应2”发生反应的化学方程式:_____ 。“反应2”需要控制反应温度不能过高,温度过高可能导致_____ ;_____ 。
(4)从“母液”中可回收的主要物质是_____ 。
(5)为探究 的氧化性,可以选择下列试剂
的氧化性,可以选择下列试剂_____ 。根据选择的试剂,描述能体现 氧化性的实验现象是
氧化性的实验现象是_____ 。
A.淀粉 溶液 B.酸性高锰酸钾溶液 C.氯水 D.
溶液 B.酸性高锰酸钾溶液 C.氯水 D. 溶液
溶液
(6)针对不同物品的消毒,亚氯酸钠溶液需要稀释到不同的浓度来使用。取含亚氯酸钠18.1g/L的消毒液lmL,加水稀释至100mL,则稀释后的溶液中亚氯酸钠的物质的量浓度为_____  。
。
 )主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下
)主要用于棉纺,造纸业的漂白,也用于食品消毒、水处理等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下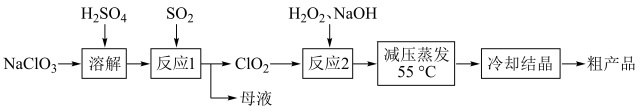
 )受热易分解;
)受热易分解;②高浓度的
 易爆炸。
易爆炸。(1)
 与
与 ,因有强氧化性而用作常用消毒剂,消毒时均被还原为
,因有强氧化性而用作常用消毒剂,消毒时均被还原为 ,则
,则 的消毒能力是等质量的
的消毒能力是等质量的 的
的(2)反应1涉及的反应方程式为:
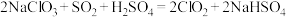 反应中生成的氧化产物与还原产物的个数比为
反应中生成的氧化产物与还原产物的个数比为(3)“反应2”发生反应的化学方程式:
(4)从“母液”中可回收的主要物质是
(5)为探究
 的氧化性,可以选择下列试剂
的氧化性,可以选择下列试剂 氧化性的实验现象是
氧化性的实验现象是A.淀粉
 溶液 B.酸性高锰酸钾溶液 C.氯水 D.
溶液 B.酸性高锰酸钾溶液 C.氯水 D. 溶液
溶液(6)针对不同物品的消毒,亚氯酸钠溶液需要稀释到不同的浓度来使用。取含亚氯酸钠18.1g/L的消毒液lmL,加水稀释至100mL,则稀释后的溶液中亚氯酸钠的物质的量浓度为
 。
。
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂(LiFePO4)。LiFePO4的一种制备方法如图。
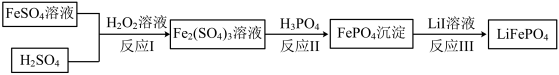
已知:H3PO4能电离出PO 。
。
(1)LiFePO4中,铁元素的化合价为_____ 。
(2)反应I中H2O2的作用是_____ 。
(3)检测反应II中铁离子是否完全反应的操作是_____ 。(离子检验常用的表达方式为:取xx试剂,向其中滴加xx,若出现xx现象,则说明xx结论。)
(4)反应Ⅲ的化学方程式是_____ 。

已知:H3PO4能电离出PO
 。
。(1)LiFePO4中,铁元素的化合价为
(2)反应I中H2O2的作用是
(3)检测反应II中铁离子是否完全反应的操作是
(4)反应Ⅲ的化学方程式是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】以铜为原料可制备应用广泛的氧化亚铜。
方法I.先向CuCl2溶液中通入SO2可得CuCl沉淀,过滤后由CuCl 水解再热分解可得到纳米Cu2O。
(1)向CuCl2溶液中通入SO2可得CuCl 沉淀,该反应的氧化剂与还原剂的物质的量之比为___________ 。
(2)CuCl水解为: CuCl (s) +H2O(1) CuOH (s) +Cl-(aq) +H+ (aq)。该反应的平衡常数K与此温度下Kw、Ksp(CuOH)、 Ksp (CuCl) 的关系为K=
CuOH (s) +Cl-(aq) +H+ (aq)。该反应的平衡常数K与此温度下Kw、Ksp(CuOH)、 Ksp (CuCl) 的关系为K=___________ 。
方法II.电解法
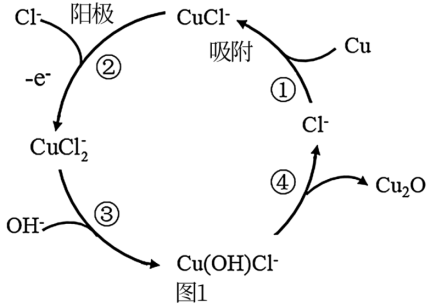
(3)用铜作阳极,钛片作阴极,电解一定浓度的NaCl和NaOH的混合溶液可得到Cu2O,阳极及其溶液中有关转化如图1所示。溶液中③、④二步总反应的离子方程式为:___________ 。
III.氧化亚铜的应用
(4)Cu2O与ZnO组成的催化剂可用于工业上合成甲醇: CO(g) +2H2(g) CH3OH(g) △H =a kJ∙mol−1。按
CH3OH(g) △H =a kJ∙mol−1。按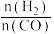 =2:1投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测定CO的平衡转化率与温度、压强的关系如图2所示。
=2:1投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测定CO的平衡转化率与温度、压强的关系如图2所示。

①该反应的△H___________ 0 (填“<”或“>”),图中压强P1、P2、P3由大到小的关系是___________ 。
②恒容密闭容器中,以下描述标志此反应一定达平衡的是___________ 。
A.甲醇的体积分数不再随时间的改变而改变
B.氢气与一氧化碳的浓度比不再改变
C.混合气体的平均摩尔质量不再改变
③当反应达平衡时,温度为T1°C,压强为P3,此时反应的压强平衡常数Kp为___________ 。(用含有P3的代数式表达) (用平衡分压代替平衡浓度计算,分压=总压×体积分数)
方法I.先向CuCl2溶液中通入SO2可得CuCl沉淀,过滤后由CuCl 水解再热分解可得到纳米Cu2O。
(1)向CuCl2溶液中通入SO2可得CuCl 沉淀,该反应的氧化剂与还原剂的物质的量之比为
(2)CuCl水解为: CuCl (s) +H2O(1)
 CuOH (s) +Cl-(aq) +H+ (aq)。该反应的平衡常数K与此温度下Kw、Ksp(CuOH)、 Ksp (CuCl) 的关系为K=
CuOH (s) +Cl-(aq) +H+ (aq)。该反应的平衡常数K与此温度下Kw、Ksp(CuOH)、 Ksp (CuCl) 的关系为K=方法II.电解法
(3)用铜作阳极,钛片作阴极,电解一定浓度的NaCl和NaOH的混合溶液可得到Cu2O,阳极及其溶液中有关转化如图1所示。溶液中③、④二步总反应的离子方程式为:

III.氧化亚铜的应用
(4)Cu2O与ZnO组成的催化剂可用于工业上合成甲醇: CO(g) +2H2(g)
 CH3OH(g) △H =a kJ∙mol−1。按
CH3OH(g) △H =a kJ∙mol−1。按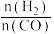 =2:1投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测定CO的平衡转化率与温度、压强的关系如图2所示。
=2:1投料比将H2与CO充入VL恒容密闭容器中,在一定条件下发生反应,测定CO的平衡转化率与温度、压强的关系如图2所示。
①该反应的△H
②恒容密闭容器中,以下描述标志此反应一定达平衡的是
A.甲醇的体积分数不再随时间的改变而改变
B.氢气与一氧化碳的浓度比不再改变
C.混合气体的平均摩尔质量不再改变
③当反应达平衡时,温度为T1°C,压强为P3,此时反应的压强平衡常数Kp为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】镍电池的电极活性材料为多组分合金(主要成分为镍、钴,还含有铝、铁等),可重新回收利用。利用废镍电池资源化生产醋酸钴晶体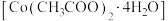 的工艺流程如下。
的工艺流程如下。
②部分金属阳离子沉淀的pH如下表。
请回答下列问题:
(1)“浸取”时可以提高浸取率的操作有___________ (任写1条)。
(2)“调pH”时溶液的pH范围是___________ ,所得滤渣1的主要成分为___________ (填化学式)。
(3)“氧化分离”操作控制溶液pH=2,加入NaClO发生反应的离子方程式为___________ 。
(4)“溶解1”操作中加入H2O2的作用为___________ ,“沉钴”操作过程中发生反应的离子方程式为___________ 。
(5)“溶解2”操作后得到醋酸钴晶体,要使该醋酸钴晶体的纯度更高,所采取的实验操作名称应为___________ 。
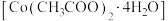 的工艺流程如下。
的工艺流程如下。
②部分金属阳离子沉淀的pH如下表。
| 沉淀物 |  |  | 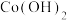 | Co(OH)3 |  |  |
| 开始沉淀pH | 2.2 | 7.4 | 7.6 | 0.1 | 4.0 | 7.6 |
| 完全沉淀pH | 3.2 | 8.9 | 9.2 | 1.1 | 5.2 | 9.2 |
(1)“浸取”时可以提高浸取率的操作有
(2)“调pH”时溶液的pH范围是
(3)“氧化分离”操作控制溶液pH=2,加入NaClO发生反应的离子方程式为
(4)“溶解1”操作中加入H2O2的作用为
(5)“溶解2”操作后得到醋酸钴晶体,要使该醋酸钴晶体的纯度更高,所采取的实验操作名称应为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】某化工厂欲以工业生产废料(金属铁、铝及其氧化物)为原料制取PAFC(聚合氯化铁铝)[AlFe(OH)nCl6-n]m,设计生产流程如下,请回答下列问题:

(1)用10mol·L-1的浓盐酸配制2mol·L-1的稀盐酸500mL,所取浓盐酸的体积_______ mL,所用玻璃仪器除量筒、玻璃棒和胶头滴管外,还有_______ 。
A.500mL容量瓶 B.蒸发皿 C.烧瓶
(2)写出Al2O3和Fe2O3粉末与盐酸反应的离子方程式:_______ 、_______ 。
(3)取少量酸性溶液滴加几滴KSCN试剂,溶液变为_______ 色,证明含有Fe3+。
(4)通入氯气的目的是_______ 。
(5)加入NaOH调节pH时,氢氧化钠不宜过多,生成一种红褐色沉淀,已知Al(OH)3+NaOH=NaAlO2+2H2O。写出溶液中Al3+和Fe3+分别与过量NaOH反应的离子方程式:_______ 、_______ 。

(1)用10mol·L-1的浓盐酸配制2mol·L-1的稀盐酸500mL,所取浓盐酸的体积
A.500mL容量瓶 B.蒸发皿 C.烧瓶
(2)写出Al2O3和Fe2O3粉末与盐酸反应的离子方程式:
(3)取少量酸性溶液滴加几滴KSCN试剂,溶液变为
(4)通入氯气的目的是
(5)加入NaOH调节pH时,氢氧化钠不宜过多,生成一种红褐色沉淀,已知Al(OH)3+NaOH=NaAlO2+2H2O。写出溶液中Al3+和Fe3+分别与过量NaOH反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】电子工业常用FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。从腐蚀废液(主要含FeCl3、FeCl2、CuCl2)中回收铜,并重新获得FeCl3溶液。废液处理流程如下:
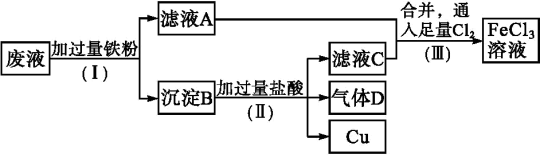
(1)步骤(Ⅰ)中涉及反应的离子方程式:_______ ;_______ 。
(2)沉淀B中主要含有_______ ,气体D是_______ ;
(3)写出步骤(Ⅲ)中生成FeCl3的化学方程式_______ ;
(4)步骤(Ⅲ)中,将氯气换成H2O2也能达到同样的目的,写出H2O2将Fe2+氧化为Fe3+的离子方程式:_______ 。
(5)取FeCl3溶液加入少量KI溶液混合,再滴加淀粉溶液,溶液变蓝。该氧化还原反应的离子方程式为_______ 。
(6)如果向FeCl2溶液中滴加NaOH溶液,现象是_______ ;沉淀变色的原因是_______ (用化学方程式解释)。

(1)步骤(Ⅰ)中涉及反应的离子方程式:
(2)沉淀B中主要含有
(3)写出步骤(Ⅲ)中生成FeCl3的化学方程式
(4)步骤(Ⅲ)中,将氯气换成H2O2也能达到同样的目的,写出H2O2将Fe2+氧化为Fe3+的离子方程式:
(5)取FeCl3溶液加入少量KI溶液混合,再滴加淀粉溶液,溶液变蓝。该氧化还原反应的离子方程式为
(6)如果向FeCl2溶液中滴加NaOH溶液,现象是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐3】一种以赤铁矿(主要含有Fe2O3,含少量Al2O3、CaO等)为原料制备高纯度铁红的流程如下:
(1)“酸浸”时,Al2O3发生反应的离子方程式是___________ 。
(2)“酸浸”后的实验操作名称是___________ ,滤渣的主要成分是___________ 。
(3)“调pH1”不能用氢氧化钠溶液代替氨水的原因是___________ 。
(4)“氧化”时可选用多种氧化剂,若选择氯水,反应的离子方程式为___________ 。
(5)“氧化”后如何检验氧化产物,操作步骤是___________ 。
(6)灼烧时发生反应的化学方程式为___________ 。
(7)写出铁红在生产生活中的一种用途___________ 。
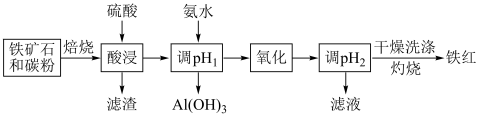
(1)“酸浸”时,Al2O3发生反应的离子方程式是
(2)“酸浸”后的实验操作名称是
(3)“调pH1”不能用氢氧化钠溶液代替氨水的原因是
(4)“氧化”时可选用多种氧化剂,若选择氯水,反应的离子方程式为
(5)“氧化”后如何检验氧化产物,操作步骤是
(6)灼烧时发生反应的化学方程式为
(7)写出铁红在生产生活中的一种用途
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】制取物质、探究物质的性质是学习化学必备的素养之一。
(1)实验室从含碘废液(除水外含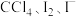 等)中回收碘,其实验流程如下。
等)中回收碘,其实验流程如下。

回答下列问题:
①物质X为_______ 。
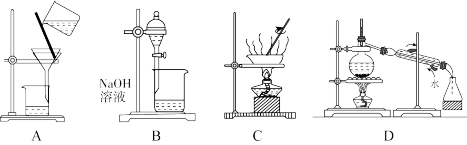
②操作Ⅰ选用的装置为_______ (填标号)。
③含碘废液中加入稍过量的 溶液将
溶液将 还原为
还原为 ,反应的离子方程式为:
,反应的离子方程式为:_______ 。
(2)某研究小组查阅资料知:氧化性的强弱顺序为: 。用如图装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色。
。用如图装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色。

①NaOH溶液的作用是_______ 。
②溶液由黄色最后变为无色,该反应中氧化剂是_______ 。
(3)我国最近成功研制出由Cl2制取ClO2的新方法,其反应的微观过程如图所示:

该反应的化学方程式为_______ 。
(1)实验室从含碘废液(除水外含
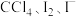 等)中回收碘,其实验流程如下。
等)中回收碘,其实验流程如下。
回答下列问题:
①物质X为
②操作Ⅰ选用的装置为

③含碘废液中加入稍过量的
 溶液将
溶液将 还原为
还原为 ,反应的离子方程式为:
,反应的离子方程式为:(2)某研究小组查阅资料知:氧化性的强弱顺序为:
 。用如图装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色。
。用如图装置对Cl2与KI溶液的反应进行探究,发现通入Cl2一段时间后,KI溶液变为黄色,继续通入Cl2,则溶液黄色变浅,最后变为无色。
①NaOH溶液的作用是
②溶液由黄色最后变为无色,该反应中氧化剂是
(3)我国最近成功研制出由Cl2制取ClO2的新方法,其反应的微观过程如图所示:

该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:

(1)请列举海水淡化的两种方法:___________ 、___________ 。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是___________ 。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为___________ 。
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:

请你参与分析讨论:
①图中仪器B的名称是___________ ;
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是___________ ;
③实验装置气密性良好,要达到提纯溴的目的,操作中控制温度计b为___________ ℃
④C中溶液颜色为___________ ,为除去该产物中残留的Cl2可向其中加入NaBr溶液,反应离子方程式为___________ 。

(1)请列举海水淡化的两种方法:
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为
(4)某化学研究性学习小组为了了解从工业溴中提纯溴的方法,查阅了有关资料知:Br2的沸点为59℃,微溶于水,有毒并有强腐蚀性。他们参观生产过程后,画了如下装置简图:

请你参与分析讨论:
①图中仪器B的名称是
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是
③实验装置气密性良好,要达到提纯溴的目的,操作中控制温度计b为
④C中溶液颜色为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】石墨在材料领域有重要应用。某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质。设计的提纯和综合应用流程如下:

(注:SiCl4的沸点是57.6ºC,金属氯化物的沸点均高于150ºC)
(1)已知1mol石墨完全转化为金刚石需要吸收1.9kJ的能量。请写出石墨转化为金刚石的热化学反应方程式:_________________________ 。
(2)①向反应器中通入Cl2前,需通一段时间的N2。高温反应后,石墨中的氧化物杂质均转变为相应氯化物。80℃冷凝的目的是:_____________________ 。②由活性炭得到气体Ⅱ的化学反应方程式为:_____________________ 。
(3)加入过量NaOH溶液得到溶液IV的离子反应方程式为:_________________________ 。
(4)用化学反应原理解释得到沉淀V的过程中乙酸乙酯和加热的作用:________ 。1kg初级石墨最多可获得V的质量为_______________ kg。

(注:SiCl4的沸点是57.6ºC,金属氯化物的沸点均高于150ºC)
(1)已知1mol石墨完全转化为金刚石需要吸收1.9kJ的能量。请写出石墨转化为金刚石的热化学反应方程式:
(2)①向反应器中通入Cl2前,需通一段时间的N2。高温反应后,石墨中的氧化物杂质均转变为相应氯化物。80℃冷凝的目的是:
(3)加入过量NaOH溶液得到溶液IV的离子反应方程式为:
(4)用化学反应原理解释得到沉淀V的过程中乙酸乙酯和加热的作用:
您最近一年使用:0次

 具有强氧化性,在消毒和果蔬保鲜等方面有广泛应用。下列是制备
具有强氧化性,在消毒和果蔬保鲜等方面有广泛应用。下列是制备
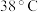 时析出
时析出 时,电子转移的数目是
时,电子转移的数目是 的作用是
的作用是

