将6.4g铜片加入 一定浓度的硝酸溶液中,铜片完全溶解,产生2.24L气体(标准状况),向反应后的溶液中加入
一定浓度的硝酸溶液中,铜片完全溶解,产生2.24L气体(标准状况),向反应后的溶液中加入
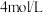
 溶液,溶液中的
溶液,溶液中的 恰好完全沉淀。下列说法正确的是
恰好完全沉淀。下列说法正确的是
 一定浓度的硝酸溶液中,铜片完全溶解,产生2.24L气体(标准状况),向反应后的溶液中加入
一定浓度的硝酸溶液中,铜片完全溶解,产生2.24L气体(标准状况),向反应后的溶液中加入
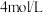
 溶液,溶液中的
溶液,溶液中的 恰好完全沉淀。下列说法正确的是
恰好完全沉淀。下列说法正确的是A.铜与硝酸反应产生的气体为 、 、 |
B.原硝酸溶液的浓度为 |
C.铜片溶解后,溶液中溶质为 |
D.若将产生的气体与足量 混合通入水中充分反应,消耗 混合通入水中充分反应,消耗  |
更新时间:2024-02-01 14:03:05
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】常温下将盛有10 mL NO2和10 mL NO的混合气体的试管倒立于水槽中,并向其中通入O2一段时间后,试管内还剩余2 mL气体,则通入O2的体积为
| A.8mL | B.8.5mL | C.l0mL | D.12mL |
您最近一年使用:0次
【推荐2】H2O2是一种“绿色”试剂,Br2等物质会使较高浓度的H2O2溶液发生催化分解。有人提出反应机理可能有2步,第1步反应为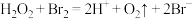 。下列说法正确的是
。下列说法正确的是
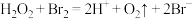 。下列说法正确的是
。下列说法正确的是| A.在第1步反应中,每生成0.1 mol O2,转移0.2 mol电子 |
| B.H2O2可与高锰酸钾溶液反应体现H2O2的氧化性 |
C.机理中第2步反应为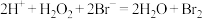 |
| D.若在加入Br2的H2O2溶液中检出Br-,则说明一定发生了第1步反应 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】氨作为化工原料有多种应用。氨水配成的银氨溶液,可用于工业制镜。强碱性条件NaClO和NH3生成火箭燃料N2H4(肼),1mol液态肼完全燃烧生成N2气体和液态水放577kJ的热量。NH3和CO2反应制备尿素[CO(NH2)2],尿素在高温条件下可净化汽车尾气中的NO。下列有关说法正确的是
A.NH3中的键角小于 中的键角 中的键角 |
| B.1molNaClO可得到1molN2H4 |
| C.1mol[Ag(NH3)2]+中有2molσ键 |
| D.净化汽车尾气时氧化产物为CO2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】将12.8 g铜与80 mL 10 mol/L的HNO3充分反应后,溶液中含0.1 mol H+,由此可知
| A.生成的气体只有二氧化氮 |
| B.反应中转移的电子的物质的量为0.4 mol |
| C.被还原的硝酸的物质的量为0.3 mol |
D.反应后溶液中所含 的物质的量为0.4 mol 的物质的量为0.4 mol |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】一种以Pd―Cu为催化剂还原去除水体中 的机理如图a所示;其他条件相同,不同pH时,
的机理如图a所示;其他条件相同,不同pH时, 转化率和不同产物在总还原产物中所占的物质的量的百分比如图b所示。
转化率和不同产物在总还原产物中所占的物质的量的百分比如图b所示。
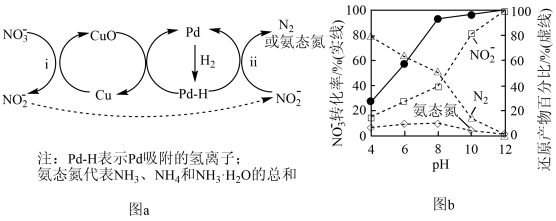
已知:溶液pH会影响Pd对 的吸附,不影响对H的吸附。
的吸附,不影响对H的吸附。
下列说法正确的是
 的机理如图a所示;其他条件相同,不同pH时,
的机理如图a所示;其他条件相同,不同pH时, 转化率和不同产物在总还原产物中所占的物质的量的百分比如图b所示。
转化率和不同产物在总还原产物中所占的物质的量的百分比如图b所示。
已知:溶液pH会影响Pd对
 的吸附,不影响对H的吸附。
的吸附,不影响对H的吸附。下列说法正确的是
A.pH越大,Pd对 的吸附能力越强 的吸附能力越强 |
B.通过调节溶液的pH,可使 更多的转化为 更多的转化为 |
C.反应ii中生成 的离子方程式为 的离子方程式为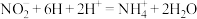 |
D.pH=12时,每处理6.2g ,理论上消耗标准状况下5.6L ,理论上消耗标准状况下5.6L |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】下列实验不能达到预期目的的是
| 序号 | 实验操作 | 实验目的 |
| A | 将Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
| B | 将Cu分别与浓、稀HNO3反应 | 证明稀HNO3氧化性大于浓HNO3 |
| C | 将SO2通入酸性KMnO4溶液中 | 证明SO2具有漂白性 |
| D | 将CO2通入Na2SiO3溶液中 | 比较碳酸、硅酸的酸性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】从离子反应的角度可以认识反应的本质。已知Cu片投入稀 中无现象,向稀硫酸中加入下列物质后Cu片会溶解的是
中无现象,向稀硫酸中加入下列物质后Cu片会溶解的是
 中无现象,向稀硫酸中加入下列物质后Cu片会溶解的是
中无现象,向稀硫酸中加入下列物质后Cu片会溶解的是 | A.NaCl | B. | C. | D.NaOH |
您最近一年使用:0次
【推荐3】为达到实验目的,下列方案设计、现象和结论都正确的是
| 选项 | 实验目的 | 方案设计 | 现象和结论 |
| A | 检验某无色溶液中是否含有 | 取少量该溶液于试管中,加入足量稀盐酸,将产生的气体通入品红溶液中 | 若品红溶液褪色,则该溶液中含有 |
| B | 判断Fe(NO3)2固体是否变质 | 取少量固体溶于蒸馏水,然后滴加少量稀硫酸,再滴入KSCN溶液 | 若溶液变红,则Fe(NO3)2固体已变质 |
| C | 探究酸性:H2SO4>H2SiO3 | 将稀硫酸与Na2CO3混合后产生的气体直接通入硅酸钠溶液中 | 若硅酸钠溶液变浑浊,则硫酸的酸性比硅酸的强 |
| D | 探究浓硫酸的性质 | 向蔗糖中加入几滴蒸馏水,然后再加入浓硫酸 | 若产生疏松多孔的海绵状炭,并放出刺激性气味的气体,则浓硫酸具有脱水性和强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



