电池为我们的生活带来了极大的便利,在生产生活中发挥着重要作用。
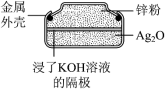
(1)纽扣电池是一种携带方便的微型银锌电池,其结构如图所示:___________ 。
(2)铅蓄电池是传统汽车中使用的启动电源,其工作原理为:PbO2+Pb+2H2SO4 2PbSO4+2H2O。充电时,外接电源负极与
2PbSO4+2H2O。充电时,外接电源负极与___________ (填“Pb”或“PbO2”)连接,溶液的pH会___________ (填“增大”、“减小”或“不变”)。
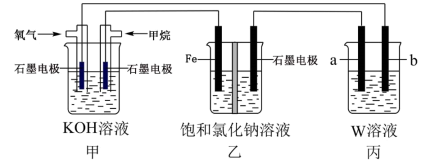
(3)燃料电池是一种把燃料所具有的化学能直接转换成电能的化学装置。用CH4燃料电池连接装置如图所示:___________ 。
②乙池中石墨电极作___________ 极(填“阳”或“阴”),当有1mol甲烷发生反应时,理论上生成Cl2的物质的量为___________ 。
③若丙中要实现铁上镀铜,则电解质溶液W为___________ 溶液,为补充电解质溶液中的阳离子,b电极材料为___________ 。
(1)纽扣电池是一种携带方便的微型银锌电池,其结构如图所示:
(2)铅蓄电池是传统汽车中使用的启动电源,其工作原理为:PbO2+Pb+2H2SO4
 2PbSO4+2H2O。充电时,外接电源负极与
2PbSO4+2H2O。充电时,外接电源负极与(3)燃料电池是一种把燃料所具有的化学能直接转换成电能的化学装置。用CH4燃料电池连接装置如图所示:
②乙池中石墨电极作
③若丙中要实现铁上镀铜,则电解质溶液W为
更新时间:2024-01-20 18:24:19
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知X、Y、Z、W、M、N为短周期主族元素且原子序数依次增大,W和M同主族,Z的最高价氧化物对应的水化物能与其气态氢化物发生化合反应生成盐为Q,Y是形成化合物种类最多的元素,X2W是常见的液态物质,元素R的焰色反应为紫色(透过蓝色钴玻璃),请回答下列问题:
(1)R元素在周期表中的位置:_______ ,其原子结构示意图为:_______ 。
(2)Q所含有的化学键类型是_______ ,X2W2的电子式:_______ 。M、N、R简单离子半径由大到小的顺序:_______ 。
(3)写出一个可证明M和N非金属性强弱的离子反应方程式:_______ 。
(4)以稀X2MW4溶液作电解质溶液,石墨作电极,X的单质和W的双原子分子组成燃料电池,电池工作时,正极的电极反应式为_______ 。
(1)R元素在周期表中的位置:
(2)Q所含有的化学键类型是
(3)写出一个可证明M和N非金属性强弱的离子反应方程式:
(4)以稀X2MW4溶液作电解质溶液,石墨作电极,X的单质和W的双原子分子组成燃料电池,电池工作时,正极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】填空。
(1)在一个容积不变的 密闭容器中加入
密闭容器中加入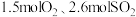 和合适的催化剂,发生反应
和合适的催化剂,发生反应 ,反应温度对
,反应温度对 的平衡转化率[
的平衡转化率[ 的平衡转化率
的平衡转化率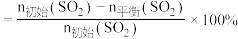 ]和催化剂的催化效率的影响如下图所示。
]和催化剂的催化效率的影响如下图所示。
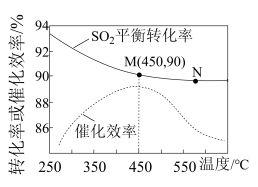
①在催化剂作用下合成 的最佳温度为
的最佳温度为___________ (填标号)。
A.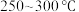 B.
B.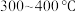 C.
C.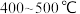
② 时,若经过
时,若经过 反应达到平衡,则
反应达到平衡,则 内用
内用 表示的平均反应速率为
表示的平均反应速率为________ 。
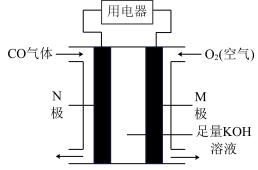
(2)某实验小组结合原电池原理设计了如图所示的燃料电池装置, 极为
极为___________ 极(填“正”或“负”),M极的电极反应式为___________ 。
(3) 气体在一定条件下可被氧气氧化,反应的化学方程式为
气体在一定条件下可被氧气氧化,反应的化学方程式为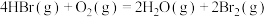 。已知:键能是指气态分子中
。已知:键能是指气态分子中 化学键断裂成气态原子所吸收的能量,试利用下表中键能数据计算上述反应中有
化学键断裂成气态原子所吸收的能量,试利用下表中键能数据计算上述反应中有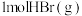 被氧化时,该反应
被氧化时,该反应___________ (填“吸收”或“放出”)的能量为___________ 。
(4)向温度、体积均相同的两个恒容密闭容器中均充入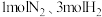 ,在不同催化剂下发生反应:
,在不同催化剂下发生反应: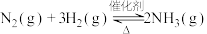 ,测得不同催化剂下氨气浓度随时间的变化如下表所示。
,测得不同催化剂下氨气浓度随时间的变化如下表所示。
对比可知,催化效果较好的是催化剂___________ 除催化剂外,对于该反应,请写出一种加快反应速率的方法:___________ 。
(1)在一个容积不变的
 密闭容器中加入
密闭容器中加入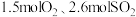 和合适的催化剂,发生反应
和合适的催化剂,发生反应 ,反应温度对
,反应温度对 的平衡转化率[
的平衡转化率[ 的平衡转化率
的平衡转化率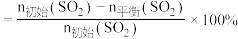 ]和催化剂的催化效率的影响如下图所示。
]和催化剂的催化效率的影响如下图所示。
①在催化剂作用下合成
 的最佳温度为
的最佳温度为A.
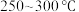 B.
B.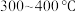 C.
C.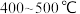
②
 时,若经过
时,若经过 反应达到平衡,则
反应达到平衡,则 内用
内用 表示的平均反应速率为
表示的平均反应速率为(2)某实验小组结合原电池原理设计了如图所示的燃料电池装置,
 极为
极为
(3)
 气体在一定条件下可被氧气氧化,反应的化学方程式为
气体在一定条件下可被氧气氧化,反应的化学方程式为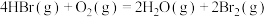 。已知:键能是指气态分子中
。已知:键能是指气态分子中 化学键断裂成气态原子所吸收的能量,试利用下表中键能数据计算上述反应中有
化学键断裂成气态原子所吸收的能量,试利用下表中键能数据计算上述反应中有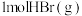 被氧化时,该反应
被氧化时,该反应| 共价键 |  |  |  |  |
键能 | 366 | 498 | 464 | 193 |
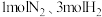 ,在不同催化剂下发生反应:
,在不同催化剂下发生反应: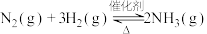 ,测得不同催化剂下氨气浓度随时间的变化如下表所示。
,测得不同催化剂下氨气浓度随时间的变化如下表所示。| 编号 | 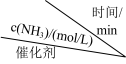 | 0 | 20 | 40 | 60 | 80 |
| ① | 催化剂1 | 0.00 | 0.40 | 0.78 | 1.13 | 1.44 |
| ② | 催化剂2 | 0.00 | 0.20 | 0.38 | 0.54 | 0.67 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】锂被誉为“高能金属”,以废旧锂离子电池的正极材料(主要含有 及少量
及少量 、
、 等)为原料制备
等)为原料制备 的一种工艺流程如图1所示。
的一种工艺流程如图1所示。
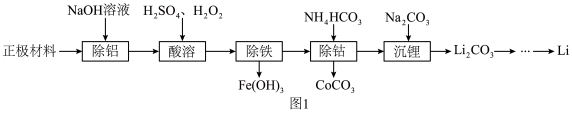
回答下列问题:
(1)“除铝”时所得溶液中含铝微粒为___________ (填化学式,下同)。
(2)“酸溶”时,若用浓盐酸代替 和
和 的混合液,则有一种黄绿色气体生成,该反应的还原剂为
的混合液,则有一种黄绿色气体生成,该反应的还原剂为___________ 。
(3)该流程中涉及过滤,实验室过滤时玻璃棒的作用为___________ 。
(4)写出“除钴”过程中发生反应的离子方程式:___________ 。
(5)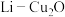 电池是近年来发明的一种低成本高效电池,该电池首先通过
电池是近年来发明的一种低成本高效电池,该电池首先通过 与
与 反应产生
反应产生 ,然后通过还原反应再生,电池结构如图2所示。
,然后通过还原反应再生,电池结构如图2所示。
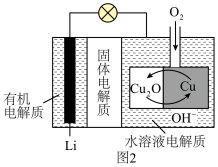
①正极反应式为___________ 。
②每转移 电子,理论上消耗
电子,理论上消耗___________ 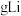 。
。
(6)锂—空气二次电池的反应原理为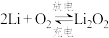 ,其放电时的工作原理如图3所示。
,其放电时的工作原理如图3所示。
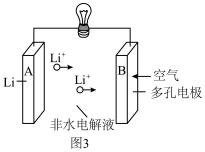
①充电时阳极电极反应式为___________ 。
②放电时,若B极增重 ,则通过外电路电子的物质的量为
,则通过外电路电子的物质的量为___________  。
。
 及少量
及少量 、
、 等)为原料制备
等)为原料制备 的一种工艺流程如图1所示。
的一种工艺流程如图1所示。
回答下列问题:
(1)“除铝”时所得溶液中含铝微粒为
(2)“酸溶”时,若用浓盐酸代替
 和
和 的混合液,则有一种黄绿色气体生成,该反应的还原剂为
的混合液,则有一种黄绿色气体生成,该反应的还原剂为(3)该流程中涉及过滤,实验室过滤时玻璃棒的作用为
(4)写出“除钴”过程中发生反应的离子方程式:
(5)
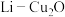 电池是近年来发明的一种低成本高效电池,该电池首先通过
电池是近年来发明的一种低成本高效电池,该电池首先通过 与
与 反应产生
反应产生 ,然后通过还原反应再生,电池结构如图2所示。
,然后通过还原反应再生,电池结构如图2所示。
①正极反应式为
②每转移
 电子,理论上消耗
电子,理论上消耗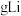 。
。(6)锂—空气二次电池的反应原理为
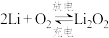 ,其放电时的工作原理如图3所示。
,其放电时的工作原理如图3所示。
①充电时阳极电极反应式为
②放电时,若B极增重
 ,则通过外电路电子的物质的量为
,则通过外电路电子的物质的量为 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】降低能耗是氯碱工业发展的重要方向。
(1)我国利用氯碱厂生产的 作为电池燃料,再将电池应用于氯碱工业,原理如图,a、b、c、d均为石墨电极。
作为电池燃料,再将电池应用于氯碱工业,原理如图,a、b、c、d均为石墨电极。
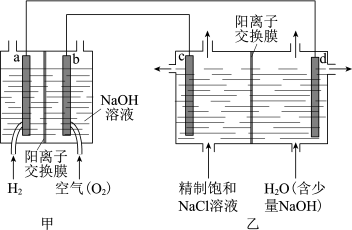

①乙装置中电解饱和 溶液的化学方程式为
溶液的化学方程式为_______ ;反应一段时间后,d极产生 气体时,乙装置中转移电子
气体时,乙装置中转移电子_______  。
。
②下列说法正确的是_______ (填字母序号)。
A.甲装置可实现化学能向电能的转化
B.甲装置中 透过阳离子交换膜向a极移动
透过阳离子交换膜向a极移动
C.乙装置中c极一侧流出的是浓盐水
(2)①金属腐蚀一般可分为化学腐蚀和电化学腐蚀.炒过菜的铁锅未及时清洗容易发生电化学腐蚀而生锈.请写出铁锅生锈过程的正极反应式:_______ 。
②图丙所示方案也可以减缓铁闸门的腐蚀速率,则铁闸门应连接直流电源的_______ 极。
(3)蓄电池是一种可以反复充电、放电的装置.有一种蓄电池在充电和放电时发生的反应是: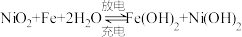 。
。
①若此蓄电池放电时,该电池某一电极发生还原反应的物质是_______ (填序号)。
A.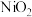 B.
B. C.
C. D.
D.
②该电池放电时,正极附近溶液的pH_______ (填增大、减小、不变)。
③充电时该电池阴极的电极反应式_______ 。
(1)我国利用氯碱厂生产的
 作为电池燃料,再将电池应用于氯碱工业,原理如图,a、b、c、d均为石墨电极。
作为电池燃料,再将电池应用于氯碱工业,原理如图,a、b、c、d均为石墨电极。

①乙装置中电解饱和
 溶液的化学方程式为
溶液的化学方程式为 气体时,乙装置中转移电子
气体时,乙装置中转移电子 。
。②下列说法正确的是
A.甲装置可实现化学能向电能的转化
B.甲装置中
 透过阳离子交换膜向a极移动
透过阳离子交换膜向a极移动C.乙装置中c极一侧流出的是浓盐水
(2)①金属腐蚀一般可分为化学腐蚀和电化学腐蚀.炒过菜的铁锅未及时清洗容易发生电化学腐蚀而生锈.请写出铁锅生锈过程的正极反应式:
②图丙所示方案也可以减缓铁闸门的腐蚀速率,则铁闸门应连接直流电源的
(3)蓄电池是一种可以反复充电、放电的装置.有一种蓄电池在充电和放电时发生的反应是:
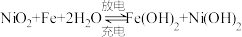 。
。①若此蓄电池放电时,该电池某一电极发生还原反应的物质是
A.
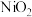 B.
B. C.
C. D.
D.
②该电池放电时,正极附近溶液的pH
③充电时该电池阴极的电极反应式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】下图是一个电化学过程的示意图,请按要求填空:

(1)通入CH3CH2OH的电极名称是______________ ,B电极的名称是_____________ 。
(2)通入CH3CH2OH一极的电极反应式为_____________________________________ 。
(3)乙池中总反应的化学方程式为___________________________________________ 。
(4)当乙池中A(Fe)极的质量增加12.8g时,甲池中消耗O2_______ mL(标况下)
(5)火箭发射时可用肼(N2H4)为燃料,以二氧化氮做氧化剂,它们相互反应生成氮气和水蒸气。
①写出在碱性条件下负极反应式为:___________________________________________ 。
②已知:N2(g)+2O2(g)=2NO2(g),ΔH=+67.7 kJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g),ΔH=-534 kJ·mol-1,则N2H4和NO2反应的热化学方程式__________________________________________ 。

(1)通入CH3CH2OH的电极名称是
(2)通入CH3CH2OH一极的电极反应式为
(3)乙池中总反应的化学方程式为
(4)当乙池中A(Fe)极的质量增加12.8g时,甲池中消耗O2
(5)火箭发射时可用肼(N2H4)为燃料,以二氧化氮做氧化剂,它们相互反应生成氮气和水蒸气。
①写出在碱性条件下负极反应式为:
②已知:N2(g)+2O2(g)=2NO2(g),ΔH=+67.7 kJ·mol-1;N2H4(g)+O2(g)=N2(g)+2H2O(g),ΔH=-534 kJ·mol-1,则N2H4和NO2反应的热化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.利用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂,以下为草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:
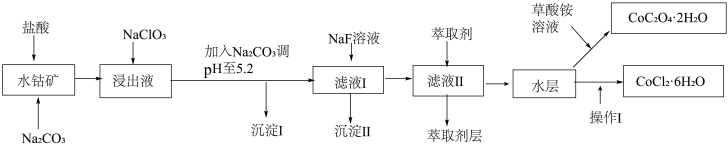
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等。
②沉淀Ⅰ中只含有两种沉淀。
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)浸出过程中加入Na2SO3目的是______ 。
(2)NaClO3在浸出液中发生反应的离子方程式为______ 。
(3)加入Na2CO3调pH至5.2,目的是______ ;萃取剂层含锰元素,则沉淀Ⅱ的主要成分为______ 。
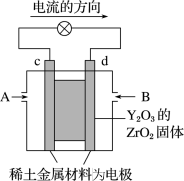
Ⅱ.科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。图甲所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-(O2+4e-=2O2-)
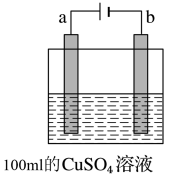
甲 乙
(1)d电极上的电极反应式为______ ;
(2)图乙是用惰性电极电解100mL 0.5mol•L-1 CuSO4溶液,a电极上的电极反应式为______ ;若a电极产生56mL(标准状况)气体,则所得溶液的pH=______ (不考虑溶液体积变化及离子的水解),若要使电解质溶液恢复到电解前的状态,可加入______ (选填字母序号)。
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等。
②沉淀Ⅰ中只含有两种沉淀。
③流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入Na2SO3目的是
(2)NaClO3在浸出液中发生反应的离子方程式为
(3)加入Na2CO3调pH至5.2,目的是
Ⅱ.科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。图甲所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-(O2+4e-=2O2-)


甲 乙
(1)d电极上的电极反应式为
(2)图乙是用惰性电极电解100mL 0.5mol•L-1 CuSO4溶液,a电极上的电极反应式为
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3
您最近一年使用:0次



