合金已成为飞机制造、化工生产等行业的重要材料。某研究性学习小组的同学,为测定某含镁40%~60%的铝镁合金(不含其他元素) 中铝的质量分数,设计下列两种不同的实验方案进行探究。回答下列问题。
方案一:
(1)研究小组同学准备用 NaOH 固体配制240mL1.0 的NaOH溶液。
的NaOH溶液。
①本实验必须用到的玻璃仪器有:量筒、胶头滴管、烧杯、___________ 。
②要配制出此溶液,研究小组同学应用托盘天平称出___________ gNaOH。
③在配制过程中,小组同学的其他操作都是正确的,但下列操作中会引起所配制溶液浓度偏高的是___________ (填字母)。
A. NaOH固体在称量前已部分变质
B. 有少量NaOH溶液残留在烧杯里
C. 定容时,俯视容量瓶的刻度线
D. 定容摇匀后,发现溶液凹液面最低处低于刻度线,用胶头滴管补水至刻度线
(2)称取8.1g 铝镁合金粉末样品,溶于VmL1.0 的NaOH溶液中,充分反应,过滤、洗涤、干燥、称量固体,该步骤中若未洗涤固体,测得铝的质量分数将
的NaOH溶液中,充分反应,过滤、洗涤、干燥、称量固体,该步骤中若未洗涤固体,测得铝的质量分数将___________ (选填“偏高” “偏低”或“不受影响”)。
方案二:
将5.1g 铝镁合金与足量稀硫酸反应,测定生成气体的体积。
(3)同学们拟选用下图实验装置完成实验:
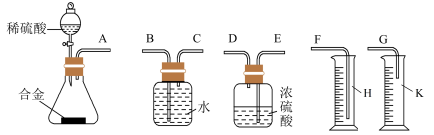
①你认为最简易的装置的连接顺序是:A接______,_______接______,______接______(填接口字母,可不填满)。___________
②实验结束时,在测量实验中生成氢气的体积时,你认为合理的是___________ (填字母)。
A.待实验装置冷却后再读数
B.上下移动量筒H,使其中液面与广口瓶中液面相平
C.视线与凹液面的最低点水平相切,读取量筒中水的体积
D.上下移动量筒K,使其中液面与广口瓶中液面相平
(4)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:
①稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;
②实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小,于是他们设计了如图所示的实验装置:
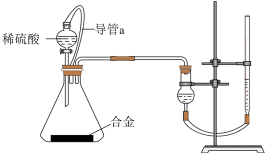
①装置中导管a的作用是___________
②实验后测得生成的氢气在标准状况下的体积为5.6 L,则铝的质量分数为___________ (请保留1位小数) 。
方案一:
(1)研究小组同学准备用 NaOH 固体配制240mL1.0
 的NaOH溶液。
的NaOH溶液。①本实验必须用到的玻璃仪器有:量筒、胶头滴管、烧杯、
②要配制出此溶液,研究小组同学应用托盘天平称出
③在配制过程中,小组同学的其他操作都是正确的,但下列操作中会引起所配制溶液浓度偏高的是
A. NaOH固体在称量前已部分变质
B. 有少量NaOH溶液残留在烧杯里
C. 定容时,俯视容量瓶的刻度线
D. 定容摇匀后,发现溶液凹液面最低处低于刻度线,用胶头滴管补水至刻度线
(2)称取8.1g 铝镁合金粉末样品,溶于VmL1.0
 的NaOH溶液中,充分反应,过滤、洗涤、干燥、称量固体,该步骤中若未洗涤固体,测得铝的质量分数将
的NaOH溶液中,充分反应,过滤、洗涤、干燥、称量固体,该步骤中若未洗涤固体,测得铝的质量分数将方案二:
将5.1g 铝镁合金与足量稀硫酸反应,测定生成气体的体积。
(3)同学们拟选用下图实验装置完成实验:

①你认为最简易的装置的连接顺序是:A接______,_______接______,______接______(填接口字母,可不填满)。
②实验结束时,在测量实验中生成氢气的体积时,你认为合理的是
A.待实验装置冷却后再读数
B.上下移动量筒H,使其中液面与广口瓶中液面相平
C.视线与凹液面的最低点水平相切,读取量筒中水的体积
D.上下移动量筒K,使其中液面与广口瓶中液面相平
(4)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:
①稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;
②实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小,于是他们设计了如图所示的实验装置:

①装置中导管a的作用是
②实验后测得生成的氢气在标准状况下的体积为5.6 L,则铝的质量分数为
更新时间:2024-01-27 11:25:35
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】镁铝合金具有良好的强度、刚性、优良的电磁屏蔽性和导热性,使之成为笔记本电脑和轻薄手机的首选外壳材料。为测定某手机外壳镁铝合金中镁和铝的含最,并回收镁铝,某实验小组设计如下实验方案。
①除去手机外壳的涂层,剪其中一小块,称取其质量;
②组装仪器,检查气密性,用足盘稀盐酸溶解合金;
③测量产生气体的体积,计算结果;
④利用下列流程,从溶解合金后的溶液中回收分离镁铝。

(1)请利用下图给定的仪器组成一套实验装置(每个仪器只能使用一次,可不选用)。各种仪器连接的先后顺序(用小写字母表示)_______

(2)除了测定产生气体的体积外,还应测定_______ 。
(3)回收流程中,操作I需要的玻璃仪器有烧杯、玻璃棒和_______ ,为保证回收产品的纯度,操作I后应_______ 。
(4)滤液b的溶质是_______ (填化学式),试剂X是_______ 。
(5)向滤渣a中加入盐酸,产物是_______ (填化学式),若从晶体中获得金属,应进行的操作是_______ 。
(6)若从除去涂层的手机壳上取样品mg加入足量盐酸后,测得产生的气体nL,实验条件下的气体摩尔体积为VmL/mol,则合金中Mg的质量为________ g。
①除去手机外壳的涂层,剪其中一小块,称取其质量;
②组装仪器,检查气密性,用足盘稀盐酸溶解合金;
③测量产生气体的体积,计算结果;
④利用下列流程,从溶解合金后的溶液中回收分离镁铝。

(1)请利用下图给定的仪器组成一套实验装置(每个仪器只能使用一次,可不选用)。各种仪器连接的先后顺序(用小写字母表示)

(2)除了测定产生气体的体积外,还应测定
(3)回收流程中,操作I需要的玻璃仪器有烧杯、玻璃棒和
(4)滤液b的溶质是
(5)向滤渣a中加入盐酸,产物是
(6)若从除去涂层的手机壳上取样品mg加入足量盐酸后,测得产生的气体nL,实验条件下的气体摩尔体积为VmL/mol,则合金中Mg的质量为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】理想气体状态方程 ,是描述理想气体的物质的量与其体积、分压、温度间关系的状态方程。其中气体常数R可通过如下实验测定。
,是描述理想气体的物质的量与其体积、分压、温度间关系的状态方程。其中气体常数R可通过如下实验测定。

(1)组装仪器:简易量气装置的量气管可用_______ (填一种常用仪器名称)代替;组装完成后,须进行_______ (填操作名称)。
(2)装药品:向反应管内加入足量的稀硫酸,_______ (填“能”或“不能”)用稀硝酸代替稀硫酸,理由是_______ ;铝片打磨后称量,再用铜丝缠绕并放在反应管口,用铜丝缠绕铝片的目的是_______ 。
反应:读取量气管的起始读数后,移动反应管,使铝片滑入稀硫酸中。
(3)测量体积:待反应管内溶液无明显气泡产生后,对量气管进行第2次读数。读数时,应注意_______ 、_______ (回答2点)。
(4)数据计算:实验数据如下表所示。
甲同学用以上数据代入公式进行计算,得到气体常数
_______  (用计算式表示)。
(用计算式表示)。
(5)误差分析:通过计算发现,气体常数R的测量值稍大于理论值,若排除实验过程的操作误差,导致测量值偏大可能的原因是_______ 。
 ,是描述理想气体的物质的量与其体积、分压、温度间关系的状态方程。其中气体常数R可通过如下实验测定。
,是描述理想气体的物质的量与其体积、分压、温度间关系的状态方程。其中气体常数R可通过如下实验测定。
(1)组装仪器:简易量气装置的量气管可用
(2)装药品:向反应管内加入足量的稀硫酸,
反应:读取量气管的起始读数后,移动反应管,使铝片滑入稀硫酸中。
(3)测量体积:待反应管内溶液无明显气泡产生后,对量气管进行第2次读数。读数时,应注意
(4)数据计算:实验数据如下表所示。
| 铝片质量 | 反应前量气管读数 | 反应后反应后量气管读数 | 室内温度 | 室内压强 |
| 0.0270g | 0.50mL | 38.90mL | 295.4K |  |

 (用计算式表示)。
(用计算式表示)。(5)误差分析:通过计算发现,气体常数R的测量值稍大于理论值,若排除实验过程的操作误差,导致测量值偏大可能的原因是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】以冶铝的废弃物铝灰为原料制取超细α—氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:

(1)为了提高酸浸的速率,可以采取的方法有:___________ (填一种方法即可)。
(2)铝灰中氧化铝与硫酸反应的化学方程式为___________ 。
(3)图中“滤渣”的主要成分为___________ (填化学式),其与氢氧化钠溶液反应的离子方程式为___________ 。
(4)检验“沉铁”是否完全的操作:___________ 。
(5)煅烧硫酸铝铵晶体,发生的主要反应为: ,将产生的气体通过下图所示的装置:
,将产生的气体通过下图所示的装置:
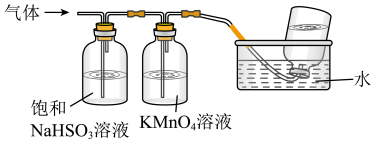
①集气瓶中收集到的气体是___________ (填化学式)。
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有___________ (填化学式)。
③KMnO4溶液褪色( 还原为Mn2+),发生反应的离子方程式为
还原为Mn2+),发生反应的离子方程式为___________ 。

(1)为了提高酸浸的速率,可以采取的方法有:
(2)铝灰中氧化铝与硫酸反应的化学方程式为
(3)图中“滤渣”的主要成分为
(4)检验“沉铁”是否完全的操作:
(5)煅烧硫酸铝铵晶体,发生的主要反应为:
 ,将产生的气体通过下图所示的装置:
,将产生的气体通过下图所示的装置:
①集气瓶中收集到的气体是
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有
③KMnO4溶液褪色(
 还原为Mn2+),发生反应的离子方程式为
还原为Mn2+),发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】下图表示有关物质之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物(反应条件图中已省略)

(1)A,D代表的物质分别为:________ ,________ (填化学式);
(2)反应①中的C,D均过量,该反应的化学方程式是____________________________________ ;
(3)反应②中,若B与F物质的量之比为4∶3,G,H分别是_______ ,_______ (填化学式);其物质的量之比为__________ .
(4)反应③产物中K的化学式为____________ ;④的离子方程式为_____________________________ .

(1)A,D代表的物质分别为:
(2)反应①中的C,D均过量,该反应的化学方程式是
(3)反应②中,若B与F物质的量之比为4∶3,G,H分别是
(4)反应③产物中K的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】从废旧磷酸铁锂电池的正极材料(含LiFePO4、石墨粉和铝箔等)中综合回收锂、铁和磷等的工艺流程如图所示:
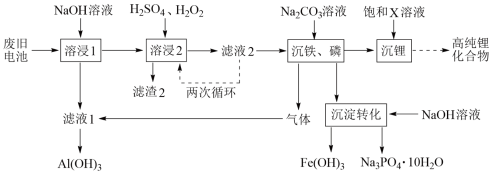
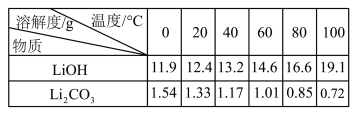
回答下列问题:
(1)“溶浸1”中铝溶解的化学方程式为___________________________ 。
(2)完成“溶浸2”反应的离子方程式___________________________ :
 LiFePO4+
LiFePO4+ H2O2+
H2O2+ =
= Li++
Li++ +
+ H2PO4-+
H2PO4-+ H2O
H2O
(3)“滤渣2”的主要成分是_______________ 。
(4)“滤液2”循环两次的目的是___________________________ 。
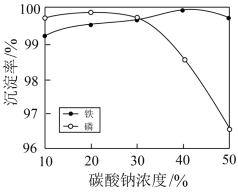
(5)“沉铁、磷”时,析出FePO4沉淀,反应的离子方程式为_______________________ 。实验中,铁、磷的沉淀率结果如图所示。碳酸钠浓度大于30%后,铁沉淀率仍然升高,磷沉淀率明显降低,其可能原因是___________________________ 。
(6)为了充分沉淀,“沉锂”时所用的X和适宜温度是___ (填标号)。
A.NaOH20-40℃B.NaOH80-100℃
C.Na2CO320-40℃D.Na2CO360-80℃


回答下列问题:
(1)“溶浸1”中铝溶解的化学方程式为
(2)完成“溶浸2”反应的离子方程式
 LiFePO4+
LiFePO4+ H2O2+
H2O2+ =
= Li++
Li++ +
+ H2PO4-+
H2PO4-+ H2O
H2O(3)“滤渣2”的主要成分是
(4)“滤液2”循环两次的目的是
(5)“沉铁、磷”时,析出FePO4沉淀,反应的离子方程式为

(6)为了充分沉淀,“沉锂”时所用的X和适宜温度是
A.NaOH20-40℃B.NaOH80-100℃
C.Na2CO320-40℃D.Na2CO360-80℃
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知:
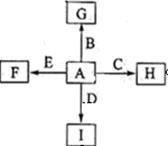
①反应C+G B+H能放出大量的热,G是红综色固体粉末;
B+H能放出大量的热,G是红综色固体粉末;
②I是一种常见的温室气体,它和E可以发生反应:2E+I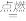 2F+D,F中的E元素的质量分数为60%.
2F+D,F中的E元素的质量分数为60%.
回答问题:
(1)①中反应的化学方程式为______________________________ ;
(2)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,至少需要铜粉__________ 克;
(3)C与过量NaOH溶液反应的离子方程式为________________________________ ,
反应后的溶液与过量的化合物I反应的离子方程式为_______________________ ;
(4)E与I反应的化学方程式为______________________________ ;
(5)写出H物质在工业上的一种用途___________________ ;
(6)将一定量的B完全溶于过量盐酸中,然后通入0.005mol Cl2,再加入0.01mol重铬酸钾晶体(K2Cr2O7),恰好使溶液中B2+全部转化为B3+,铬元素本身被还原为+3价铬离子。通过计算确定原B的物质的量为______ 。
A.0.01mol B.0.03mol C.0.04mol D.0.07mol

①反应C+G
 B+H能放出大量的热,G是红综色固体粉末;
B+H能放出大量的热,G是红综色固体粉末;②I是一种常见的温室气体,它和E可以发生反应:2E+I
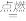 2F+D,F中的E元素的质量分数为60%.
2F+D,F中的E元素的质量分数为60%.回答问题:
(1)①中反应的化学方程式为
(2)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,至少需要铜粉
(3)C与过量NaOH溶液反应的离子方程式为
反应后的溶液与过量的化合物I反应的离子方程式为
(4)E与I反应的化学方程式为
(5)写出H物质在工业上的一种用途
(6)将一定量的B完全溶于过量盐酸中,然后通入0.005mol Cl2,再加入0.01mol重铬酸钾晶体(K2Cr2O7),恰好使溶液中B2+全部转化为B3+,铬元素本身被还原为+3价铬离子。通过计算确定原B的物质的量为
A.0.01mol B.0.03mol C.0.04mol D.0.07mol
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】Ⅰ.下列实验操作或对实验事实的描述正确的是____________ (填序号)
①实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉;
②配制一定浓度的溶液时,俯视容量瓶的刻度线,会使配制的浓度偏高;实验室测定中和热时,过早读数会使测定结果偏低;
③试管中加入少量淀粉,再加入一定量稀硫酸,加热3-4分钟,然后加入银氨溶液,片刻后管壁上有“银镜”出现
④分别向体积和pH均相同的盐酸和醋酸中滴加等浓度的氢氧化钠溶液,完全中和时消耗的氢氧化钠溶液的体积一样多
⑤向NaOH溶液、KSCN溶液、沸腾的蒸馏水中分别滴加饱和的FeCl3溶液得到的分散系依次为:浊液、溶液、胶体
Ⅱ.某研究性学习小组利用下图所示装置研究乙醇与氧化铁的反应,请回答下列问题:

(1)装置中试管B的作用是____________________________ 。
(2)实验中可观察到石英管A中的现象为_______________________________ 。
(3)反应停止后,取出试管C在酒精灯上加热至沸腾,可观察到有红色沉淀产生。写出该反应的化学方程式________________________________ 。
(4)为了测定反应后石英管A左侧固体中铁元素的含量,进行如下实验:
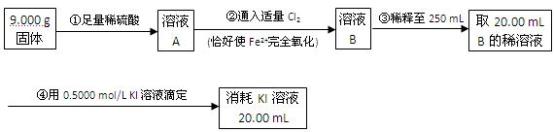
(i)步骤③中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、__________________ 。
(ii)下列有关步骤④的操作中说法正确的是__________________________ 。
a.滴定过程中可利用淀粉溶液作为指示剂
b.滴定管用蒸馏水洗涤后可以直接装液
c.锥形瓶不需要用待测夜润洗
d.滴定过程中,眼睛注视滴定管中液面变化
e.滴定结束后,30 s内溶液不恢复原来的颜色,再读数
(iii)由框图中数据计算,可得石英管A左侧固体中铁元素的百分含量为_______ 。
①实验室配制氯化亚铁溶液时,将氯化亚铁先溶解在盐酸中,然后用蒸馏水稀释并加入少量铁粉;
②配制一定浓度的溶液时,俯视容量瓶的刻度线,会使配制的浓度偏高;实验室测定中和热时,过早读数会使测定结果偏低;
③试管中加入少量淀粉,再加入一定量稀硫酸,加热3-4分钟,然后加入银氨溶液,片刻后管壁上有“银镜”出现
④分别向体积和pH均相同的盐酸和醋酸中滴加等浓度的氢氧化钠溶液,完全中和时消耗的氢氧化钠溶液的体积一样多
⑤向NaOH溶液、KSCN溶液、沸腾的蒸馏水中分别滴加饱和的FeCl3溶液得到的分散系依次为:浊液、溶液、胶体
Ⅱ.某研究性学习小组利用下图所示装置研究乙醇与氧化铁的反应,请回答下列问题:

(1)装置中试管B的作用是
(2)实验中可观察到石英管A中的现象为
(3)反应停止后,取出试管C在酒精灯上加热至沸腾,可观察到有红色沉淀产生。写出该反应的化学方程式
(4)为了测定反应后石英管A左侧固体中铁元素的含量,进行如下实验:

(i)步骤③中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、
(ii)下列有关步骤④的操作中说法正确的是
a.滴定过程中可利用淀粉溶液作为指示剂
b.滴定管用蒸馏水洗涤后可以直接装液
c.锥形瓶不需要用待测夜润洗
d.滴定过程中,眼睛注视滴定管中液面变化
e.滴定结束后,30 s内溶液不恢复原来的颜色,再读数
(iii)由框图中数据计算,可得石英管A左侧固体中铁元素的百分含量为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】草酸晶体的组成可表示为H2C2O4·xH2O,为测定x值,进行下列实验。
①称取m g草酸晶体,配成100.0 mL溶液。
②取25.0 mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol·L-1 KMnO4溶液滴定。滴定时,所发生反应为:2KMnO4+5H2C2O4+3H2SO4===K2SO4+10CO2↑+2MnSO4+8H2O
请回答下列问题:
(1)实验①中为了配制准确浓度的草酸溶液,所需要的实验仪器主要有:天平(含砝码)、烧杯、药匙、胶头滴管和____________ 、____________ 。
(2)在实验②中,滴定时KMnO4溶液应装在________ 式滴定管中,锥形瓶中________ (填“需要”或 “不需要”)滴加指示剂。
(3)在滴定过程中,目光应注视______________________ 。
(4)某学生实验时用草酸润洗了锥形瓶测定的浓度会偏_____ 。(填“偏高”、“偏低”或“无影响”)
①称取m g草酸晶体,配成100.0 mL溶液。
②取25.0 mL所配草酸溶液置于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol·L-1 KMnO4溶液滴定。滴定时,所发生反应为:2KMnO4+5H2C2O4+3H2SO4===K2SO4+10CO2↑+2MnSO4+8H2O
请回答下列问题:
(1)实验①中为了配制准确浓度的草酸溶液,所需要的实验仪器主要有:天平(含砝码)、烧杯、药匙、胶头滴管和
(2)在实验②中,滴定时KMnO4溶液应装在
(3)在滴定过程中,目光应注视
(4)某学生实验时用草酸润洗了锥形瓶测定的浓度会偏
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】(NH4)2Fe(SO4)2比FeSO4稳定,其标准溶液是定量实验中的常用试剂。
(1) 实验室用(NH4)2Fe(SO4)2固体配制一定浓度的(NH4)2Fe(SO4)2标准溶液。
①配制溶液时,需要使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的__________ (填字母代号)

②若要配制0.100 mol·L-1的(NH4)2Fe(SO4)2标准溶液250ml,需称取(NH4)2Fe(SO4)2____ g
③若在配制过程中,烧杯中的(NH4)2Fe(SO4)2溶液有少量溅出,则所得溶液浓度_______ ;若在定容时,俯视液面,则所得溶液浓度_____ 。(填“偏高”、“偏低”、“无影响”)
(2)能电离出两种阳离子的盐称为复盐,下列物质中属于复盐的有_______ 。
a.KAl(SO4)2 b.KAlO2 c.NH4Al(SO4)2 d.[Ag(NH3)2]NO3
(3)(NH4)2Fe(SO4)2溶液呈酸性,试用离子方程式解释其原因:
_________________________ ;____________________________ 。
(1) 实验室用(NH4)2Fe(SO4)2固体配制一定浓度的(NH4)2Fe(SO4)2标准溶液。
①配制溶液时,需要使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的

②若要配制0.100 mol·L-1的(NH4)2Fe(SO4)2标准溶液250ml,需称取(NH4)2Fe(SO4)2
③若在配制过程中,烧杯中的(NH4)2Fe(SO4)2溶液有少量溅出,则所得溶液浓度
(2)能电离出两种阳离子的盐称为复盐,下列物质中属于复盐的有
a.KAl(SO4)2 b.KAlO2 c.NH4Al(SO4)2 d.[Ag(NH3)2]NO3
(3)(NH4)2Fe(SO4)2溶液呈酸性,试用离子方程式解释其原因:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】钴的某些化合物与铁的化合物性质相似,某研究性学习小组为探究钴的化合物的性质,进行了以下实验:
Ⅰ.探究草酸钴的热分解产物
(1)为探究草酸钴的热分解产物,按气体流动方向,各装置的连接顺序为:A→E→________________ 。
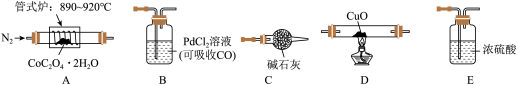
(2)能证明分解产物中有CO的实验现象是_____________________________________________________ 。
(3)取5.49gCoC2O4·2H2O于硬质玻璃管中加热至恒重,冷却、称量,剩余固体的质量为2.25g,球形干燥管增重1.32g。则球形干燥管吸收的气体的结构式为:__________________ ;A中发生反应的化学方程式为:_____________________________________________________ 。
Ⅱ.探究Co(OH)2的还原性及Co(OH)3的氧化性
取A装置所得固体溶解于稀H2SO4中得到粉红色溶液,备用。
已知试剂颜色:CoSO4溶液(粉红色),Co(OH)2(粉红色),Co(OH)3(棕褐色)。
实验记录如表:
Ⅰ.探究草酸钴的热分解产物
(1)为探究草酸钴的热分解产物,按气体流动方向,各装置的连接顺序为:A→E→

(2)能证明分解产物中有CO的实验现象是
(3)取5.49gCoC2O4·2H2O于硬质玻璃管中加热至恒重,冷却、称量,剩余固体的质量为2.25g,球形干燥管增重1.32g。则球形干燥管吸收的气体的结构式为:
Ⅱ.探究Co(OH)2的还原性及Co(OH)3的氧化性
取A装置所得固体溶解于稀H2SO4中得到粉红色溶液,备用。
已知试剂颜色:CoSO4溶液(粉红色),Co(OH)2(粉红色),Co(OH)3(棕褐色)。
实验记录如表:
| 实验操作及现象 | 实验分析 | |
| 实验1 | 取少许粉红色溶液于试管中,滴加0.1mol·L-1NaOH溶液,生成粉红色沉淀,并将该沉淀分成两份 | |
| 实验2 | 取一份实验1中所得的粉红色沉淀,加入3%的H2O2溶液,粉红色沉淀立即变为棕褐色 | 反应的化学方程式为 |
| 实验3 | 向实验2得到的棕褐色沉淀中滴加浓盐酸,固体逐渐溶解,并有黄绿色气体产生 | 反应的离子方程式为 |
| 实验4 | 取另一份实验1中所得的粉红色沉淀,滴加浓盐酸,粉红色沉淀溶解,未见气体生成 | 酸性条件下,Cl2、Co(OH)2、Co(OH)3的氧化能力由大到小的顺序是 |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】工业上常采用硝酸工业的含硝尾气制备亚硝酸钠,再利用亚硝酸钠制备亚硝酸钾,相关制备流程如下:
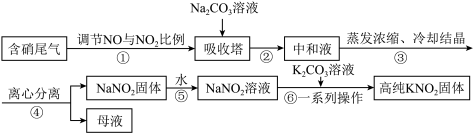
已知:①亚硝酸钠(NaNO2)是一种白色至浅黄色晶体或粉末,受热易分解,露置于空气中缓慢氧化。
②KMnO4在中性或碱性溶液中的还原产物为MnO2,在酸性条件下为Mn2+。
请回答:
(1)下列操作或描述正确的是________ 。
A. 步骤①调节NO与NO2比例使尾气被碱液充分吸收,且提高NaNO2产率
B. 在吸收塔中含硝尾气从底部通入,Na2CO3溶液从塔顶喷淋
C. 母液中溶质只有Na2CO3和NaNO3
D. 所得NaNO2固体产品中含有杂质NaNO3
(2)离心分离是一种固液分离操作,步骤④可用以下三个操作中的________ (选最佳)代替。
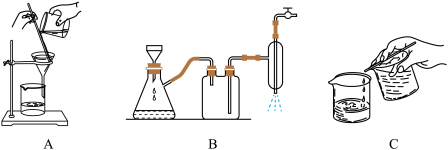
(3)NaNO2产品纯度分析。若用NaNO2待测液滴定酸性KMnO4标准溶液,终点现象是___ ,测定结果与真实值非常接近;而采用酸性KMnO4标准液滴定NaNO2待测液的方法进行测定,根据滴定结果计算NaNO2产品纯度总是大于100%,可能的原因是________ 。
(4)已知相关物质的溶解表如下:
(i)根据相关物质溶解性信息,写出步骤⑥的化学方程式________ 。
(ii)步骤⑥正确的操作顺序为:b→_____ →_____ →c。
a 在85℃下蒸发浓缩,并不断将析出的Na2CO3晶体捞出
b 将NaNO2溶液与K2CO3溶液充分混合
c 离心分离,在60~70℃下干燥,迅速冷却,密封储存
d 热溶液冷却结晶获得高纯KNO2

已知:①亚硝酸钠(NaNO2)是一种白色至浅黄色晶体或粉末,受热易分解,露置于空气中缓慢氧化。
②KMnO4在中性或碱性溶液中的还原产物为MnO2,在酸性条件下为Mn2+。
请回答:
(1)下列操作或描述正确的是
A. 步骤①调节NO与NO2比例使尾气被碱液充分吸收,且提高NaNO2产率
B. 在吸收塔中含硝尾气从底部通入,Na2CO3溶液从塔顶喷淋
C. 母液中溶质只有Na2CO3和NaNO3
D. 所得NaNO2固体产品中含有杂质NaNO3
(2)离心分离是一种固液分离操作,步骤④可用以下三个操作中的

(3)NaNO2产品纯度分析。若用NaNO2待测液滴定酸性KMnO4标准溶液,终点现象是
(4)已知相关物质的溶解表如下:
| 物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ |
| Na2CO3 | 7 | 21.5 | 49 | 46 | 43.9 |
| K2CO3 | 105 | 111 | 117 | 127 | 140 |
| NaNO2 | 71.2 | 80.8 | 94.9 | 111 | 113 |
| KNO2 | 279 | 306 | 329 | 348 | 376 |
(i)根据相关物质溶解性信息,写出步骤⑥的化学方程式
(ii)步骤⑥正确的操作顺序为:b→
a 在85℃下蒸发浓缩,并不断将析出的Na2CO3晶体捞出
b 将NaNO2溶液与K2CO3溶液充分混合
c 离心分离,在60~70℃下干燥,迅速冷却,密封储存
d 热溶液冷却结晶获得高纯KNO2
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】固体X(相对分子质量在140-200之间)由两种短周期元素组成,在常温下为橙黄色晶体,取7.36g固体X分成两等份,分别进行以下两组实验。(气体体积均为标况下体积)。
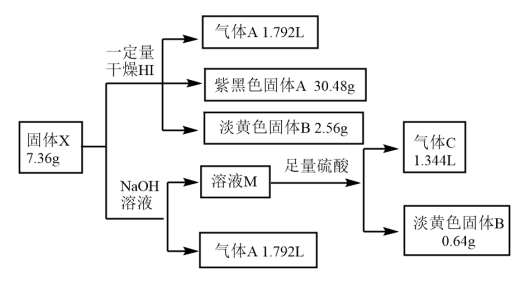
已知:气体A能使湿润的红色石蕊试纸变蓝,气体C能使品红溶液褪色。
(1)组成X的元素是_______ ,X的化学式为________ 。
(2)固体X与一定量干燥HI反应时的化学方程式为______________ 。
(3)①溶液M中含有高中较常见的两种钠盐,其元素组成相同,其中一种钠盐和足量硫酸反应生成等物质的量的固体B和气体C,该反应的离子方程式为___________ 。
②溶液M在空气中久置可能会变质,请设计实验证明溶液M是否已经变质?____________ 。

已知:气体A能使湿润的红色石蕊试纸变蓝,气体C能使品红溶液褪色。
(1)组成X的元素是
(2)固体X与一定量干燥HI反应时的化学方程式为
(3)①溶液M中含有高中较常见的两种钠盐,其元素组成相同,其中一种钠盐和足量硫酸反应生成等物质的量的固体B和气体C,该反应的离子方程式为
②溶液M在空气中久置可能会变质,请设计实验证明溶液M是否已经变质?
您最近一年使用:0次



