已知反应: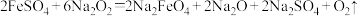 。下列关于该反应的说法不正确的是
。下列关于该反应的说法不正确的是
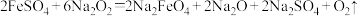 。下列关于该反应的说法不正确的是
。下列关于该反应的说法不正确的是A. 可以对水体进行杀菌消毒、净化 可以对水体进行杀菌消毒、净化 |
B. 在该反应中既是氧化剂又是还原剂 在该反应中既是氧化剂又是还原剂 |
C.1mol 还原等物质的量的 还原等物质的量的 |
D.每生成1mol ,该反应转移4mol电子 ,该反应转移4mol电子 |
2023·浙江温州·模拟预测 查看更多[2]
更新时间:2024-01-24 11:02:37
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列变化中,一定要加还原剂才能实现的是
A.SO2→HSO | B.FeCl3→FeCl2 | C.Cl2→Cl- | D.KMnO4→MnO2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】新型净水剂高铁酸钾(K2FeO4)为暗紫色固体,可溶于水.工业上制备K2FeO4的常用方法之一是次氯酸盐氧化法:①2FeCl3+10NaOH+3NaClO = 2Na2FeO4+9NaCl+5H2O,② Na2FeO4 + 2KOH = K2FeO4 + 2NaOH .下列说法不正确 的是
| A.反应①为氧化还原反应,反应②为复分解反应 |
| B.反应①中NaClO 是氧化剂 |
| C.反应②的产物K2FeO4中Fe为+4价,具有强氧化性,能杀菌消毒 |
| D.若有2 mol FeCl3 发生反应,转移电子的物质的量为 6 mol |
您最近一年使用:0次
【推荐1】 是有机合成中一种重要的还原剂,能与
是有机合成中一种重要的还原剂,能与 等强氧化剂剧烈反应。利用
等强氧化剂剧烈反应。利用 氧化尿素制备
氧化尿素制备 (水合肼)的实验流程如图所示:
(水合肼)的实验流程如图所示:

已知:氯气与烧碱溶液的反应是放热反应。下列说法不正确的是
 是有机合成中一种重要的还原剂,能与
是有机合成中一种重要的还原剂,能与 等强氧化剂剧烈反应。利用
等强氧化剂剧烈反应。利用 氧化尿素制备
氧化尿素制备 (水合肼)的实验流程如图所示:
(水合肼)的实验流程如图所示:
已知:氯气与烧碱溶液的反应是放热反应。下列说法不正确的是
| A.步骤I中为避免温度过高,可采用冰水浴 |
B.步骤I制备 溶液时,测得产物中 溶液时,测得产物中 与 与 的物质的量之比为 的物质的量之比为 ,则参与反应的氧化剂与还原剂的物质的量之比为 ,则参与反应的氧化剂与还原剂的物质的量之比为 |
C.步骤II中可将尿素水溶液逐滴滴入 碱性溶液中 碱性溶液中 |
D.步骤II反应的离子方程式为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些 气体与112LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得 硝酸铜溶液中加入1mol/LNaOH溶液至Cu2+恰好完全沉淀,则此消耗NaOH溶液的体积是
| A.10 L | B.20 L | C.30 L | D.4L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列应用涉及氧化还原反应的是
| A.用TiCl4制备纳米级TiO2 |
| B.高铁酸钾(K2FeO4)用作新型水处理剂 |
| C.用明矾溶液除去铜制品表面的铜绿 |
| D.工业上将NH3和CO2通入饱和食盐水制备小苏打 |
您最近一年使用:0次
【推荐2】高铁酸钠(Na2FeO4)具有很强的氧化性,能有效地杀灭水中的细菌和病毒,同时被还原成Fe(OH)3能高效地除去水中的悬浮物,是一种新型高效水处理剂。其制备方法如下: 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是| A.该反应中氧化剂和还原剂的物质的量之比为3∶2 |
| B.碱性条件下NaClO氧化性强于Na2FeO4 |
| C.每生成1mol Na2FeO4转移6mol电子 |
| D.在水处理中,Na2FeO4兼具消毒和净水两种功能 |
您最近一年使用:0次
【推荐1】黄铁矿(主要成分为FeS2)因其呈浅黄铜色且具有明亮的金属光泽,常被误认为是黄金,故又称为“愚人金”。在酸和催化剂的作用下FeS2发生如图所示的转化。下列分析正确的是
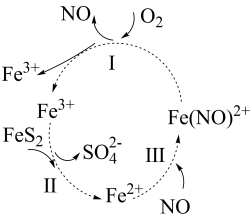

| A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应 |
B.在酸性条件下,黄铁矿催化氧化中只有 作催化剂 作催化剂 |
C.反应Ⅱ中,每消耗 ,转移电子的物质的量为14mol ,转移电子的物质的量为14mol |
D.反应Ⅰ的离子方程式: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向 溶液中加入
溶液中加入 可以加快
可以加快 分解速率。其反应机理可能有两步,第 1 步:
分解速率。其反应机理可能有两步,第 1 步: 。下列说法正确的是
。下列说法正确的是
 溶液中加入
溶液中加入 可以加快
可以加快 分解速率。其反应机理可能有两步,第 1 步:
分解速率。其反应机理可能有两步,第 1 步: 。下列说法正确的是
。下列说法正确的是A. 分子中含有离子键和非极性键 分子中含有离子键和非极性键 |
B.第 2 步反应为: |
C.第 1 步反应每生成 ,转移 ,转移 电子 电子 |
D.该反应机理中, 催化 催化 分解产生 分解产生 |
您最近一年使用:0次

 的物质的量浓度之比为3∶1,则Cl2与NaOH溶液反应时,被还原的氯元素与被氧化的氯元素的物质的量之比为
的物质的量浓度之比为3∶1,则Cl2与NaOH溶液反应时,被还原的氯元素与被氧化的氯元素的物质的量之比为
 )可用于饮用水的消毒,由此可预测,高铁酸盐(FeO
)可用于饮用水的消毒,由此可预测,高铁酸盐(FeO

