化学与生产生活密切相关,利用所学化学知识回答下列问题。
(1)雷雨天闪电时空气中有 生成。
生成。 与
与 的关系是互为
的关系是互为_______ ,等质量的 和
和 的分子数之比为
的分子数之比为_______ 。
(2)铁路工人经常用铝热反应来焊接钢轨,反应产物为 、Al2O3,
、Al2O3, 溶液可检验反应后的产物中是否有
溶液可检验反应后的产物中是否有 残留,用离子方程式说明其原理
残留,用离子方程式说明其原理_______ 。
(3)阅读下列科普短文并填空。
地表的天然水中含有很多杂质,为满足人们生产生活的需要,必须对其进行处理。利用混凝剂 可除去天然水中的县浮物。
可除去天然水中的县浮物。 在水中发生电离,产生的
在水中发生电离,产生的 与水反应生成
与水反应生成 胶体,可以吸附悬浮物与色素。为获得饮用水,还需对天然水消毒杀菌。过去广泛采用氯水作水体的消毒剂,近年来
胶体,可以吸附悬浮物与色素。为获得饮用水,还需对天然水消毒杀菌。过去广泛采用氯水作水体的消毒剂,近年来 和
和 备受关注。
备受关注。 溶于水能释放大量的原子氧,从而有效杀灭水中的病菌,同时生成具有良好吸附性的
溶于水能释放大量的原子氧,从而有效杀灭水中的病菌,同时生成具有良好吸附性的 胶体,所以
胶体,所以 具有广阔的应用前景。
具有广阔的应用前景。
①可利用_______ 证明 溶于水后得到
溶于水后得到 胶体。
胶体。
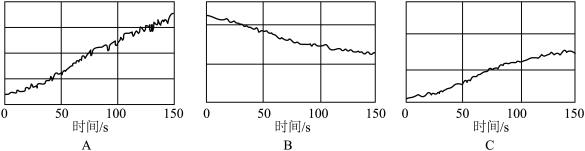
②利用数字化实验对光照过程中新制氯水的变化进行检测,下图能表示氯水的 随时间变化的图像是
随时间变化的图像是_______ (填字母),用化学方程式说明这一变化的原因_______ 。
(4)配平 溶于水后发生反应的离子方程式:
溶于水后发生反应的离子方程式:_______ 。
_______ _______
_______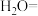 _______
_______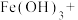 _______
_______ 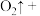 _______
_______ 。
。
每转移电子 ,生成标准状况下
,生成标准状况下 的体积为
的体积为_______ 。
(1)雷雨天闪电时空气中有
 生成。
生成。 与
与 的关系是互为
的关系是互为 和
和 的分子数之比为
的分子数之比为(2)铁路工人经常用铝热反应来焊接钢轨,反应产物为
 、Al2O3,
、Al2O3, 溶液可检验反应后的产物中是否有
溶液可检验反应后的产物中是否有 残留,用离子方程式说明其原理
残留,用离子方程式说明其原理(3)阅读下列科普短文并填空。
地表的天然水中含有很多杂质,为满足人们生产生活的需要,必须对其进行处理。利用混凝剂
 可除去天然水中的县浮物。
可除去天然水中的县浮物。 在水中发生电离,产生的
在水中发生电离,产生的 与水反应生成
与水反应生成 胶体,可以吸附悬浮物与色素。为获得饮用水,还需对天然水消毒杀菌。过去广泛采用氯水作水体的消毒剂,近年来
胶体,可以吸附悬浮物与色素。为获得饮用水,还需对天然水消毒杀菌。过去广泛采用氯水作水体的消毒剂,近年来 和
和 备受关注。
备受关注。 溶于水能释放大量的原子氧,从而有效杀灭水中的病菌,同时生成具有良好吸附性的
溶于水能释放大量的原子氧,从而有效杀灭水中的病菌,同时生成具有良好吸附性的 胶体,所以
胶体,所以 具有广阔的应用前景。
具有广阔的应用前景。①可利用
 溶于水后得到
溶于水后得到 胶体。
胶体。②利用数字化实验对光照过程中新制氯水的变化进行检测,下图能表示氯水的
 随时间变化的图像是
随时间变化的图像是
(4)配平
 溶于水后发生反应的离子方程式:
溶于水后发生反应的离子方程式:_______
 _______
_______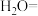 _______
_______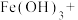 _______
_______ 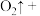 _______
_______ 。
。每转移电子
 ,生成标准状况下
,生成标准状况下 的体积为
的体积为
更新时间:2024-02-14 17:20:39
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】T℃时,向容积为2L的恒容密闭容器中充入2molA气体和3molB气体,发生如下反应: 。反应进行到10s末,达到平衡状态,测得A的物质的量为1.2mol,C的物质的量浓度为
。反应进行到10s末,达到平衡状态,测得A的物质的量为1.2mol,C的物质的量浓度为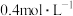 。回答下列问题:
。回答下列问题:
(1)x的值为_______ ,用D表示10s内反应的平均反应速率为_______ 。
(2)0~10s容器内气体的平均摩尔质量变化是_______ (填“增大”“减小”或“不变”,下同),气体的密度变化是_______ 。
(3)平衡后,若改变下列条件。生成D的速率如何变化(填“增大”“减小”或“不变”):
①降低温度_______ ;
②增大A的浓度_______ ;
③恒容下充入氖气_______ 。
 。反应进行到10s末,达到平衡状态,测得A的物质的量为1.2mol,C的物质的量浓度为
。反应进行到10s末,达到平衡状态,测得A的物质的量为1.2mol,C的物质的量浓度为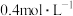 。回答下列问题:
。回答下列问题:(1)x的值为
(2)0~10s容器内气体的平均摩尔质量变化是
(3)平衡后,若改变下列条件。生成D的速率如何变化(填“增大”“减小”或“不变”):
①降低温度
②增大A的浓度
③恒容下充入氖气
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)浩瀚的大海蕴藏着丰富的资源,从海水中可以获得很多化学物质。海水晒盐得到___ ,氯碱工业的产品有氯气、___ 、___ 。
(2)以下物质中:①葡萄糖;②氧化钠;③氯化镁溶液;④液态氯化氢,其中属于电解质的是___ 。
(3)15.6gNa2X含有0.2molX2-,含有Na+的物质的量是___ mol,Na2X的摩尔质量为___ g·mol-1。
(2)以下物质中:①葡萄糖;②氧化钠;③氯化镁溶液;④液态氯化氢,其中属于电解质的是
(3)15.6gNa2X含有0.2molX2-,含有Na+的物质的量是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】完成下列填空:
(1)0.3molNH3分子中所含原子数与___ 个H2O分子中所含原子数相等。
(2)在一定的温度和压强下,1体积气体X2跟3体积气体Y2刚好化合生成2体积气体A,则A的化学式可表示为___ 。
(3)在同温同压同体积的条件下,H2与气体B的质量之比是1:8,则B的摩尔质量为___ 。
(4)在25℃、101kPa的条件下,同质量的CH4和气体C的体积之比是15:8,则C的摩尔质量为___ 。
(5)在两个相同容积的密闭容器D、E中,分别充入相同质量的X气体和CO气体,D和E中的压强之比是7:16,则X的摩尔质量为___ 。
(6)物质的量浓度相同的NaCl、MgCl2、AlCl3,溶液中Cl-的物质的量浓度之比为___ ;体积相同的、物质的量浓度之比为1:2:3的NaCl、MgCl2、AlCl3三种溶液中Cl-的物质的量之比为___ 。
(1)0.3molNH3分子中所含原子数与
(2)在一定的温度和压强下,1体积气体X2跟3体积气体Y2刚好化合生成2体积气体A,则A的化学式可表示为
(3)在同温同压同体积的条件下,H2与气体B的质量之比是1:8,则B的摩尔质量为
(4)在25℃、101kPa的条件下,同质量的CH4和气体C的体积之比是15:8,则C的摩尔质量为
(5)在两个相同容积的密闭容器D、E中,分别充入相同质量的X气体和CO气体,D和E中的压强之比是7:16,则X的摩尔质量为
(6)物质的量浓度相同的NaCl、MgCl2、AlCl3,溶液中Cl-的物质的量浓度之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】用电弧法合成碳纳米管,常伴有大量杂质 碳纳米颗粒
碳纳米颗粒 这种碳纳米颗粒可用氧化气化法提纯
这种碳纳米颗粒可用氧化气化法提纯 其反应方程式为:2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑
其反应方程式为:2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑
(1)用双线桥法表示出该反应电子转移的方向和数目___ 。
(2)此反应的氧化产物和还原产物的物质的量之比为___ 。
(3)若产生6.72LCO2 标准状况下
标准状况下 气体,该反应转移电子的物质的量为
气体,该反应转移电子的物质的量为___ 。
 碳纳米颗粒
碳纳米颗粒 这种碳纳米颗粒可用氧化气化法提纯
这种碳纳米颗粒可用氧化气化法提纯 其反应方程式为:2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑
其反应方程式为:2K2Cr2O7+3C+8H2SO4=2Cr2(SO4)3+2K2SO4+8H2O+3CO2↑(1)用双线桥法表示出该反应电子转移的方向和数目
(2)此反应的氧化产物和还原产物的物质的量之比为
(3)若产生6.72LCO2
 标准状况下
标准状况下 气体,该反应转移电子的物质的量为
气体,该反应转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】阅读下面一段材料并回答问题。
(1) 中铁元素的化合价为
中铁元素的化合价为_______ 。
(2)制备 需要在
需要在_______  填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性” 环境中进行。
环境中进行。
(3)下列关于 的说法中,不正确的是
的说法中,不正确的是_______ 。
 是强氧化性的盐
是强氧化性的盐
 固体保存需要防潮
固体保存需要防潮
 其消毒和净化水的原理相同
其消毒和净化水的原理相同
 其净水优点有:作用快、安全性好、无异味
其净水优点有:作用快、安全性好、无异味
(4)将 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整:_______
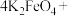 _______
_______ _______
_______ 胶体
胶体 _______
_______ _______
_______
该反应消耗1个 时,转移的电子数为
时,转移的电子数为_______ 个
(5)消毒净化 水,至少需要
水,至少需要 的质量为
的质量为_______  。
。
| 高铁酸钾使用说明书 【化学式】K2FeO4 【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着pH减小,稳定性下降,与水反应放出氧气K2FeO4通过强烈 的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。K2FeO4与水反应还能产生具有强吸附 性的Fe(OH)3胶体,可除去水中细微的悬浮物,有净水作用 【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放5 mg K2FeO4即可达到卫生标准 ... ... |
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在 填“酸性”、“碱性”或“中性”
填“酸性”、“碱性”或“中性” 环境中进行。
环境中进行。(3)下列关于
 的说法中,不正确的是
的说法中,不正确的是 是强氧化性的盐
是强氧化性的盐 固体保存需要防潮
固体保存需要防潮 其消毒和净化水的原理相同
其消毒和净化水的原理相同 其净水优点有:作用快、安全性好、无异味
其净水优点有:作用快、安全性好、无异味(4)将
 与水反应的化学方程式补充完整:
与水反应的化学方程式补充完整: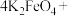 _______
_______ _______
_______ 胶体
胶体 _______
_______ _______
_______
该反应消耗1个
 时,转移的电子数为
时,转移的电子数为(5)消毒净化
 水,至少需要
水,至少需要 的质量为
的质量为 。
。
您最近一年使用:0次
【推荐3】实验室可用如下方法制取Cl2,根据相关信息,回答下列问题:
(1)用双线桥法表示电子转移方向和数目_____ :①MnO2 +4HCl(浓)= Cl2↑+ MnCl2+ 2H2O
(2)若反应中有0.1mol的氧化剂被还原,则被氧化的物质为__ (填化学式),被氧化的物质的量为 _____ ,同时转移电子数为_____ 。
(3)将(2)生成的氯气与 0.2mol H2 完全反应,生成的气体在标准状况下所占体积为_____ L,将此产物溶于水配成100mL溶液,此溶液的物质的量浓度为_______ 。(已知:H2+Cl2 2HCl)
2HCl)
(4)②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O③2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O
若要制得相同质量的氯气,①②③三个反应中电子转移的数目之比为____ 。
(5)已知反应4HCl(g)+O2 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由弱到强的顺序为
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由弱到强的顺序为_______ 。
(6)将不纯的NaOH样品2.50 g(样品含少量Na2CO3和水),放入50.0 mL 2.00mol/L盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40.0 mL 1.00 mol/L的NaOH溶液。蒸发中和后的溶液,最终得到_____ g固体。
(1)用双线桥法表示电子转移方向和数目
(2)若反应中有0.1mol的氧化剂被还原,则被氧化的物质为
(3)将(2)生成的氯气与 0.2mol H2 完全反应,生成的气体在标准状况下所占体积为
 2HCl)
2HCl)(4)②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O③2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O
若要制得相同质量的氯气,①②③三个反应中电子转移的数目之比为
(5)已知反应4HCl(g)+O2
 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由弱到强的顺序为
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由弱到强的顺序为(6)将不纯的NaOH样品2.50 g(样品含少量Na2CO3和水),放入50.0 mL 2.00mol/L盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40.0 mL 1.00 mol/L的NaOH溶液。蒸发中和后的溶液,最终得到
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I.有下列物质:①氢氧化钡固体 ②KHSO4 ③HNO3 ④稀硫酸 ⑤二氧化碳气体 ⑥铜 ⑦碳酸钠粉末 ⑧蔗糖晶体 ⑨熔融氯化钠 ⑩CuSO4·5H2O晶体。请用序号填空:
(1)上述状态下可导电的是___________ 。
(2)属于电解质的是___________ 。
(3)属于非电解质的是___________ 。
II.实验小组为探究次氯酸消毒剂的分解规律,进行了下列实验。
①制备和净化氯气。使用MnO2等几种原料制备并净化氯气。
②制备氯水。将氯气通入水中,得到氯水。
③除去尾气。用烧碱溶液吸收多余的氯气。
④探究次氯酸的分解规律。用数字传感器测量光照条件下装有氯水的容器中氧气浓度的变化、氯水的pH变化以及氯离子浓度的变化,装置如图1所示。测量的数据如图2所示。
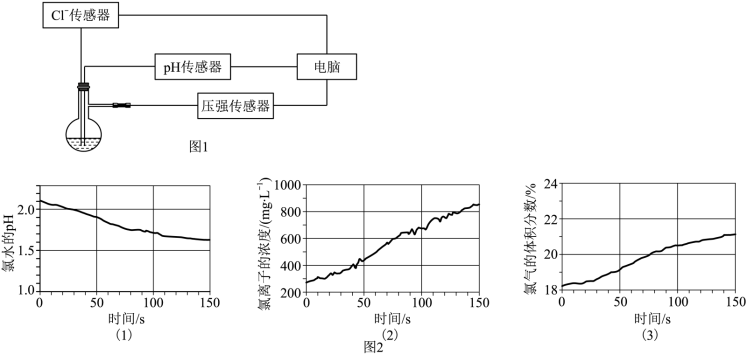
(4)实验室制备氯气时发生反应的化学方程式为___________ ; 上述实验所制备的氯气中含有的杂质气体为水蒸气和___________ 。为除去所填杂质气体,常使用的试剂是___________ 。
(5)制备氯水的方法是将氯气通入水中,反应的离子方程式为___________ 。多余氯气常用过量的烧碱溶液吸收处理,吸收时反应的离子方程式为___________ 。
(6)依据数字传感器所测量的图2中(1)和(2)数据,解释光照时氯水的pH变化及氯离子浓度变化的原因___________ (结合化学方程式说明)
(1)上述状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
II.实验小组为探究次氯酸消毒剂的分解规律,进行了下列实验。
①制备和净化氯气。使用MnO2等几种原料制备并净化氯气。
②制备氯水。将氯气通入水中,得到氯水。
③除去尾气。用烧碱溶液吸收多余的氯气。
④探究次氯酸的分解规律。用数字传感器测量光照条件下装有氯水的容器中氧气浓度的变化、氯水的pH变化以及氯离子浓度的变化,装置如图1所示。测量的数据如图2所示。

(4)实验室制备氯气时发生反应的化学方程式为
(5)制备氯水的方法是将氯气通入水中,反应的离子方程式为
(6)依据数字传感器所测量的图2中(1)和(2)数据,解释光照时氯水的pH变化及氯离子浓度变化的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】新制氯水中有很多种微粒,与不同的物质相遇时,由不同的微粒参与反应。
(1)向FeCl2溶液中滴加氯水,主要反应的离子方程式是__________________________ 。
(2)氯水可以消毒杀菌,氯水中起作用的主要微粒是________ ,利用该微粒的_____________ 性。
(3)向AgNO3溶液中滴加氯水,反应的离子方程是____________________________ 。
(4)新制氯水中滴加紫色石蕊试液,溶液变红,氯水中起作用的主要微粒是________ ,然后又褪色,起作用的微粒是 _________ 。
(5)新制氯水久置失效,主要原因是(用化学方程式表达)_______________________ 。
(1)向FeCl2溶液中滴加氯水,主要反应的离子方程式是
(2)氯水可以消毒杀菌,氯水中起作用的主要微粒是
(3)向AgNO3溶液中滴加氯水,反应的离子方程是
(4)新制氯水中滴加紫色石蕊试液,溶液变红,氯水中起作用的主要微粒是
(5)新制氯水久置失效,主要原因是(用化学方程式表达)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某同学在复习元素化合物的性质时,做了如下学习笔记,请你一起完成。
氯气的颜色为__________ ;由氯的原子结构示意图推测,氯气具有很强的______ 性。为了证明推测是否正确,进行如下实验:
I:将红热的铁丝伸入盛满氯气的集气瓶,观察铁丝在氯气中燃烧,有大量棕黄色烟。该反应的化学方程式是___________ 。
II:在空气中点燃H2,然后将导管缓缓伸入盛满氯气的集气瓶,可观察到H2在氯气中安静燃烧,产生______ 色的火焰,瓶口有白雾的现象。
由实验I、II可知,上述推测_____ (填“正确”或“不正确”)。
III:将氯气溶于水,制得氯水。下列物质不能与新制氯水反应的是_____ 。
A.Na2CO3溶液 B.FeCl2溶液 C.AgNO3 溶液 D.CuCl2溶液
氯气的颜色为
I:将红热的铁丝伸入盛满氯气的集气瓶,观察铁丝在氯气中燃烧,有大量棕黄色烟。该反应的化学方程式是
II:在空气中点燃H2,然后将导管缓缓伸入盛满氯气的集气瓶,可观察到H2在氯气中安静燃烧,产生
由实验I、II可知,上述推测
III:将氯气溶于水,制得氯水。下列物质不能与新制氯水反应的是
A.Na2CO3溶液 B.FeCl2溶液 C.AgNO3 溶液 D.CuCl2溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】Ⅰ.X、Y、Z、W、M为短周期主族元素,25℃时,其最高价氧化物对应的水化物(浓度均为0.01mol·L-1)溶液的pH和原子半径的关系如图所示。
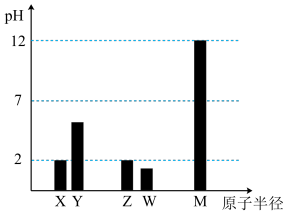
(1)Y的最高价氧化物的电子式为:___________
(2)最简单气态氢化物的热稳定性:Z___________ W(>或<)
(3)X、M两种元素形成的简单离子半径大小顺序:X___________ M(>或<)
(4)X的氢化物与Z的氢化物反应后生成的化合物中的化学键类型是___________
Ⅱ.铝自然形成的氧化膜易脱落。以硫酸为电解液,分别以石墨和铝材作阴、阳极材料,经过电解处理形成氧化铝膜,抗蚀能力强。其制备的简要流程如图所示。
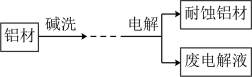
(5)碱洗目的是___________ 相关离子反应是:___________
(6)碱洗时铝材表面会出现气泡,可能的原因是___________ (化学反应方程式),用稀氨水洗去耐蚀铝材表面的酸,离子方程式___________
Ⅲ.为证明铁的金属活动性比铜强,某同学设计了如下一些方案:
(7)能根据现象或产物证明铁的金属活动性比铜强的方案有___________

(1)Y的最高价氧化物的电子式为:
(2)最简单气态氢化物的热稳定性:Z
(3)X、M两种元素形成的简单离子半径大小顺序:X
(4)X的氢化物与Z的氢化物反应后生成的化合物中的化学键类型是
Ⅱ.铝自然形成的氧化膜易脱落。以硫酸为电解液,分别以石墨和铝材作阴、阳极材料,经过电解处理形成氧化铝膜,抗蚀能力强。其制备的简要流程如图所示。

(5)碱洗目的是
(6)碱洗时铝材表面会出现气泡,可能的原因是
Ⅲ.为证明铁的金属活动性比铜强,某同学设计了如下一些方案:
| 方案 | 现象或产物 |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| ②将铁丝和铜丝分别在氯气中燃烧 | 产物分别为FeCl3和CuCl2 |
| ③将铁片和铜片分别放入热浓硫酸中 | 产物为Fe2(SO4)3和CuSO4 |
| ④将铜片置于FeCl3溶液中 | 铜片逐渐溶解 |
| ⑤将铁片和铜片置于盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铝和铁是中学化学常见的金属。请回答下列问题:
(1)常温下,铝和铁放入浓HNO3中会发生_______ ;
A.都反应产生氢气B.只有铝反应产生氢气
C.只有铁反应产生氢气D.都钝化
(2)常温下,铝粉和铁粉分别放入氢氧化钠溶液中,能反应产生氢气的是_______ ,
(3)铝热反应的化学方程式:2Al+Fe2O3 2Fe+Al2O3,其氧化剂是
2Fe+Al2O3,其氧化剂是_________ 。
A.AlB.FeC.Fe2O3D.Al2O3
(1)常温下,铝和铁放入浓HNO3中会发生
A.都反应产生氢气B.只有铝反应产生氢气
C.只有铁反应产生氢气D.都钝化
(2)常温下,铝粉和铁粉分别放入氢氧化钠溶液中,能反应产生氢气的是
(3)铝热反应的化学方程式:2Al+Fe2O3
 2Fe+Al2O3,其氧化剂是
2Fe+Al2O3,其氧化剂是A.AlB.FeC.Fe2O3D.Al2O3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】近年来,科技人员研究得到一种新型材料——泡沫铝。它是把发泡剂加到熔融或固体粉末的铝合金中而制成的,其优点是硬度高、密度小(约为0.16~0.5 g/cm3),比木材还轻,可浮于水面,又有很大刚性,且隔音、保温,是一种良好的建筑材料和轻质材料,可大批量投放市场。回答下列问题:
(1)铝制成铝箔用于食品包装,是利用它的__________ (填序号)。
A.金属光泽 B.延展性C.导电性 D.导热性
(2)铝在空气中会被氧化生成一层致密的氧化膜(氧化物)而对铝起保护作用,但这层氧化膜(氧化物)遇到强酸或强碱都会溶解,请写出其与盐酸反应的离子方程式:_________ 。与氢氧化钠溶液反应的化学方程式: _________ 。
(3)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,相同条件下所得H2的体积之比为______ 。
(4)足量的两份铝分别投入到等体积、一定物质的量浓度的HCl、NaOH溶液中,二者恰好完全反应且产生的H2相等,则HCl和NaOH的物质的量浓度之比是__________ 。
(1)铝制成铝箔用于食品包装,是利用它的
A.金属光泽 B.延展性C.导电性 D.导热性
(2)铝在空气中会被氧化生成一层致密的氧化膜(氧化物)而对铝起保护作用,但这层氧化膜(氧化物)遇到强酸或强碱都会溶解,请写出其与盐酸反应的离子方程式:
(3)等质量的两份铝分别与足量的盐酸、氢氧化钠溶液反应,相同条件下所得H2的体积之比为
(4)足量的两份铝分别投入到等体积、一定物质的量浓度的HCl、NaOH溶液中,二者恰好完全反应且产生的H2相等,则HCl和NaOH的物质的量浓度之比是
您最近一年使用:0次



