向 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随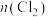 的变化曲线如图所示。(已知:
的变化曲线如图所示。(已知: 与
与 的水溶液生成
的水溶液生成 和
和 ,
, 为强酸)下列说法中不正确的是
为强酸)下列说法中不正确的是

 和
和 的混合溶液中不断通入
的混合溶液中不断通入 ,溶液中n(含碘的某微粒)和n(含铁的某微粒)随
,溶液中n(含碘的某微粒)和n(含铁的某微粒)随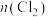 的变化曲线如图所示。(已知:
的变化曲线如图所示。(已知: 与
与 的水溶液生成
的水溶液生成 和
和 ,
, 为强酸)下列说法中不正确的是
为强酸)下列说法中不正确的是
A.a点溶液中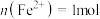 |
B.b点时已通入氯气的总体积为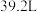 (标况) (标况) |
C.c点的总反应离子方程式为 |
D.d点溶液中阴离子的个数为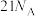 |
更新时间:2024-02-08 13:32:05
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】2021年我国科学家实现了二氧化碳到淀粉的人工合成。有关物质的转化过程示意如图所示,下列说法不正确的是(设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)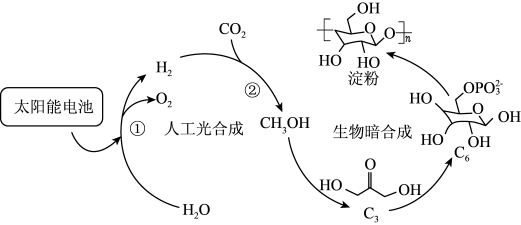
A.1mol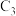 分子中含极性共价键的电子对数为6 分子中含极性共价键的电子对数为6 |
| B.人工合成淀粉为解决粮食危机提供了新思路 |
C. 合成甲醇,每消耗1mol 合成甲醇,每消耗1mol ,则转移电子数为6 ,则转移电子数为6 |
D.由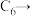 淀粉的过程中涉及C-O键和O—H键的断裂 淀粉的过程中涉及C-O键和O—H键的断裂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】设NA为阿伏加德罗常数值。下列有关叙述正确的是
| A.常温常压下,48 g O3中的氧原子数为3NA |
| B.24 g金属镁变为镁离子时失去的电子数为NA |
| C.4 ℃时9 mL水和标准状况下11.2 L氮气中的原子数均为NA |
D.2 mol L−l的CuCl2溶液中含有的氯离子数为4NA L−l的CuCl2溶液中含有的氯离子数为4NA |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】NA为阿伏加 德罗常数的值。下列有关叙述正确的是
| A.107 g Fe(OH)3胶体中胶体粒子的数目为NA |
| B.1 L 0.1 mol·L-1Na2CO3溶液中CO32-和HCO3-的离子数之和为0.1NA |
| C.常温常压下,3.6 g D2O与H218O中含有中子数2NA |
| D.30 g由14C2H2和C18O组成的混合气体中含有的质子数为14NA |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】下列离子方程式的书写正确的是
A.小苏打用于治疗胃酸过多: |
B.将少量溴水滴入过量 Na2SO3溶液中: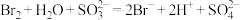 |
C.将过量 SO2通入 K2S 溶液中: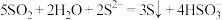 |
D.H2SO4与 Ba(OH)2反应: |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】铼(Re)被称为“类锰元素”,与锰的价电子排布相同,可以与氧气反应。一种对废氧化铝载体铂铼催化剂中金属元素综合回收利用的工艺如图:
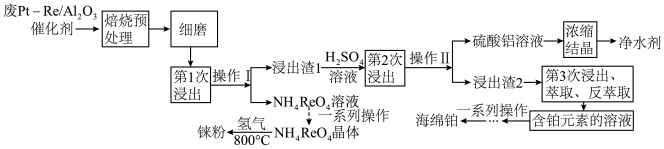
下列说法正确的是

下列说法正确的是
| A.“第1次浸出”中可以用氢氧化钠溶液代替氨水,浸出渣1成分不变 |
| B.铼元素的最高价氧化物Re2O7为碱性氧化物 |
| C.制备铼粉过程中,氢气只体现还原作用 |
D.“第3次浸出”中若用HC1-NaClO3作浸出液,反应离子方程式可能为:3Pt+16Cl-+2C1O +12H+=3[PtCl6]2-+6H2O +12H+=3[PtCl6]2-+6H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】前一时期“非典型肺炎”在我国部分地区流行,严重危害广大人民的身体健康,做好环境消毒是预防“非典型肺炎”的重要措施,常用的消毒剂是ClO2或Cl2等的稀溶液,其中ClO2溶液的消毒效果较好。已知ClO2常温下呈气态,其分子构型与水分子的分子构型相似,在自然环境中ClO2最终变为Cl-。下列有关说法中正确的是
| A.ClO2的分子结构呈V形,属非极性分子 |
| B.ClO2中氯元素显+4价,具有很强的氧化性,其消毒效率(以单位体积得电子的数目表示)是Cl2的5倍 |
| C.ClO2、Cl2的稀溶液用于环境消毒,具有广谱高效的特点,对人畜无任何危害 |
| D.常用Na2SO3在H2SO4的酸性条件下,还原NaClO3来制ClO2,这一反应的化学方程式可表示为Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】已知反应:FeO·Cr2O3+Na2CO3+NaNO3 Na2CrO4+Fe2O3+CO2+NaNO2 (未配平)。下列说法正确的是
Na2CrO4+Fe2O3+CO2+NaNO2 (未配平)。下列说法正确的是
 Na2CrO4+Fe2O3+CO2+NaNO2 (未配平)。下列说法正确的是
Na2CrO4+Fe2O3+CO2+NaNO2 (未配平)。下列说法正确的是| A.Na2CrO4是还原产物 | B.该反应中有3种元素的化合价发生变化 |
| C.NaNO3是还原剂 | D.1 mol FeO·Cr2O3参与反应将得到7 mol电子 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】某新型纳米材料氧缺位铁酸盐ZnFe2Ox(3<x<4),能在常温下将工业废气中的SO2、NO2等转化为单质而除去,由锌灰(含ZnO和少量PbO、CuO、Fe2O3等)为主要原料制备氧缺位铁酸盐及其转化废气的流程如图所示,下列说法不正确 的是
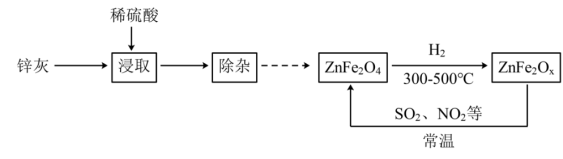

| A.浸取时为了提高酸浸效率,可以搅拌或延长浸取时间 |
| B.“除杂”过程中需要加入足量锌粉等操作,与锌粉反应的金属离子有Fe3+、Cu2+ |
| C.除去SO2时,ZnFe2Ox在反应中表现出氧化性 |
| D.ZnFe2O4与H2反应制得1molZnFe2Ox时,转移的电子物质的量为(8-2x)mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与11.2L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.若向所得硝酸铜溶液中加入2mol·L-1 NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
| A.2L | B.1 L | C.0.5L | D.3L |
您最近一年使用:0次
【推荐2】向27.2 g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5 L,固体物质完全反应,得到标准状况下8.96 L NO和NO2的混合气体及Cu(NO3)2。在所得溶液中加入1.0 mol/L的NaOH溶液1.0 L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2 g。下列有关说法不正确的是
| A.Cu和Cu2O的物质的量之比为2:1 | B.硝酸的物质的量浓度为2.8 mol/L |
| C.产生的NO2的体积在标准状况下为2.24 L | D.原混合物中Cu元素的质量分数为94.1% |
您最近一年使用:0次

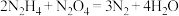 ,氧化产物与还原产物质量比为1:2
,氧化产物与还原产物质量比为1:2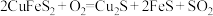 ,
, 仅作还原剂,硫元素被氧化
仅作还原剂,硫元素被氧化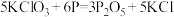 消耗3molP时,转移电子的物质的量为15mol
消耗3molP时,转移电子的物质的量为15mol

