前一时期“非典型肺炎”在我国部分地区流行,严重危害广大人民的身体健康,做好环境消毒是预防“非典型肺炎”的重要措施,常用的消毒剂是ClO2或Cl2等的稀溶液,其中ClO2溶液的消毒效果较好。已知ClO2常温下呈气态,其分子构型与水分子的分子构型相似,在自然环境中ClO2最终变为Cl-。下列有关说法中正确的是
| A.ClO2的分子结构呈V形,属非极性分子 |
| B.ClO2中氯元素显+4价,具有很强的氧化性,其消毒效率(以单位体积得电子的数目表示)是Cl2的5倍 |
| C.ClO2、Cl2的稀溶液用于环境消毒,具有广谱高效的特点,对人畜无任何危害 |
| D.常用Na2SO3在H2SO4的酸性条件下,还原NaClO3来制ClO2,这一反应的化学方程式可表示为Na2SO3+2NaClO3+H2SO4=2Na2SO4+2ClO2↑+H2O |
11-12高三上·河北唐山·期中 查看更多[4]
贵州省普定县一中2018-2019学年高二上学期期中考试化学试题云南省西双版纳州民族中学2017-2018学年高二6月份考试化学试题宁夏吴忠市高二人教版选修3第2章 分子结构与性质综合练习2(已下线)2012届河北省唐山一中高三上学期期中考试化学试卷
更新时间:2016-12-09 02:10:58
|
相似题推荐
【推荐1】将27.2 g Cu和 组成的混合物加入500 mL一定浓度的稀硝酸中,固体完全溶解生成
组成的混合物加入500 mL一定浓度的稀硝酸中,固体完全溶解生成 和NO。向所得溶液中加入500 mL 2.0 mol/L NaOH溶液,恰好生成沉淀的质量为39.2 g。下列说法正确的是
和NO。向所得溶液中加入500 mL 2.0 mol/L NaOH溶液,恰好生成沉淀的质量为39.2 g。下列说法正确的是
 组成的混合物加入500 mL一定浓度的稀硝酸中,固体完全溶解生成
组成的混合物加入500 mL一定浓度的稀硝酸中,固体完全溶解生成 和NO。向所得溶液中加入500 mL 2.0 mol/L NaOH溶液,恰好生成沉淀的质量为39.2 g。下列说法正确的是
和NO。向所得溶液中加入500 mL 2.0 mol/L NaOH溶液,恰好生成沉淀的质量为39.2 g。下列说法正确的是A.原固体混合物中,Cu和 的物质的量之比为1∶1 的物质的量之比为1∶1 |
| B.在标准状况下,产生的NO的体积为4.48 L |
| C.原稀硝酸的浓度为2.0 mol/L |
D.Cu、 与硝酸反应后剩余硝酸的物质的量为0.4 mol 与硝酸反应后剩余硝酸的物质的量为0.4 mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】羟胺(NH2OH)是一种还原剂。将16.00mL 0.05mol/L的羟胺酸性溶液与足量硫酸铁在煮沸条件下反应,生成的Fe2+又恰好被24.00mL 0.02mol/L的酸性KMnO4溶液所氧化。在上述反应中,羟胺的氧化产物为( )
| A.NO2 | B.NO | C.N2O | D.N2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】二氯化二硫 ( S2Cl2)是一种黄红色液体,常用作橡胶的低温硫化剂和粘结剂。S2Cl2分子中各原子最外层均有8个电子。S2Cl2遇水反应会产生淡黄色沉淀和刺激性气味气体。下列说法不正确 的是
| A.S2Cl2的结构式为 Cl—S —S—Cl |
| B.S2Cl2 可能使品红溶液褪色 |
| C.S2Cl2 与水反应时 ,氧化产物与还原产物的物质的量之比为 1 : 3 |
| D.将S2Cl2气体通入 AgNO3溶液中,若有白色沉淀产生,则 S2Cl2气体中有 HCl |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】磷酸亚铁锂(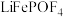 )是新型锂电池的正极材料,
)是新型锂电池的正极材料,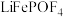 可通过
可通过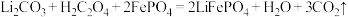 制得。该电池充电时
制得。该电池充电时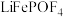 变成
变成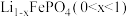 。(在制备和充电时:H、Li、P、O化合价不变,分别为+1、+1、+5、-2)。下列说法正确的是
。(在制备和充电时:H、Li、P、O化合价不变,分别为+1、+1、+5、-2)。下列说法正确的是
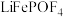 )是新型锂电池的正极材料,
)是新型锂电池的正极材料,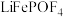 可通过
可通过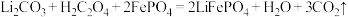 制得。该电池充电时
制得。该电池充电时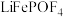 变成
变成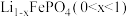 。(在制备和充电时:H、Li、P、O化合价不变,分别为+1、+1、+5、-2)。下列说法正确的是
。(在制备和充电时:H、Li、P、O化合价不变,分别为+1、+1、+5、-2)。下列说法正确的是A.该制备原理中 作氧化剂 作氧化剂 |
B.由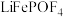 变成 变成 时,属于还原反应 时,属于还原反应 |
C.当 中 中 时, 时, 中的 中的 和 和 个数之比为2:3 个数之比为2:3 |
D.常温常压下生成150个 时,反应中转移100个电子 时,反应中转移100个电子 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列对试验现象的解释或结论均正确的是
| 实验操作 | 实验现象 | 解释与结论 | |
| A | 向鸡蛋清溶液中加入饱和 溶液 溶液 | 有白色沉淀产生 | 蛋白质发生了变性 |
| B | 室温下,向苯酚钠溶液中通入 | 出现白色浑浊 |  结合质子的能力比 结合质子的能力比 强 强 |
| C | 向苯中滴入少量浓溴水,振荡,静置 | 溶液分层,上层呈橙红色,下层几乎无色 | 苯和溴水发生取代反应,使溴水褪色 |
| D | 向蔗糖中加入浓硫酸 | 蔗糖变黑,体积膨胀,放热并放出刺激性气味气体 | 浓硫酸具有脱水性和强氧化性,反应中生成C、 和 和 等 等 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列有关实验原理、方法和结论都正确的是
| A.向某溶液中加入盐酸酸化的氯化钡溶液有白色沉淀生成,该溶液不一定含SO42- |
| B.向蛋白质溶液中加入硫酸铜溶液,将得到的沉淀分离出来,再加水可重新溶解 |
| C.等体积的pH都为3的酸HA和HB分别与足量的Mg反应,HA放出的H2多,说明酸性:HA>HB |
| D.在硫酸钡中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列化学实验中的操作、现象及结论都正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向苯中滴入少量浓溴水,充分振荡,静置 | 下层接近无色 | 说明苯与溴发生了取代反应 |
| B | 向蛋白质溶液中加入适量CuSO4溶液并充分混合 | 溶液中有沉淀析出 | CuSO4溶液使蛋白质发生变性 |
| C | 向AgI沉淀中滴入KCl溶液 | 有白色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| D | 向适量淀粉溶液中加入少量稀硫酸,加热约5 min,冷却后再加入新制Cu(OH)2浊液并加热 | 混合液中无红色沉淀出现 | 说明淀粉没有发生水解反应生成葡萄糖 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】东北师范大学杜锡光教授曾表示“化学就是键”。化学研究的物质的变化实际上就是“键”的断裂和生成,物质是否稳定也取决于“键”的稳定性,甚至一些分子间作附力也被叫做“次级键”……关于化学键的相关内容,你认为以下描述符合 事实的是
| A.“头碰头”形成的键一定比“肩并肩”形成的键稳定 |
| B.只含非极性键的分子一定是非极性分子,因此臭氧是非极性分子 |
C. 是平面正三角形,是因为该粒子中键角为120°且所有共价键的键长相等 是平面正三角形,是因为该粒子中键角为120°且所有共价键的键长相等 |
| D.所有共价键都和氢键一样有方向性和饱和性 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】二氯二吡啶合铂分子是一种铂配合物,空间构型为平面四边形,有顺式和反式两种同分异构体(如图)。科学研究表明,顺式分子具有抗癌活性。下列说法错误的是
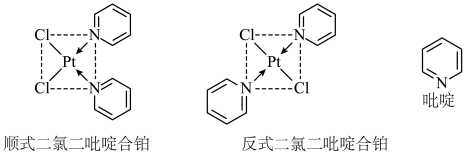
| A.二氯二吡啶合铂分子中铂为+2价 |
| B.顺式二氯二吡啶合铂分子的极性小于反式二氯二吡啶合铂 |
C.已知吡啶为平面形,可推知吡啶中N原子的杂化方式为 |
| D.吡啶分子中与Pt形成配位键的电子对位于N原子的p轨道上 |
您最近一年使用:0次

 (
( ,且
,且 为整数)型分子中,若中心原子没有孤对电子,则
为整数)型分子中,若中心原子没有孤对电子,则 、
、 、
、 分子中的
分子中的 分别形成2个、3个、4个键,故
分别形成2个、3个、4个键,故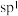 、
、 、
、 杂化
杂化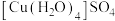 中,中心离子是
中,中心离子是 ,配体是
,配体是 ,配位数是1
,配位数是1

