随着原子序数的递增,7种短周期元素A~G的最高正价或最低负价与原子序数的关系如图。
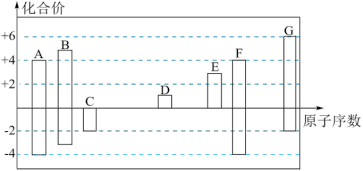
回答下列问题:
(1)写出中子数为8的A元素的一种核素的化学符号_______ 。
(2)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为_______ 。
(3)E元素最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式为_______ 。
(4)元素A与G形成的电子总数为38的分子的结构式为_______ 。
(5)元素C与D按原子个数比1:1形成的化合物的电子式为_______ ,所含有化学键类型有_______ 。
(6)如图表示由C、G元素组成的两种气体分子在一定条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:_______ 。
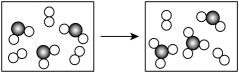

回答下列问题:
(1)写出中子数为8的A元素的一种核素的化学符号
(2)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为
(3)E元素最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式为
(4)元素A与G形成的电子总数为38的分子的结构式为
(5)元素C与D按原子个数比1:1形成的化合物的电子式为
(6)如图表示由C、G元素组成的两种气体分子在一定条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:

更新时间:2024-02-22 14:03:01
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】下表是元素周期表一部分,针对表中的①~⑧种元素,请按要求填写下列空白:
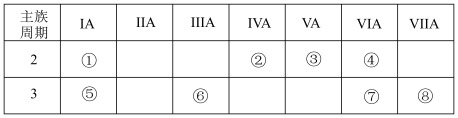
(1)在元素①⑤⑥对应的最高价氧化物对应水化物中,碱性最强的化合物电子式是:_______ 。
(2)④⑤⑥⑦四种元素的简单离子半径从大到小排序_______ (用离子符号表示)。
(3)写出元素⑥的最高价氧化物与元素⑤的最高价氧化物对应的水化物反应的离子反应方程式_______ 。
(4)写出元素③的常见氢化物和它的最高价氧化物对应的水化物反应的化学反应方程式_____ 。
(5)用电子式来表示⑤与⑦组成化合物的形成过程_______ 。

(1)在元素①⑤⑥对应的最高价氧化物对应水化物中,碱性最强的化合物电子式是:
(2)④⑤⑥⑦四种元素的简单离子半径从大到小排序
(3)写出元素⑥的最高价氧化物与元素⑤的最高价氧化物对应的水化物反应的离子反应方程式
(4)写出元素③的常见氢化物和它的最高价氧化物对应的水化物反应的化学反应方程式
(5)用电子式来表示⑤与⑦组成化合物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】某固体混合物中,可能含有 、
、 、
、 、
、 、
、 、
、 等离子,溶于水配成溶液,取两份该固体的溶液进行如图的实验:
等离子,溶于水配成溶液,取两份该固体的溶液进行如图的实验:
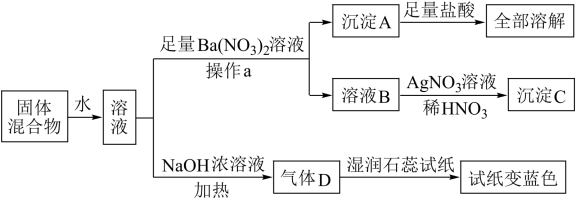
已知:氨气可以使湿润石蕊试纸变蓝色,请回答下列问题:
(1)操作a的名称是___________ 。
(2)沉淀A的化学式为___________ ,沉淀A加入足量的盐酸全部溶解的离子方程式为___________ 。
(3)生成沉淀C的的离子方程式为___________ 。
(4)混合物中,一定存在的离子有 和
和___________ ,一定不存在的离子有___________ ,可能存在的离子是___________ 。
 、
、 、
、 、
、 、
、 、
、 等离子,溶于水配成溶液,取两份该固体的溶液进行如图的实验:
等离子,溶于水配成溶液,取两份该固体的溶液进行如图的实验:
已知:氨气可以使湿润石蕊试纸变蓝色,请回答下列问题:
(1)操作a的名称是
(2)沉淀A的化学式为
(3)生成沉淀C的的离子方程式为
(4)混合物中,一定存在的离子有
 和
和
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】海水中含有丰富的化学资源,从海水中可提取多种化工原料。如图是某工厂对海水资源综合利用的示意图。

试回答下列问题:
(1)反应①、②、③、④中,属于氧化还原反应的是_________ 。
(2)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO 等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
a.向浓缩后的海水中加入过量的NaOH溶液;
b.向滤液中加过量的________ 溶液;
c.向滤液中加过量的________ 溶液,过滤;
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
(3)请写出反应③的离子方程式____ 。
(4)母液中通入氯气,还可以制备溴单质,工业以浓缩海水为原料提取溴的部分过程如图:
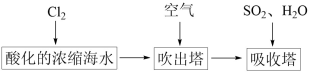
a.先通入Cl2的目的是(用离子方程式表示)__________ 。
b.吸收塔中发生反应的化学方程式是________ 。

试回答下列问题:
(1)反应①、②、③、④中,属于氧化还原反应的是
(2)海水中含有大量的NaCl,以及少量的Ca2+、Mg2+、SO
 等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:
等离子。为得到纯净的饱和NaCl溶液,进行了如下操作。请补全操作步骤:a.向浓缩后的海水中加入过量的NaOH溶液;
b.向滤液中加过量的
c.向滤液中加过量的
d.向滤液中加入足量的稀盐酸;
e.加热煮沸一段时间,得到饱和NaCl溶液。
(3)请写出反应③的离子方程式
(4)母液中通入氯气,还可以制备溴单质,工业以浓缩海水为原料提取溴的部分过程如图:

a.先通入Cl2的目的是(用离子方程式表示)
b.吸收塔中发生反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表为九种主族元素在周期表中的位置:
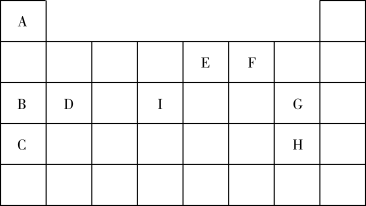
请回答下列问题:
(1)I元素的位置是第________ 周期,第______ 族。
(2)C、B、D 三种元素的金属性由强到弱的顺序为___________________ (填元素符号)。
(3)E、F两种元素对应的最简单氢化物的稳定性:________________ (填化学式)。
(4)C的单质与稀盐酸反应的离子方程式为_________________________ 。
(5)G 的单质气体通入H、C形成化合物的水溶液中,写出该反应的化学方程式:______

请回答下列问题:
(1)I元素的位置是第
(2)C、B、D 三种元素的金属性由强到弱的顺序为
(3)E、F两种元素对应的最简单氢化物的稳定性:
(4)C的单质与稀盐酸反应的离子方程式为
(5)G 的单质气体通入H、C形成化合物的水溶液中,写出该反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表为元素周期表得一部分。
回答下列问题:
(1)X元素在周期表中位于_____ 周期_______ 族。
(2)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是____________ 。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol Y单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(3)表中某元素的气态氢化物与该元素的最高价氧化物对应的水化物可以反应,写出该反应的化学方程式__________________ 。
(4)常温下,将稀氨水逐滴加入稀硫酸溶液中,当pH=7时,2c( )
)_______ c( )(填<、>、=)。
)(填<、>、=)。
(5)已知元素Na与元素Y可形成原子个数比为1∶1的离子化合物,写出该化合物的电子式_______ ,该化合物中的化学键类型有_____________ 。
(6)向Z单质的水溶液加入少量下列物质,能增强溶液漂白能力的是___________ 。
A.碳酸钙粉末 B.稀硫酸 C.氯化钙溶液 D.二氧化硫的水溶液
碳 | 氮 | Y | |
X | 硫 | Z |
(1)X元素在周期表中位于
(2)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1mol Y单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(3)表中某元素的气态氢化物与该元素的最高价氧化物对应的水化物可以反应,写出该反应的化学方程式
(4)常温下,将稀氨水逐滴加入稀硫酸溶液中,当pH=7时,2c(
 )
) )(填<、>、=)。
)(填<、>、=)。(5)已知元素Na与元素Y可形成原子个数比为1∶1的离子化合物,写出该化合物的电子式
(6)向Z单质的水溶液加入少量下列物质,能增强溶液漂白能力的是
A.碳酸钙粉末 B.稀硫酸 C.氯化钙溶液 D.二氧化硫的水溶液
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】X、Y、Z、W是原子序数依次增大的短周期主族元素,X、Y同主族且Y的单质可用于制造太阳能电池板,Z的族序数等于X的核外电子数。回答下列问题:
(1)Y、Z、W原子半径由大到小的顺序为_______ (用元素符号表示)。
(2) 在工业上可用作溶剂、制作粘胶纤维。500℃~700℃时,以Y的最高价含氧酸作催化剂,用X的简单氢化物和Z单质反应可制备
在工业上可用作溶剂、制作粘胶纤维。500℃~700℃时,以Y的最高价含氧酸作催化剂,用X的简单氢化物和Z单质反应可制备 ,同时生成Z的简单氢化物,此反应的化学方程式为
,同时生成Z的简单氢化物,此反应的化学方程式为___ 。
(3)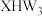 和
和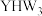 均是重要的化工原料,二者结构相似。
均是重要的化工原料,二者结构相似。
①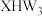 的电子式为
的电子式为_______ 。
②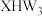 的沸点为
的沸点为 ,
,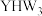 的沸点为
的沸点为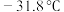 ,
,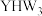 的沸点更高的原因为
的沸点更高的原因为_______ 。
③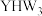 遇水时发生反应生成两种酸和
遇水时发生反应生成两种酸和 。有研究表明该反应分两步进行:
。有研究表明该反应分两步进行:
第一步: ;
;
第二步:_______ 请补全第二步反应的化学方程式(用元素符号表示)。
(4)Z和W的简单氢化物中热稳定性更好的是_______ (填化学式)。 中各原子最外层均满足8电子结构,
中各原子最外层均满足8电子结构, 中含有的共价键类型为
中含有的共价键类型为_______ 。
(1)Y、Z、W原子半径由大到小的顺序为
(2)
 在工业上可用作溶剂、制作粘胶纤维。500℃~700℃时,以Y的最高价含氧酸作催化剂,用X的简单氢化物和Z单质反应可制备
在工业上可用作溶剂、制作粘胶纤维。500℃~700℃时,以Y的最高价含氧酸作催化剂,用X的简单氢化物和Z单质反应可制备 ,同时生成Z的简单氢化物,此反应的化学方程式为
,同时生成Z的简单氢化物,此反应的化学方程式为(3)
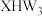 和
和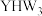 均是重要的化工原料,二者结构相似。
均是重要的化工原料,二者结构相似。①
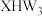 的电子式为
的电子式为②
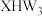 的沸点为
的沸点为 ,
,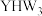 的沸点为
的沸点为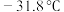 ,
,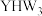 的沸点更高的原因为
的沸点更高的原因为③
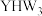 遇水时发生反应生成两种酸和
遇水时发生反应生成两种酸和 。有研究表明该反应分两步进行:
。有研究表明该反应分两步进行:第一步:
 ;
;第二步:
(4)Z和W的简单氢化物中热稳定性更好的是
 中各原子最外层均满足8电子结构,
中各原子最外层均满足8电子结构, 中含有的共价键类型为
中含有的共价键类型为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】如下图所示:在上述转化关系中,已知B、D都是淡黄色固体,且A与D可反应生成离子化合物A2D。回答:

(1)写出下列物质的化学式A._______ ,H._______ 。
(2)写出C的电子式_______ ,B中含有的化学键类型是____________
(3)写出E→F的化学方程式___________________ 。

(1)写出下列物质的化学式A.
(2)写出C的电子式
(3)写出E→F的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表为元素周期表的短周期区域一部分,回答下列问题:
(1)⑤的简单离子结构示意图为 ,此元素在周期表中的位置为
,此元素在周期表中的位置为________ ,同主族元素中,非金属性强于此元素的有___________ (填元素符号)。
(2)④与⑤组成的化合物常用于食品调味,用电子式表示此化合物的形成过程__________ 。
(3)②、③、④元素的简单离子半径由大到小的顺序为_________ (填离子符号)。
(4)由③、④组成的化合物中可能含有化学键的类型为_______________ 。
(5)②与③的简单氢化物稳定性更强的是_______ (填化学式)。
(6)设计实验证明②的非金属性强于①:____________________ 。
| ① | ② | ③ | ||||
| ④ | ⑤ |
 ,此元素在周期表中的位置为
,此元素在周期表中的位置为(2)④与⑤组成的化合物常用于食品调味,用电子式表示此化合物的形成过程
(3)②、③、④元素的简单离子半径由大到小的顺序为
(4)由③、④组成的化合物中可能含有化学键的类型为
(5)②与③的简单氢化物稳定性更强的是
(6)设计实验证明②的非金属性强于①:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)E在周期表中的位置为第_____ 周期第_____ 族;
(2)B元素形成的最高价氧化物的化学式为_____ ;
(3)化合物D2C2中所含的化学键类型是_____ ;
(4)元素C、D、E形成的简单离子半径大小关系是_____ (用离子符号表示);
(5)由A、B、C三种元素形成的离子化合物的化学式为_____ ,它与强碱溶液共热,发生反应的离子方程式是_____ 。
(1)E在周期表中的位置为第
(2)B元素形成的最高价氧化物的化学式为
(3)化合物D2C2中所含的化学键类型是
(4)元素C、D、E形成的简单离子半径大小关系是
(5)由A、B、C三种元素形成的离子化合物的化学式为
您最近一年使用:0次




