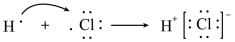三氟化氯(ClF3)是极强助燃剂,能自耦电离:2ClF3 ClF
ClF +ClF
+ClF ,其分子空间结构如图。下列推测合理的是
,其分子空间结构如图。下列推测合理的是
 ClF
ClF +ClF
+ClF ,其分子空间结构如图。下列推测合理的是
,其分子空间结构如图。下列推测合理的是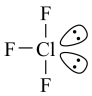
| A.ClF3分子是含有极性键的非极性分子 |
| B.BrF3比ClF3更易发生自耦电离 |
| C.ClF3水解反应的产物为HCl和HFO |
D.ClF 与H2O、ClF 与H2O、ClF 与CCl4的空间结构分别相同 与CCl4的空间结构分别相同 |
更新时间:2024-02-20 19:02:29
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列推断正确的是
A.CO 是三角锥形分子 是三角锥形分子 |
B.NH 的电子式: 的电子式: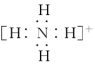 ,离子呈平面形结构 ,离子呈平面形结构 |
| C.CH4分子中的4个C-H键都是氢原子的1s轨道与碳原子的p轨道形成的s-pσ键 |
| D.CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个C-H σ键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】科研人员利用高压 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位,下列说法正确的是
气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位,下列说法正确的是
 气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位,下列说法正确的是
气流将水微滴喷射到涂覆催化剂的石墨网上,研究常温制氨,其反应历程中微粒转化关系如图1,相对能量变化关系如图2,图中“*”表示催化剂表面吸附位,下列说法正确的是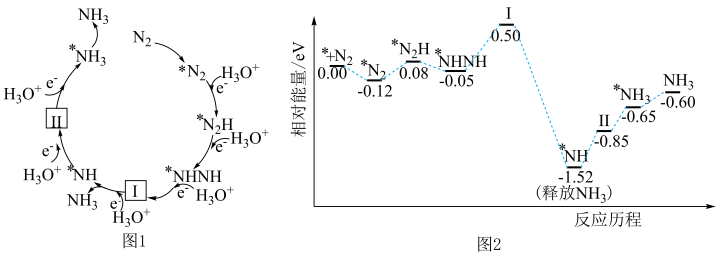
A. 与 与 的 的 模型不相同 模型不相同 |
B. 过程中存在极性键和非极性键的断裂与形成 过程中存在极性键和非极性键的断裂与形成 |
C.反应历程中放热最多的反应是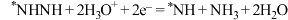 |
D.总反应为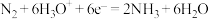 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的有个
①价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数
②所有σ键强度都大于π键
③杂化轨道只用于形成共价键
④只要分子的空间结构为平面三角形,中心原子均为sp2杂化
⑤NH3与H3O+的VSEPR构型均为四面体形,二者空间结构一致
⑥p能级能量一定比s能级的能量高
①价层电子对互斥模型中,π键电子对数不计入中心原子的价层电子对数
②所有σ键强度都大于π键
③杂化轨道只用于形成共价键
④只要分子的空间结构为平面三角形,中心原子均为sp2杂化
⑤NH3与H3O+的VSEPR构型均为四面体形,二者空间结构一致
⑥p能级能量一定比s能级的能量高
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于物质结构的说法错误几项是
① 的空间结构为四面体形
的空间结构为四面体形
②基态氮原子有7种能量不同的电子,电子有5种空间运动状态
③ 表示处于激发态的B的电子排布图
表示处于激发态的B的电子排布图
④甲醛( )和光气(
)和光气( )分子中的键角
)分子中的键角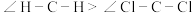
⑤含有非极性键的分子一定是非极性分子
⑥氢键的存在一定能使物质的熔、沸点升高
⑦ 、
、 、
、 均易溶于水的原因之一是与
均易溶于水的原因之一是与 均能形成氢键
均能形成氢键
⑧ 的沸点高于
的沸点高于
⑨只要分子的空间结构为平面三角形,中心原子均为 杂化
杂化
⑩ 分子中
分子中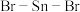 的键角
的键角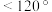
①
 的空间结构为四面体形
的空间结构为四面体形②基态氮原子有7种能量不同的电子,电子有5种空间运动状态
③
 表示处于激发态的B的电子排布图
表示处于激发态的B的电子排布图④甲醛(
 )和光气(
)和光气( )分子中的键角
)分子中的键角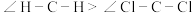
⑤含有非极性键的分子一定是非极性分子
⑥氢键的存在一定能使物质的熔、沸点升高
⑦
 、
、 、
、 均易溶于水的原因之一是与
均易溶于水的原因之一是与 均能形成氢键
均能形成氢键⑧
 的沸点高于
的沸点高于
⑨只要分子的空间结构为平面三角形,中心原子均为
 杂化
杂化⑩
 分子中
分子中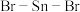 的键角
的键角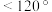
| A.三项 | B.四项 | C.五项 | D.六项 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】COCl2又称为光气,是一种重要的有机试剂,其结构如图,下列关于COCl2的说法不正确 的是
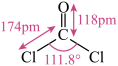
| A.它是一个非极性分子 |
| B.碳原子的杂化方式为sp2 |
| C.C=O与C—Cl间的排斥大于两个C—Cl间的排斥 |
| D.C—Cl键长更长与Cl原子半径较大、C—Cl键是单键有关 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于氮、磷、砷的单质及化合物的说法正确的是


A.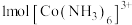 中含有 中含有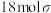 键 键 |
B.白磷分子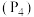 是极性分子,白磷可保存在水中 是极性分子,白磷可保存在水中 |
C.肼 的沸点为113.5℃,说明肼分子间可能存在氢键 的沸点为113.5℃,说明肼分子间可能存在氢键 |
| D.砷化镓的晶胞结构如图所示,镓原子配位数为8 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】第VA族元素的原子可与Cl结合形成NCl3、AsCl3、AsCl5等分子。化合价为+3的铬的卤化物有CrF3、CrCl3等,制备三氯化铬的主要反应式为Cr2O3+3CCl4 2CrCl3+3COCl2。CrCl3溶于水得到的配合物为[Cr(H2O)4Cl2]Cl。已知CrCl3、CrF3的熔点依次为83℃、1100℃。下列有关物质的说法正确的是
2CrCl3+3COCl2。CrCl3溶于水得到的配合物为[Cr(H2O)4Cl2]Cl。已知CrCl3、CrF3的熔点依次为83℃、1100℃。下列有关物质的说法正确的是
 2CrCl3+3COCl2。CrCl3溶于水得到的配合物为[Cr(H2O)4Cl2]Cl。已知CrCl3、CrF3的熔点依次为83℃、1100℃。下列有关物质的说法正确的是
2CrCl3+3COCl2。CrCl3溶于水得到的配合物为[Cr(H2O)4Cl2]Cl。已知CrCl3、CrF3的熔点依次为83℃、1100℃。下列有关物质的说法正确的是| A.[Cr(H2O)4Cl2]Cl的中心离子配位数为7 |
| B.CCl4是极性键形成的非极性分子 |
| C.CrCl3和CrF3晶体类型相同 |
| D.1mol[Cr(H2O)4Cl2]Cl和足量硝酸银溶液反应生成3molAgCl |
您最近一年使用:0次