已知反应① 和②
和② 。下列说法错误的是
。下列说法错误的是
 和②
和② 。下列说法错误的是
。下列说法错误的是A.反应①中氧化产物与还原产物均为 |
B.反应①中 具有遇淀粉溶液变蓝的特性 具有遇淀粉溶液变蓝的特性 |
C.反应②中 是导致酸雨的主要有害污染物 是导致酸雨的主要有害污染物 |
D.由反应①和②可判断氧化性: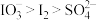 |
更新时间:2024-02-26 12:30:39
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】N2F4可作高能燃料的氧化剂,它可由以下反应制得:HNF2+Fe3+→N2F4↑+Fe2++H+(未配平)。下列说法错误的是
| A.N2F4分子中N-F键键角小于N2H4分子中N-H键键角 |
| B.上述反应中,氧化剂与还原剂的物质的量之比为1:1 |
| C.若生成标准状况下2.24LN2F4,转移电子0.2mol |
| D.N2F4作氧化剂时,其还原产物可能是N2和HF |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于反应3Cl2+6NaOH 5NaCl+NaClO3+3H2O,以下叙述正确的是
5NaCl+NaClO3+3H2O,以下叙述正确的是
 5NaCl+NaClO3+3H2O,以下叙述正确的是
5NaCl+NaClO3+3H2O,以下叙述正确的是| A.Cl2是氧化剂, NaOH是还原剂 |
| B.氧化剂得电子数与还原剂失电子数之比为1∶1 |
| C.NaCl是氧化产物 |
| D.被氧化的氯原子和被还原的氯原子的个数之比为1∶1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】如图两烧杯中盛有等体积的盐溶液,关于给出的原电池说法错误的是


| A.电子从铁电极流向石墨电极,盐桥中阴离子迁移向右侧烧杯 |
| B.电池总反应为Fe+2Fe3+=3Fe2+ |
| C.若测得铁电极溶液中c(Fe2+)增加了0.02mol·L-1,可知,石墨电极溶液中c(Fe2+)=0.09mol·L-1 |
| D.此实验验证了Fe2+氧化性小于Fe3+,还原性小于Fe |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】V2O5是工业上重要的化工原料。V2O5溶解在浓盐酸中的产物为VO2+和气体单质X,该气体可用FeCl2溶液吸收。下列关于V2O5溶解在浓盐酸中的反应的说法正确的是
| A.该反应中还原剂是V2O5 |
| B.氧化剂和还原剂的物质的量之比为2:1 |
| C.根据上述信息可判断氧化性:V2O5>X>FeCl2 |
| D.每生成1 mol VO2+,可产生11.2 L气体X |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列各物质久置于空气中,所选用的试剂或操作不可鉴别其是否变质的是
| 选项 | 物质 | 试剂或操作 |
| A |  溶液 溶液 | 稀盐酸 |
| B |  溶液 溶液 | 淀粉溶液 |
| C |  溶液 溶液 | 氯化钡溶液 |
| D | 无水硫酸铜粉末 | 观察颜色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
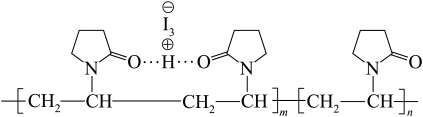
【推荐2】聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与 形成聚维酮碘,其结构表示如图(图中虚线表示氢键),下列说法
形成聚维酮碘,其结构表示如图(图中虚线表示氢键),下列说法不正确 的是
 形成聚维酮碘,其结构表示如图(图中虚线表示氢键),下列说法
形成聚维酮碘,其结构表示如图(图中虚线表示氢键),下列说法
A.聚维酮的单体是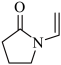 |
B.聚维酮分子由 个单体加聚而成 个单体加聚而成 |
C. 该聚维酮碘分子在 该聚维酮碘分子在 溶液中完全反应,消耗 溶液中完全反应,消耗 |
| D.聚维酮碘的水溶液遇淀粉能发生显色反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学实验小组同学用如图所示装置进行氯气系列实验以探究其性质,气体X是Cl2(部分仪器已略去),下列说法不正确的是( )
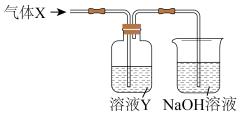

| A.若溶液Y为KI淀粉溶液,则可观察到广口瓶中溶液变蓝的实验现象 |
| B.X与NaOH溶液反应既体现其氧化性又体现其还原性 |
| C.若溶液Y为NaBr溶液,则可观察到广口瓶中溶液变蓝的实验现象 |
| D.若溶液Y为NaBr溶液,取广口瓶中反应后的溶液于试管中滴加几滴KI淀粉溶液观察到溶液变蓝,不能证明氧化性:Br2>I2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】硫酸是当今世界上最重要的化工产品之一、目前工业制备硫酸主要采用接触法,常见的有硫铁矿制酸、硫磺制酸等。以硫铁矿 ( )为原料制备硫酸的主要设备有:沸腾炉、接触室、吸收塔。硫酸工业、金属冶炼产生的尾气中含有
)为原料制备硫酸的主要设备有:沸腾炉、接触室、吸收塔。硫酸工业、金属冶炼产生的尾气中含有 ,需经回收利用处理才能排放到空气中。下列有关硫铁矿为原料制备硫酸说法
,需经回收利用处理才能排放到空气中。下列有关硫铁矿为原料制备硫酸说法不正确 的是
 )为原料制备硫酸的主要设备有:沸腾炉、接触室、吸收塔。硫酸工业、金属冶炼产生的尾气中含有
)为原料制备硫酸的主要设备有:沸腾炉、接触室、吸收塔。硫酸工业、金属冶炼产生的尾气中含有 ,需经回收利用处理才能排放到空气中。下列有关硫铁矿为原料制备硫酸说法
,需经回收利用处理才能排放到空气中。下列有关硫铁矿为原料制备硫酸说法| A.将原料硫铁矿经过粉碎后投入沸腾炉 |
| B.产生的气体无需除尘净化可直接通入接触室 |
C.用98.3%浓硫酸代替水吸收 |
D.金属冶炼产生的含 的废气经回收也可用于制硫酸 的废气经回收也可用于制硫酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在探究某地刚落下的酸雨成分的实验中,下列根据实验现象得出的结论不正确的是
A.在酸雨试样中加入 溶液有白色沉淀,说明酸雨中一定含 溶液有白色沉淀,说明酸雨中一定含 |
B.将酸雨试样浓缩后加入Cu和浓 ,试管口有红棕色气体逸出,说明酸雨中可能含 ,试管口有红棕色气体逸出,说明酸雨中可能含 |
C.每隔1h测定酸雨试样的pH,其pH先变小后不变,说明刚落下的酸雨中含 |
D.用铂丝蘸取酸雨,在酒精灯上灼烧,火焰呈黄色,说明酸雨中一定存在 |
您最近一年使用:0次

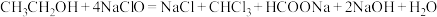 。已知:
。已知: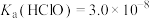 ,
,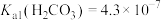 ,
, 。下列说法正确的是
。下列说法正确的是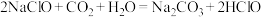
 中含有
中含有 个C原子
个C原子 ,转移
,转移 个电子
个电子

