X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为 ,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
(1)元素X的最高价氧化物的电子式为___________ ;元素Z的离子结构示意图为___________ 。
(2)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为___________ 。
(3)元素W位于周期表的第___________ 族,其非金属性比R弱,用原子结构的知识解释原因:___________ 。
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液做该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的离子方程式:___________ 。
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为 ,则该反应的化学方程式为
,则该反应的化学方程式为___________ 。
 ,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:(1)元素X的最高价氧化物的电子式为
(2)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为
(3)元素W位于周期表的第
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液做该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的离子方程式:
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为
 ,则该反应的化学方程式为
,则该反应的化学方程式为
更新时间:2024-04-03 15:40:34
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】表中列出了①~⑩九种元素在周期表中的位置。
请按要求回答下列问题:
(1)①~⑩十种元素中非金属性最强的是_______ (填元素符号)。元素②在元素周期表中的位置为_______
(2)元素⑧的原子结构示意图是_______ ;由①、④、⑥三种元素组成的化合物,其电子式是_______ 。
(3)元素②、⑧的气态氢化物的稳定性较强的是_______ (填化学式);元素③的一种核素核内的中子数与质子数相等,则该种核素可以表示为_______ ;
(4)③、④、⑧三种元素的原子半径由大到小的顺序是_______ (填元素符号)。
(5)用电子式表示⑤、⑥组成的化合物的形成过程_______ 。
(6)元素⑥的最高价氧化物对应的水化物与元素⑩的最高价氧化物对应的水化物反应的化学方程式是_______ 。
(7)用一实验事实能说明⑩元素的非金属性比⑨元素的非金属性强的是_______ (用化学方程式表示)
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(1)①~⑩十种元素中非金属性最强的是
(2)元素⑧的原子结构示意图是
(3)元素②、⑧的气态氢化物的稳定性较强的是
(4)③、④、⑧三种元素的原子半径由大到小的顺序是
(5)用电子式表示⑤、⑥组成的化合物的形成过程
(6)元素⑥的最高价氧化物对应的水化物与元素⑩的最高价氧化物对应的水化物反应的化学方程式是
(7)用一实验事实能说明⑩元素的非金属性比⑨元素的非金属性强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图表示由短周期元素组成的些物质之间的转化关系(某些反应产物或条件已略去)。各方框表示有关的一种反应物或生成物(某些物质已经略去),其中A、B、D在常温下均为无色无刺激性气味的气体,C是使湿润的红色石蕊试纸变蓝的气体,M是最常见的无色液体。

(1)物质F的化学式___ 。
(2)物质C的电子式___ 。
(3)写出C→E的化学方程式___ 。
(4)写出G→E的离子方程式___ 。

(1)物质F的化学式
(2)物质C的电子式
(3)写出C→E的化学方程式
(4)写出G→E的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】一种由粗铋(Bi:97.88%,Pb:1.69%,Cu:0.427%,其他不与硝酸反应的难溶性物质:0.003%)制备高纯铋的氧化物的工艺流程如图所示。

已知:滤液1的主要成分为 ,还含有少量的
,还含有少量的 、
、 。
。
回答下列问题:
(1)将粗铋熔化后水淬成颗粒状的目的为______ 。
(2)操作a的名称为______ 。
(3)加入碳酸铵溶液调pH时应对溶液进行适当加热的原因为_____ ,加热时温度不宜过高的原因为______ 。
(4)加入氨水—碳酸铵溶液后可使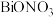 转化为
转化为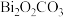 ,对应的化学方程式为
,对应的化学方程式为______ 。
(5)采用热重法分析碳酸氧铋(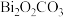 )(摩尔质量为
)(摩尔质量为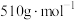 )“煅烧”时的分解产物,测得样品煅烧时固体残留率(
)“煅烧”时的分解产物,测得样品煅烧时固体残留率(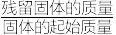
 )随温度的变化始质图所示,则流程图中“煅烧”所得“产品”的化学式和所得“气体”的电子式分别为
)随温度的变化始质图所示,则流程图中“煅烧”所得“产品”的化学式和所得“气体”的电子式分别为______ 、______ 。

(6)流程图中所示“产品”也可以通过直接煅烧硝酸氧铋制得,该方案的缺点是______ 。

已知:滤液1的主要成分为
 ,还含有少量的
,还含有少量的 、
、 。
。回答下列问题:
(1)将粗铋熔化后水淬成颗粒状的目的为
(2)操作a的名称为
(3)加入碳酸铵溶液调pH时应对溶液进行适当加热的原因为
(4)加入氨水—碳酸铵溶液后可使
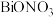 转化为
转化为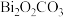 ,对应的化学方程式为
,对应的化学方程式为(5)采用热重法分析碳酸氧铋(
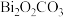 )(摩尔质量为
)(摩尔质量为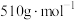 )“煅烧”时的分解产物,测得样品煅烧时固体残留率(
)“煅烧”时的分解产物,测得样品煅烧时固体残留率(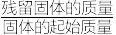
 )随温度的变化始质图所示,则流程图中“煅烧”所得“产品”的化学式和所得“气体”的电子式分别为
)随温度的变化始质图所示,则流程图中“煅烧”所得“产品”的化学式和所得“气体”的电子式分别为
(6)流程图中所示“产品”也可以通过直接煅烧硝酸氧铋制得,该方案的缺点是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度大,电绝缘性好,化学性质稳定,但生产成本较高。不溶于酸(氢氟酸除外)。高温下氧气及水蒸气能明显腐蚀氮化硅。一种用工业硅(含少量铁、铜的单质及氧化物)和 (含少量
(含少量 )合成氮化硅的工艺流程如下:
)合成氮化硅的工艺流程如下: 净化时,铜屑的作用是
净化时,铜屑的作用是_______ ;硅胶的作用是_______ 。
(2) 可能是
可能是_______ (选填:“盐酸”、“硝酸”、“硫酸”、“氢氟酸”)。
(3)如何说明氮化硅产品已用水洗干净?_______ 。
(4)推测氮化硅可能有哪些用途:_______ (填字母)。
a. 制作切削刀具 b. 制作坩埚 c. 制作耐高温轴承
(5)工业上还可以采用化学气相沉积法,在 的环境中,使
的环境中,使 与
与 在高温下反应生成
在高温下反应生成 沉积在石墨表面,该反应的化学方程式为
沉积在石墨表面,该反应的化学方程式为_______ 。
 (含少量
(含少量 )合成氮化硅的工艺流程如下:
)合成氮化硅的工艺流程如下:
 净化时,铜屑的作用是
净化时,铜屑的作用是(2)
 可能是
可能是(3)如何说明氮化硅产品已用水洗干净?
(4)推测氮化硅可能有哪些用途:
a. 制作切削刀具 b. 制作坩埚 c. 制作耐高温轴承
(5)工业上还可以采用化学气相沉积法,在
 的环境中,使
的环境中,使 与
与 在高温下反应生成
在高温下反应生成 沉积在石墨表面,该反应的化学方程式为
沉积在石墨表面,该反应的化学方程式为
您最近一年使用:0次
【推荐2】某小组实验验证“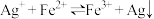 ”为可逆反应并测定其平衡常数。
”为可逆反应并测定其平衡常数。
(1)实验验证
实验Ⅰ:将0.0100mol/L 溶液与0.0400mol/L
溶液与0.0400mol/L 溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液呈黄色。
溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液呈黄色。
实验Ⅱ:向少量Ag粉中加入0.0100mol/L 溶液(pH=1),固体完全溶解。
溶液(pH=1),固体完全溶解。
①取Ⅰ中沉淀,加入浓硝酸,证实沉淀为Ag。现象是_______ 。
②Ⅱ中溶液选用 ,不选用
,不选用 的原因是
的原因是_______ 。
综合上述实验,证实“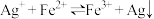 ”为可逆反应。
”为可逆反应。
(2)测定平衡常数
实验Ⅲ:一定温度下,待实验Ⅰ中反应达到平衡状态时,取v mL上层清液,用c1 mol/L KSCN标准溶液滴定 ,至出现稳定的浅红色时,消耗KSCN标准溶液v1 mL。
,至出现稳定的浅红色时,消耗KSCN标准溶液v1 mL。
资料: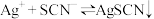 (白色)K=1012
(白色)K=1012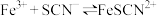 (红色) K
(红色) K
①滴定过程中 的作用是
的作用是_______ 。
②测得平衡常数K=_______ 。
(3)思考问题
①不用实验Ⅱ中清液测定K的原因是_______ 。
②取实验Ⅰ的浊液测定c( ),会使所测K值
),会使所测K值_______ (填“偏高”“偏低”或“不受影响”)。
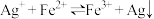 ”为可逆反应并测定其平衡常数。
”为可逆反应并测定其平衡常数。(1)实验验证
实验Ⅰ:将0.0100mol/L
 溶液与0.0400mol/L
溶液与0.0400mol/L 溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液呈黄色。
溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液呈黄色。实验Ⅱ:向少量Ag粉中加入0.0100mol/L
 溶液(pH=1),固体完全溶解。
溶液(pH=1),固体完全溶解。①取Ⅰ中沉淀,加入浓硝酸,证实沉淀为Ag。现象是
②Ⅱ中溶液选用
 ,不选用
,不选用 的原因是
的原因是综合上述实验,证实“
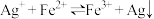 ”为可逆反应。
”为可逆反应。(2)测定平衡常数
实验Ⅲ:一定温度下,待实验Ⅰ中反应达到平衡状态时,取v mL上层清液,用c1 mol/L KSCN标准溶液滴定
 ,至出现稳定的浅红色时,消耗KSCN标准溶液v1 mL。
,至出现稳定的浅红色时,消耗KSCN标准溶液v1 mL。资料:
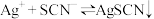 (白色)K=1012
(白色)K=1012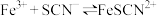 (红色) K
(红色) K①滴定过程中
 的作用是
的作用是②测得平衡常数K=
(3)思考问题
①不用实验Ⅱ中清液测定K的原因是
②取实验Ⅰ的浊液测定c(
 ),会使所测K值
),会使所测K值
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】亚硝酰氯( ,熔点为
,熔点为 ℃,沸点为
℃,沸点为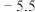 ℃)是一种红褐色液体或黄色气体,遇水反现生成一种氢化物和两种氧化物,可用于合成清洁剂、触媒剂及中间体等。某学习小组在实验室中用
℃)是一种红褐色液体或黄色气体,遇水反现生成一种氢化物和两种氧化物,可用于合成清洁剂、触媒剂及中间体等。某学习小组在实验室中用 和NO制备
和NO制备 。请回答下列问题:
。请回答下列问题:
(1)原料气NO和 的制备。
的制备。___________ 。实验室制备NO的反应的离子方程式为___________ 。
②实验室制备 可选择图中的装置
可选择图中的装置___________ (填标号);制备并收集干燥的 的装置连接顺序:a→
的装置连接顺序:a→___________ (按气流方向,用小写字母表示)。
(2)利用制得的NO和 制备亚硝酰氯
制备亚硝酰氯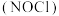 ,装置如图所示。
,装置如图所示。 外,另一个作用是
外,另一个作用是___________ 。
②装置Ⅳ的作用是___________ ;若无装置V,则装置Ⅳ中 可能发生反应的化学方相式为
可能发生反应的化学方相式为___________ 。
③查阅资料知,王水是浓硝酸与浓盐酸的混合酸,一定条件下该混合酸可自身反应生成亚硝酰氯、氯气和水,该反应的化学方程式为___________ 。
 ,熔点为
,熔点为 ℃,沸点为
℃,沸点为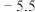 ℃)是一种红褐色液体或黄色气体,遇水反现生成一种氢化物和两种氧化物,可用于合成清洁剂、触媒剂及中间体等。某学习小组在实验室中用
℃)是一种红褐色液体或黄色气体,遇水反现生成一种氢化物和两种氧化物,可用于合成清洁剂、触媒剂及中间体等。某学习小组在实验室中用 和NO制备
和NO制备 。请回答下列问题:
。请回答下列问题:(1)原料气NO和
 的制备。
的制备。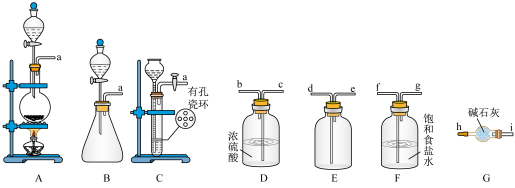
②实验室制备
 可选择图中的装置
可选择图中的装置 的装置连接顺序:a→
的装置连接顺序:a→(2)利用制得的NO和
 制备亚硝酰氯
制备亚硝酰氯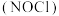 ,装置如图所示。
,装置如图所示。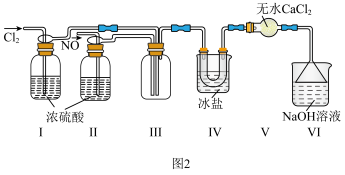
 外,另一个作用是
外,另一个作用是②装置Ⅳ的作用是
 可能发生反应的化学方相式为
可能发生反应的化学方相式为③查阅资料知,王水是浓硝酸与浓盐酸的混合酸,一定条件下该混合酸可自身反应生成亚硝酰氯、氯气和水,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】SO2直接排放会形成酸雨,危害环境。某化学实验小组用如图所示装置进行有关SO2性质的探究活动。___________ 。
(2)选用以上装置和药品探究亚硫酸与次氯酸的酸性强弱,甲同学认为按照A→C→F→尾气处理顺序连接装置可以证明,乙同学认为该方案不合理,其理由是___________ 。正确的连接顺序是:A→C→___________ (填字母)→尾气处理。证明亚硫酸的酸性强于次氯酸的酸性的实验现象是___________ 。
(3)利用如图所示的装置研究SO2的性质:(熔点:SO2 -76.1℃ SO3 16.8℃ 沸点: SO2 -10℃ SO3 45℃___________ ;装置Ⅲ中溶液逐渐褪色,则该反应的离子方程式是___________ 。
②乙同学按Ⅰ、Ⅱ、Ⅳ的顺序连接装置,若装置Ⅳ中有40 mL2.5 mol/LNaOH溶液,反应后增重4.8 g,则装置Ⅳ中发生总反应的化学方程式___________ 。
(4)该实验小组的学生丁用200 mL0.1 mol/L酸性 KMnO4溶液测定空气中:SO2含量,若气体流速为a cm3/min,当时间为t min时酸性KMnO4溶液恰好褪色,则空气中SO2的含量为___________ (g/cm3)。

(2)选用以上装置和药品探究亚硫酸与次氯酸的酸性强弱,甲同学认为按照A→C→F→尾气处理顺序连接装置可以证明,乙同学认为该方案不合理,其理由是
(3)利用如图所示的装置研究SO2的性质:(熔点:SO2 -76.1℃ SO3 16.8℃ 沸点: SO2 -10℃ SO3 45℃
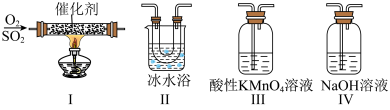
②乙同学按Ⅰ、Ⅱ、Ⅳ的顺序连接装置,若装置Ⅳ中有40 mL2.5 mol/LNaOH溶液,反应后增重4.8 g,则装置Ⅳ中发生总反应的化学方程式
(4)该实验小组的学生丁用200 mL0.1 mol/L酸性 KMnO4溶液测定空气中:SO2含量,若气体流速为a cm3/min,当时间为t min时酸性KMnO4溶液恰好褪色,则空气中SO2的含量为
您最近一年使用:0次
【推荐2】回答下列问题:
(1)用下图装置制备纯净的SO2发生装置中反应的化学方程式为___________ ,装置的连接顺序为:a→___________ (按气流方向,用小写字母表示)。
+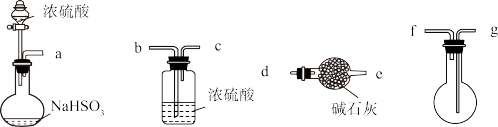
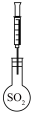
(2)用如图装置探究SO2的性质。限选试剂:NaOH溶液、稀H2SO4、H2O2溶液、FeCl3溶液、淀粉 - KI 溶液、新制H2S溶液。
(3)工业上利用硫酸厂烧渣(主要成分为Fe2O3,还含有少量FeS、SiO2等)制备绿矾的流程如下(其中所加试剂均过量):
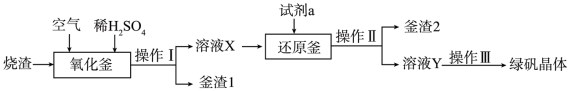
已知“釜渣 I ”中存在淡黄色固体颗粒,则“釜渣 1”主要成分为___________ ,生成该淡黄色固体反应的离子方程式为___________ 。“试剂 a”是一种单质,其名称为___________ ,其作用是 ___________ 。
(1)用下图装置制备纯净的SO2发生装置中反应的化学方程式为
+
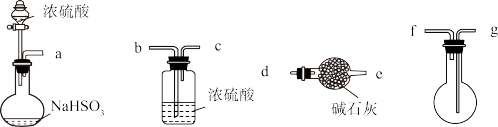
(2)用如图装置探究SO2的性质。限选试剂:NaOH溶液、稀H2SO4、H2O2溶液、FeCl3溶液、淀粉 - KI 溶液、新制H2S溶液。

| 操作步骤 | 实验现象 | 解释原因 |
| 用注射器将新制H2S溶液注入充满SO2的烧瓶中 | 产生淡黄色浑浊 | +4价S具有 |
| 用注射器将 | +4价S具有还原性,反应的离子方程式为 |

已知“釜渣 I ”中存在淡黄色固体颗粒,则“釜渣 1”主要成分为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】吊白块(NaHSO2•HCHO•2H2O,次硫酸氢钠甲醛)是易溶于水的白色块状或结晶性粉状固体,在印染工业中被用作拔染剂和还原剂。可由Na2S2O5 (焦亚硫酸钠)、甲醛及锌粉反应制取,回答下列问题:
(1)已知在pH=4.1时的过饱和NaHSO3溶液将自动脱水生成Na2S2O5,制备原料Na2S2O5的装置如下。
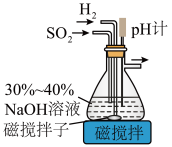
①通入H2的目的是______ 。
②吸滤瓶中先后发生的反应为_______ 、2NaHSO3=Na2S2O5↓+H2O。
③从环境保护和安全考虑,下列尾气处理方法正确的是________ (填标号)。
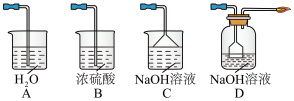
④实验室用稀NaOH溶液不能制得Na2S2O5,是因为_______ 。
(2)制备吊白块的装置(夹持及加热装置已略)如图:
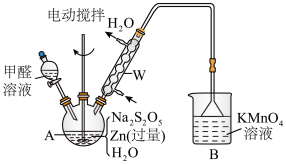
①仪器A的名称是_________ 。
②制备反应需在950C下进行,合适的加热方式是_____ ,A中发生反应的化学方程式为_____ (Zn转化为等物质的量的ZnO和Zn(OH)2)。
③从A中的悬浊液中得到产品吊白块的实验操作是_________ 及干燥。
(1)已知在pH=4.1时的过饱和NaHSO3溶液将自动脱水生成Na2S2O5,制备原料Na2S2O5的装置如下。

①通入H2的目的是
②吸滤瓶中先后发生的反应为
③从环境保护和安全考虑,下列尾气处理方法正确的是

④实验室用稀NaOH溶液不能制得Na2S2O5,是因为
(2)制备吊白块的装置(夹持及加热装置已略)如图:

①仪器A的名称是
②制备反应需在950C下进行,合适的加热方式是
③从A中的悬浊液中得到产品吊白块的实验操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】[探究实验一] 某同学探究同周期主族元素性质递变规律时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系):
请你帮助该同学整理并完成实验报告。
(1)实验目的:探究同周期主族元素性质递变规律。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液。仪器:①______ ,②_______ ,③_______ ,试管夹,镊子,小刀,玻璃片,砂纸,酒精灯等。
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)_______
(4)若用最高价氧化物的水化物的碱性相对强弱来验证Mg、Al失电子能力的强弱,请你设计实验(实验用品自选,不要求写化学方程式):
________________________________________________________________________________________ ;
(5)实验结论:___________________________________________________ ;
[探究实验二] 一定条件下,氯化镁与四氯化钛的混合物可作烯烃聚合反应
的催化剂。为了探究温度、氯化镁固体的含水量以及粉碎方式对该催化剂催化
效果的影响,设计如下对比实验:
(注:催化效果用单位时间内每克催化剂得到产品的质量来表示)
(6)表中 =
=__________________ ;
(7)从实验1、2可以得出的结论是:______________________________________________________ ;
(8)设计实验2、3的目的是:___________________________________________________ 。
| 实验步骤 | 实验现象 |
| 1.将镁条用砂纸打磨后,放入沸水中;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,做不定向运动,随之消失,溶液变成红色. |
| 2.向新制得的Na2S溶液中滴加少量新制的氯水 | B.有气体产生,溶液变成浅红色 |
| 3.将一小块金属钠放入滴有酚酞溶液的冷水中 | C.剧烈反应,迅速产生大量无色气体. |
| 4.将镁条投入稀盐酸中 | D.反应不十分剧烈,产生无色气体 |
| 5.将铝条投入稀盐酸中 | E.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告。
(1)实验目的:探究同周期主族元素性质递变规律。
(2)实验用品:试剂:金属钠,镁条,铝条,稀盐酸,新制氯水,新制Na2S溶液。仪器:①
(3)实验内容:(填写与实验步骤对应的实验现象的编号和离子方程式)
| 实验内容 | 实验现象 | 离子方程式 |
| 1 | ||
| 2 | ||
| 3 | ||
| 4 | ||
| 5 |
(4)若用最高价氧化物的水化物的碱性相对强弱来验证Mg、Al失电子能力的强弱,请你设计实验(实验用品自选,不要求写化学方程式):
(5)实验结论:
[探究实验二] 一定条件下,氯化镁与四氯化钛的混合物可作烯烃聚合反应
的催化剂。为了探究温度、氯化镁固体的含水量以及粉碎方式对该催化剂催化
效果的影响,设计如下对比实验:
| 实验 序号 | 氯化镁固体中氯元素含量/% | 温度/℃ | 粉碎方式/ | 催化效果/g·g-1 |
| 1 | 70.97 | 20 | 滚动球磨 | 3.9×104 |
| 2 | 74.45 | 20 | 滚动球磨 | 5.0×104 |
| 3 | 74.45 | 20 | 振动球磨 | 5.9×104 |
| 4 |  | 100 | 振动球磨 |
(注:催化效果用单位时间内每克催化剂得到产品的质量来表示)
(6)表中
 =
=(7)从实验1、2可以得出的结论是:
(8)设计实验2、3的目的是:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】下表为元素周期表的一部分,请针对元素①-⑨用相应的化学用语回答下列问题:
(1)化学性质最不活泼的元素是____ (填元素符号),非金属性最强的单质是____ (填化学式)。
(2)③、⑤的原子半径较小的是_____ (填元素符号)。
(3)①、②的最高价氧化物的水化物的酸性较强的是____ (填化学式)。
(4)①的最高价氧化物与⑦的最高价氧化物的熔点较高的是____ (填化学式),原因是_____ 。
(5)⑤与⑥金属性较强的是________ (填元素符号),下列表述能证明这一结论的是____ 。
A.单质的熔沸点:⑤>⑥
B.最高价氧化物的水化物的碱性:⑤>⑥
C.单质与水反应的剧烈程度:⑤>⑥
(6)②的简单氢化物的结构式___ ,它与⑧的气态氢化物反应的化学方程式是___ ,该反应生成物的晶体类型为__ 晶体。
族 周期 | IA | 0 | ||||||
1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
2 | ① | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)化学性质最不活泼的元素是
(2)③、⑤的原子半径较小的是
(3)①、②的最高价氧化物的水化物的酸性较强的是
(4)①的最高价氧化物与⑦的最高价氧化物的熔点较高的是
(5)⑤与⑥金属性较强的是
A.单质的熔沸点:⑤>⑥
B.最高价氧化物的水化物的碱性:⑤>⑥
C.单质与水反应的剧烈程度:⑤>⑥
(6)②的简单氢化物的结构式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】随原子序数的递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。

根据判断出的元素回答问题:
(1)f在元素周期表的位置是__________________ 。
(2)比较d、e常见离子的半径大小(用化学式表示)___________________ ;
(3)z的简单氢化物与z的最高价氧化物的水化物形成的化合物中化学键类型为:_______________________ 。
(4)元素y的一种同位素可用于测定文物年代,这种同位素原子符号为___________ 。
(5)元素g与元素h相比,非金属性较强的是_________ (用元素符号表示),下列表述中能证明这一事实的是_________ (填序号)。
a.常温下g的单质和h的单质状态不同
b.h的氢化物比g的氢化物稳定
c.一定条件下g和h的单质都能与氢氧化钠溶液反应
d.g、h最高价氧化物对应水化物的酸性前者弱于后者
(6)x、e反应可生成离子化合物ex。
①写出化合物ex的电子式__________________ 。
②将少量ex投入水中,剧烈反应,得到x单质。
写出反应的化学方程式:_____________________________________________ ;

根据判断出的元素回答问题:
(1)f在元素周期表的位置是
(2)比较d、e常见离子的半径大小(用化学式表示)
(3)z的简单氢化物与z的最高价氧化物的水化物形成的化合物中化学键类型为:
(4)元素y的一种同位素可用于测定文物年代,这种同位素原子符号为
(5)元素g与元素h相比,非金属性较强的是
a.常温下g的单质和h的单质状态不同
b.h的氢化物比g的氢化物稳定
c.一定条件下g和h的单质都能与氢氧化钠溶液反应
d.g、h最高价氧化物对应水化物的酸性前者弱于后者
(6)x、e反应可生成离子化合物ex。
①写出化合物ex的电子式
②将少量ex投入水中,剧烈反应,得到x单质。
写出反应的化学方程式:
您最近一年使用:0次



