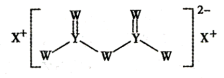
短周期主族元素X、Y、Z、W原子序数依次增大,四种元素组成的一种食品添加剂结构如图所示。Z的原子半径在短周期中最大,W基态原子的s能级电子总数是p能级电子总数的2/3。下列说法不正确的是
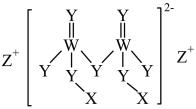
| A.电负性:Y>W>Z |
| B.简单离子半径:W>Y>Z |
| C.简单氢化物沸点:Y>W |
| D.WX3、X3Y+中W、Y两种原子的杂化轨道类型不同 |
更新时间:2024-03-13 09:03:46
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】短周期主族元素W、X、Y、Z的原子序数依次增大,X原子的最外层电子数与W的核外电子数相等,Y的周期数是族序数的3倍,Z与X同主族,化合物 的溶液可用于去除餐具表面的油污。下列说法错误的是
的溶液可用于去除餐具表面的油污。下列说法错误的是
 的溶液可用于去除餐具表面的油污。下列说法错误的是
的溶液可用于去除餐具表面的油污。下列说法错误的是| A.四种元素中,X的原子半径最小 |
| B.W、Z分别与X均可形成多种化合物 |
| C.Y、Z形成的化合物水溶液呈碱性 |
| D.X、Y形成的化合物中一定只含离子键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】短周期主族元素X、Y、Z、W的原子序数依次增大,X的主族序数是周期数的2倍,Y的核外电子数是电子层数的四倍,Z元素的金属性在短周期中最强,W与Y位于同一主族。下列说法正确的是
A.简单原子半径: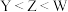 | B.Y与Z组成的化合物中不可能含非极性键 |
C.最简单气态氢化物的热稳定性: | D.X的最高价氧化物对应水化物的酸性比W的强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某种元素的电离能数据如下(单位:kJ/mol),该元素最可能是
| Ⅰ1 | Ⅰ2 | Ⅰ3 | Ⅰ4 |
| 740 | 1500 | 7700 | 10500 |
| A.s区元素 | B.f区元素 | C.p区元素 | D.d区元素 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列对价电子构型为2s22p5的元素描述正确的是( )
| A.电负性最大 | B.最高正价为+7 | C.第一电离能最大 | D.原子半径最小 |
您最近一年使用:0次
【推荐1】下列说法中正确的是
①原子光谱的特征谱线用于鉴定元素,从 2
2 s2
s2 1跃迁至
1跃迁至 2
2 s2
s2 4时释放能量
4时释放能量
②Cl2分子中,Cl-Cl键是p-pσ键
③铍原子最外层原子轨道的电子云图:
④ ,该电子排布图违背了泡利原理
,该电子排布图违背了泡利原理
⑤键能N-N>P-P、N-H>P-H,因此N2H4的沸点大于P2H4的沸点
⑥碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释
⑦氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性
⑧三氧化硫有单分子气体和三聚分子固体(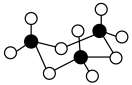 )两种存在形式,两种形式中S原子的杂化轨道类型不同
)两种存在形式,两种形式中S原子的杂化轨道类型不同
①原子光谱的特征谱线用于鉴定元素,从
 2
2 s2
s2 1跃迁至
1跃迁至 2
2 s2
s2 4时释放能量
4时释放能量②Cl2分子中,Cl-Cl键是p-pσ键
③铍原子最外层原子轨道的电子云图:

④
 ,该电子排布图违背了泡利原理
,该电子排布图违背了泡利原理⑤键能N-N>P-P、N-H>P-H,因此N2H4的沸点大于P2H4的沸点
⑥碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释
⑦氟的电负性大于氯的电负性,导致三氟乙酸的酸性大于三氯乙酸的酸性
⑧三氧化硫有单分子气体和三聚分子固体(
 )两种存在形式,两种形式中S原子的杂化轨道类型不同
)两种存在形式,两种形式中S原子的杂化轨道类型不同| A.①②④⑦ | B.①②⑤⑦ | C.①②⑦⑧ | D.①④⑥⑦ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量含氧橄榄石矿物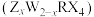 。已知前四周期元素X、Y、Z、R、W的原子序数依次增大,Y的氢化物常用于雕刻玻璃,R元素的一种氧化物可制作光导纤维,W的合金材料是生活中用途最广泛的金属材料。其态Z原子核外s,p能级上电子总数相等。下列叙述正确的是
。已知前四周期元素X、Y、Z、R、W的原子序数依次增大,Y的氢化物常用于雕刻玻璃,R元素的一种氧化物可制作光导纤维,W的合金材料是生活中用途最广泛的金属材料。其态Z原子核外s,p能级上电子总数相等。下列叙述正确的是
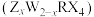 。已知前四周期元素X、Y、Z、R、W的原子序数依次增大,Y的氢化物常用于雕刻玻璃,R元素的一种氧化物可制作光导纤维,W的合金材料是生活中用途最广泛的金属材料。其态Z原子核外s,p能级上电子总数相等。下列叙述正确的是
。已知前四周期元素X、Y、Z、R、W的原子序数依次增大,Y的氢化物常用于雕刻玻璃,R元素的一种氧化物可制作光导纤维,W的合金材料是生活中用途最广泛的金属材料。其态Z原子核外s,p能级上电子总数相等。下列叙述正确的是A.电负性: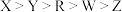 | B.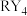 分子的键角为 分子的键角为 |
C.简单氢化物的稳定性: | D.熔点: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】光气(COCl2)是一种重要的有机中间体,其制备原理为: 。下列叙述正确的是
。下列叙述正确的是
 。下列叙述正确的是
。下列叙述正确的是| A.CHCl3是含有极性共价键的非极性分子 | B.H2O2中氧原子的杂化方式为sp2杂化 |
| C.COCl2的VSEPR模型为三角锥形 | D.HCl的沸点是同族氢化物中最低的 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、R为前四周期元素且原子序数依次增大。X的单质与H2化合生成气体G,,其水溶液呈碱性;Y的单质是一种黄色晶体;R基态原子3d轨道的电子数是4s轨道电子数的3倍。Y、Z分别与钠元素可形成化合物Q和J。J的水溶液与AgNO3溶液反应可生成不溶于稀硝酸的白色沉淀L;Z与氢元素形成的化合物与G反应生成M。下列说法正确的是
| A.M的晶体类型是分子晶体 | B.G分子中X原子的杂化轨道类型是sp3 |
| C.Q和J都含共价键 | D.R位于第四周期ⅠB族 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】北京大学和中国科学院的化学工作者成功研制出碱金属与C60形成的球碳盐K3C60。实验测知该物质属于离子晶体,具有良好的超导性。下列关于K3C60的组成和结构的分析中正确的是
| A.K3C60晶体中既有离子键又有极性键 | B.K3C60晶体的熔点比C60晶体的熔点低 |
| C.该晶体熔化时能导电 | D.C60分子中碳原子采取sp3杂化 |
您最近一年使用:0次