一种可吸附甲醇的材料,其化学式为[C(NH2)3]4[B(OCH3)4]3Cl,部分晶体结构如下图所示,其中[C(NH2)3]+为平面结构。下列说法正确的是

| A.该晶体中存在N-H…O氢键 |
| B.基态原子的第一电离能:C<N<O |
| C.基态原子未成对电子数:B<C<O |
| D.晶体中B、N和O原子轨道的杂化类型相同 |
2024·北京·模拟预测 查看更多[4]
更新时间:2024-03-19 20:53:17
|
相似题推荐
单选题
|
适中
(0.65)
真题
名校
【推荐1】W、X、Y、Z为原子序数依次增加的同一短周期元素,其中X、Y、Z相邻,W的核外电子数与X的价层电子数相等, 是氧化性最强的单质,4种元素可形成离子化合物
是氧化性最强的单质,4种元素可形成离子化合物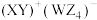 。下列说法正确的是
。下列说法正确的是
 是氧化性最强的单质,4种元素可形成离子化合物
是氧化性最强的单质,4种元素可形成离子化合物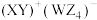 。下列说法正确的是
。下列说法正确的是A.分子的极性: | B.第一电离能:X<Y<Z |
C.氧化性: | D.键能: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】硒(34Se)元素是人体必需的微量元素之一,与溴同周期。下列说法不正确 的是
| A.电负性由大到小顺序:Cl>Br>Se |
| B.氢化物的稳定性:硒化氢<水<氟化氢 |
| C.第一电离能:Br>Se>As |
| D.原子半径:Se>Br>O |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】化合物 可作为某新型电池的正极材料,其中X、Y、Z、W是原子序数递增且属于不同主族的短周期元素,X、Y相邻,Y的氢化物可刻蚀玻璃,Z的最高价氧化物对应的水化物在同周期元素中碱性最强,W的基态原子价层p轨道半充满,M的基态原子价层电子排布式为
可作为某新型电池的正极材料,其中X、Y、Z、W是原子序数递增且属于不同主族的短周期元素,X、Y相邻,Y的氢化物可刻蚀玻璃,Z的最高价氧化物对应的水化物在同周期元素中碱性最强,W的基态原子价层p轨道半充满,M的基态原子价层电子排布式为 。下列说法错误的是
。下列说法错误的是
 可作为某新型电池的正极材料,其中X、Y、Z、W是原子序数递增且属于不同主族的短周期元素,X、Y相邻,Y的氢化物可刻蚀玻璃,Z的最高价氧化物对应的水化物在同周期元素中碱性最强,W的基态原子价层p轨道半充满,M的基态原子价层电子排布式为
可作为某新型电池的正极材料,其中X、Y、Z、W是原子序数递增且属于不同主族的短周期元素,X、Y相邻,Y的氢化物可刻蚀玻璃,Z的最高价氧化物对应的水化物在同周期元素中碱性最强,W的基态原子价层p轨道半充满,M的基态原子价层电子排布式为 。下列说法错误的是
。下列说法错误的是| A.原子半径:Z>X>Y | B.第一电离能:X>Y>M |
C. 中W采用sp3杂化 中W采用sp3杂化 | D.M2X5可作为SO2转化为SO3的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】羟胺 易溶于水,可看成是
易溶于水,可看成是 中的
中的 被
被 取代的产物,其水溶液是比肼还弱的碱性溶液。下列有关说法正确的是
取代的产物,其水溶液是比肼还弱的碱性溶液。下列有关说法正确的是
 易溶于水,可看成是
易溶于水,可看成是 中的
中的 被
被 取代的产物,其水溶液是比肼还弱的碱性溶液。下列有关说法正确的是
取代的产物,其水溶液是比肼还弱的碱性溶液。下列有关说法正确的是A. 分子稳定性较强是因为分子间含有氢键 分子稳定性较强是因为分子间含有氢键 |
B. 的水溶液显碱性是因为 的水溶液显碱性是因为 溶于水时可电离产生 溶于水时可电离产生 |
C. 与 与 中 中 的键角相同 的键角相同 |
D. 与 与 的中心 的中心 原子的价层电子对数相同 原子的价层电子对数相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】含Tp配体的钌(Ru)配合物催化氢化 生成甲酸的机理如图所示。下列叙述错误的是
生成甲酸的机理如图所示。下列叙述错误的是
 生成甲酸的机理如图所示。下列叙述错误的是
生成甲酸的机理如图所示。下列叙述错误的是
| A.循环中Ru的成键数目不变 |
| B.循环中物质所含氢键均为分子间氢键 |
C.Tp配体中, 中含有 中含有 ,N原子为 ,N原子为 杂化 杂化 |
| D.该催化反应的原子利用率为100% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在水中,水分子可彼此通过氢键形成(H2O)n的小集团。在一定温度下(H2O)n的n=5,每个水分子被4个水分子包围着形成四面体。(H2O)n的n=5时,下列说法中正确的是


| A.(H2O)n是一种新的水分子 |
| B.(H2O)n仍保留着水的化学性质 |
| C.1 mol(H2O)n中有2个氢键 |
| D.1 mol(H2O)n中有4 mol氢键 |
您最近一年使用:0次




 。则下列有关比较中正确的是
。则下列有关比较中正确的是





 与足量银氨溶液反应生成2mol银
与足量银氨溶液反应生成2mol银

