从废弃的声光器件( ,含
,含 、
、 、
、 杂质)中提取粗碲的工艺流程如图,已知
杂质)中提取粗碲的工艺流程如图,已知 性质与
性质与 相似,氧化沉碲得
相似,氧化沉碲得 ,下列说法错误的是
,下列说法错误的是
 ,含
,含 、
、 、
、 杂质)中提取粗碲的工艺流程如图,已知
杂质)中提取粗碲的工艺流程如图,已知 性质与
性质与 相似,氧化沉碲得
相似,氧化沉碲得 ,下列说法错误的是
,下列说法错误的是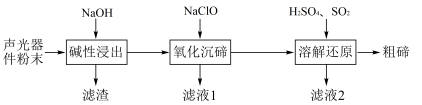
A.滤渣的主要成分为 |
| B.滤液1和滤液2混合可能产生白色沉淀 |
C.“氧化沉碲”中离子方程式为 |
| D.“溶解还原”中氧化剂和还原剂的物质的量之比为1:3 |
更新时间:2024-04-05 20:42:50
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】表示下列反应的离子方程式正确的是
| A.NaHS溶液中滴入少量CuSO4溶液:HS-+Cu2+=CuS↓+H+ |
B.铅蓄电池放电时负极反应:PbO2+2e-+4H++SO =PbSO4+2H2O =PbSO4+2H2O |
C.草酸使酸性KMnO4溶液褪色:2MnO +5C2O +5C2O +16H+=2Mn2++10CO2↑+8H2O +16H+=2Mn2++10CO2↑+8H2O |
D.NaAlO2溶液中滴入少量NH4HCO3溶液:NH +HCO +HCO +3H2O+2AlO +3H2O+2AlO =2Al(OH)3↓+NH3·H2O+CO =2Al(OH)3↓+NH3·H2O+CO |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知2Fe3++2I-=2Fe2++I2,当把Cl2通入FeI2溶液中时,下列离子方程式一定不正确 的是
| A.Cl2+2I-=I2+2Cl- |
| B.4Cl2+6I-+2Fe2+=2Fe3++3I2+8Cl- |
| C.3Cl2+2Fe2++4I-=2Fe3++2I2+6Cl- |
| D.2Cl2+2Fe2++2I-=2Fe3++I2+4Cl- |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】氢化氨(NH5)与氯化铵结构相似,其与水反应有氢气生成,下列叙述正确的是
| A.NH5中氮元素的化合价为+5价 | B.NH5溶于水所形成的溶液显酸性 |
| C.NH5与水反应时,水是氧化剂 | D.1 mol NH5中含有5NA个N-H键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】我国古代科技发展处于世界领先水平,隋唐时期发明黑火药,爆炸时的反应为①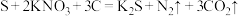 ;明代宋应星在《天工开物》中记载了火法炼锌的方法,反应为②
;明代宋应星在《天工开物》中记载了火法炼锌的方法,反应为② ,下列关于①②这两个反应的说法正确的是
,下列关于①②这两个反应的说法正确的是
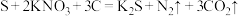 ;明代宋应星在《天工开物》中记载了火法炼锌的方法,反应为②
;明代宋应星在《天工开物》中记载了火法炼锌的方法,反应为② ,下列关于①②这两个反应的说法正确的是
,下列关于①②这两个反应的说法正确的是| A.C元素在反应①中被氧化,在反应②中被还原 |
| B.反应①中只有S作氧化剂 |
| C.反应②中还原产物只有Zn |
| D.在高温条件下,C的还原性强于Zn |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】向AgNO3溶液中通入过量SO2,过程和现象如下图。现象:通入SO2,立即生成大量白色沉淀A;放置一段时间后出现灰色固体(Ag)。下列说法不正确的是


| A.若发生复分解反应生成沉淀A,则①中生成A的离子方程式为2Ag++SO2+H2O=Ag2SO3↓+2H+ |
| B.①中不可能生成Ag2SO4 |
| C.②中的现象体现了Ag+的氧化性 |
| D.该实验条件下,SO2与AgNO3反应生成Ag2SO3的速率大于生成Ag的速率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某阴离子结构如下,M、W、X、Y、Z是原子序数依次增大的五种短周期主族元素,下列说法正确的是
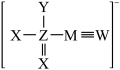
A.氢化物的沸点 |
| B.W氧化物对应的水化物为强酸 |
C. 的氢化物的水溶液需用橡胶塞的玻璃瓶盛放 的氢化物的水溶液需用橡胶塞的玻璃瓶盛放 |
D. 的一种氧化物对应的水化物可用于制备HI 的一种氧化物对应的水化物可用于制备HI |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。W、X、Z 最外层电子数之和为10;W与Y同族;W与Z形成的化合物ZW2可与浓硫酸反应,其生成物甲可腐蚀玻璃。下列说法正确的是
| A.离子半径Y>Z>X>W |
| B.最高化合价W> Z |
| C.甲物质是一种强酸,有强的腐蚀性 |
| D.W与X形成的化合物XW水溶液呈碱性 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】关于铝与氢氧化钠溶液反应的说法不正确的是
| A.铝是还原剂 | B.氧化剂是氢氧化钠和水 |
| C.只有水是氧化剂 | D.氢气是还原产物 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某实验小组用以下装置探究了铝和铜组成的原电池在不同浓度的NaOH溶液中放电的情况,NaOH溶液浓度对铝一碱电池的放电电流和持续放电时间的影响如下表。

根据以上数据分析,下列说法错误的是

| C(NaOH)/mol·L-1 | 0.1 | 0.5 | 1.0 | 1.5 | 2.0 |
| 放电电流I/mA | 0.13 | 0.26 | 0.40 | 0.52 | 0.65 |
| 放电时间t/min | 45 | 14 | 9 | 8 | 7 |
| A.在铜电极上发生还原反应放出氢气 |
| B.负极反应为Al-3e-+4OH-=[Al(OH)4]- |
| C.NaOH溶液浓度越大,反应速率越快,放电电流越大 |
| D.该电池是一种二次电池,可充电后重复使用 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用相同的铝片、6 mol·L-1稀盐酸、3 mol·L-1稀硫酸、6 mol·L-1氢氧化钠溶液、试管等分别进行表中实验:
对上述实验的相关说法不正确 的是
| 实验方案 | 实验现象 | 实验原理(化学方程式) |
| (1)铝片与足量盐酸反应 | 铝片开始无现象,一段时间后逐渐溶解,并有大量气泡产生 | Al2O3+6HCl=2AlCl3+3H2O 2Al+6HCl=2AlCl3+3H2↑ |
| (2)铝片与足量硫酸反应 | 铝片开始无现象,一段时间后反应缓慢,铝片表面有少量气泡产生 | Al2O3+3H2SO4=2Al2(SO4)3+3H2O 2Al+3H2SO4=2Al2(SO4)3+3H2↑ |
| (3)铝片与足量氢氧化钠溶液反应 | 铝片开始无现象,一段时间后铝片逐渐溶解,并有大量气泡产生 | Al2O3+2NaOH=2NaAlO2+H2O 2Al+2NaOH+2H2O=2NaAlO2+3H2↑ |
| A.对比(1)、(2)、(3)中Al2O3参与的反应可得出:Al2O3既有碱性氧化物的某些性质,又有酸性氧化物的某些性质 |
| B.对比(1)、(2)、(3)中气体产生现象和酸碱挥发性可得出:实验(3)最适宜于实验室制备H2 |
| C.对比实验(1)、(2)后来产生气泡的现象,可得出:c(H+)浓度对气泡产生的多少无影响 |
D.对比实验(1)、(2)后来产生气泡的现象,可得出: 对Al与H+的反应可能有阻碍作 对Al与H+的反应可能有阻碍作 |
您最近半年使用:0次



