硫酸是重要的化工原料,我国工业上一般以黄铁矿为原料来制备硫酸。工业制硫酸涉及下列反应:① ;②
;② ;③
;③ 。生产中用浓硫酸代替水吸收
。生产中用浓硫酸代替水吸收 ,制得焦硫酸(
,制得焦硫酸( ,也可以表示为
,也可以表示为 ),将焦硫酸稀释后可制得密度为
),将焦硫酸稀释后可制得密度为 、质量分数为98%的浓硫酸。下列说法不正确的是
、质量分数为98%的浓硫酸。下列说法不正确的是
 ;②
;② ;③
;③ 。生产中用浓硫酸代替水吸收
。生产中用浓硫酸代替水吸收 ,制得焦硫酸(
,制得焦硫酸( ,也可以表示为
,也可以表示为 ),将焦硫酸稀释后可制得密度为
),将焦硫酸稀释后可制得密度为 、质量分数为98%的浓硫酸。下列说法不正确的是
、质量分数为98%的浓硫酸。下列说法不正确的是A.每生成1mol 时,转移5.5mol电子 时,转移5.5mol电子 |
B.焦硫酸钠( )的水溶液呈酸性 )的水溶液呈酸性 |
C.质量分数为98%的浓 ,物质的量浓度为18.4mol/L ,物质的量浓度为18.4mol/L |
D.浓硫酸吸收 生成焦硫酸的变化是物理变化 生成焦硫酸的变化是物理变化 |
更新时间:2024-03-23 16:21:28
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】设NA表示阿伏加 德罗常数的值,下列关于0.2 mol·L-1 Ba(NO3)2溶液的叙述不正确的是( )
A.2 L溶液中Ba2+、 总数为1.2NA 总数为1.2NA |
B.500 mL溶液中 浓度为0.2 mol·L-1 浓度为0.2 mol·L-1 |
| C.500 mL溶液中Ba2+浓度为0.2 mol·L-1 |
D.500 mL溶液中 物质的量为0.2 mol 物质的量为0.2 mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】浓度为0.1 mol/L的HCl溶液V mL,加水稀释到2V mL,再取出10 mL,这10 mL溶液中c(H+)为
| A.0.1 mol/L | B.0.01 mol/L | C.0.02 mol/L | D.0.05 mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】关于蔗糖的说法中错误的是
| A.蔗糖是最重要的二糖,它的相对分子质量是葡萄糖相对分子质量的两倍 |
| B.纯净的蔗糖溶液中加入银氨溶液微热,不发生银镜反应 |
| C.在蔗糖与稀硫酸共热后的溶液中滴加银氨溶液,用水浴加热,看不到银镜生成 |
| D.在蔗糖里加入浓硫酸,可观察到颜色变黑,并有泡沫出现 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
【推荐2】下列实验目的可以达到的是
| A.电解熔融氯化镁制取金属镁 |
| B.醋酸钠结晶水合物与碱石灰共热制取甲烷 |
| C.浓硫酸与溴化钠共热制取溴化氢 |
| D.饱和碳酸钠溶液除去二氧化碳中的氯化氢 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】尖晶石矿的主要成分为 (含
(含 杂质)。已知:
杂质)。已知: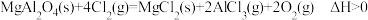 。该反应难以发生,但采用“加炭氯化法”可以制备
。该反应难以发生,但采用“加炭氯化法”可以制备 和
和 ,同时还可得到副产物
,同时还可得到副产物 (
( 沸点为
沸点为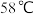 ,
, 在
在 升华):
升华):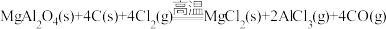 。下列说法
。下列说法不正确 的是
 (含
(含 杂质)。已知:
杂质)。已知: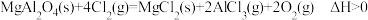 。该反应难以发生,但采用“加炭氯化法”可以制备
。该反应难以发生,但采用“加炭氯化法”可以制备 和
和 ,同时还可得到副产物
,同时还可得到副产物 (
( 沸点为
沸点为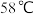 ,
, 在
在 升华):
升华):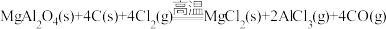 。下列说法
。下列说法| A.制备时要保持无水环境 |
B.输送气态产物的管道温度要保持在 以上 以上 |
| C.氯化时加炭,既增大了反应的趋势,又为氯化提供了能量 |
D.为避免产生大量 ,反应过程中需保持炭过量 ,反应过程中需保持炭过量 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】实验室用N2H4(肼,又名联氨,常温下为无色油状液体,沸点为113.5 ℃,具有与氨相似的气味,有弱碱性和较强的还原性)还原Cu(OH)2制备纳米Cu2O的装置(部分加热装置已省略)如图所示:已知:NaNO2溶液与NH4Cl溶液反应能得到N2。

下列说法不正确的是

下列说法不正确的是
| A.装置②⑥中分别盛装浓硫酸和稀硫酸 |
| B.无水硫酸铜由白色变为蓝色说明从装置④中出来的气体中含有水蒸气 |
C.装置④中发生反应的化学方程式为N2H4+4Cu(OH)2 2Cu2O+N2↑+6H2O 2Cu2O+N2↑+6H2O |
| D.加入反应试剂后,先打开K2,待装置④中反应完且冷却至室温,再打开K1排尽装置中的N2H4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA表示阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,0.1mol 溶于水,转移的电子数目为0.1NA 溶于水,转移的电子数目为0.1NA |
B.一定条件下,2.3g的Na完全与 反应生成3.6g产物时失去的电子数为0.1NA 反应生成3.6g产物时失去的电子数为0.1NA |
| C.在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
D.50ml 12mol/L盐酸与足量 共热,转移的电子数为0.3NA 共热,转移的电子数为0.3NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】水热法制备纳米颗粒Y(化合物)的反应为 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是A. 是还原剂 是还原剂 |
B.Y的化学式为 |
| C.a=4 |
D.标准状况下,有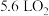 参与反应时,转移电子的物质的量为 参与反应时,转移电子的物质的量为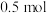 |
您最近一年使用:0次

 Na2O(s)
Na2O(s) NaOH(aq)
NaOH(aq) Fe(OH)3(胶体)
Fe(OH)3(胶体) Fe2O3(s)
Fe2O3(s) Cu(OH)2(s)
Cu(OH)2(s) Cu2O(s)
Cu2O(s) SO2(g)
SO2(g) H2SO4(aq)
H2SO4(aq) 、
、 及少量不溶性杂质)制备
及少量不溶性杂质)制备 的工艺流程如图。
的工艺流程如图。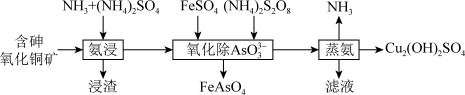
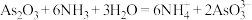

 ”时每生成1mol
”时每生成1mol ,转移的电子数目为
,转移的电子数目为
 、
、 、
、

 微粒
微粒

