下列有关物质结构或性质分类相同的是
A. 模型: 模型: 和 和 | B.晶体类型: 和 和 |
C.空间结构: 和 和 | D.分子极性: 和 和 |
更新时间:2024-03-24 14:09:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列表达方式或说法正确的是
| A.基态到激发态产生的光谱是发射光谱 |
B.氯化铵的电子式: |
| C.NH3、H2O、CO2、HCl 四分子中孤电子对最多的是 CO2 |
| D.硫离子的核外电子排布式 1s22s22p63s23p4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】甲磺酸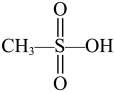 是一种强酸。下列说法正确的是
是一种强酸。下列说法正确的是
 是一种强酸。下列说法正确的是
是一种强酸。下列说法正确的是| A.推测甲磺酸难溶于水 | B.该分子中心原子S的价层电子对数为6 |
| C.分子中所有化学键均为极性共价键 | D.该分子中硫氧键的键长均相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】某化合物的分子式为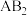 ,A属ⅥA族元素,B属ⅦA族元素,A和B在同一周期,它们的电负性值分别为
,A属ⅥA族元素,B属ⅦA族元素,A和B在同一周期,它们的电负性值分别为 和
和 ,下列推断不正确的是
,下列推断不正确的是
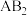 ,A属ⅥA族元素,B属ⅦA族元素,A和B在同一周期,它们的电负性值分别为
,A属ⅥA族元素,B属ⅦA族元素,A和B在同一周期,它们的电负性值分别为 和
和 ,下列推断不正确的是
,下列推断不正确的是A.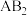 分子的空间构型为“V”形 分子的空间构型为“V”形 |
B. 键为极性共价键, 键为极性共价键,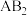 分子为非极性分子 分子为非极性分子 |
C.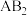 与 与 相比, 相比,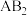 的熔点、沸点比 的熔点、沸点比 的低 的低 |
D.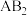 分子的中心原子的成键轨道为 分子的中心原子的成键轨道为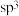 杂化轨道 杂化轨道 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
【推荐2】下列表示不正确 的是
A.中子数为10的氧原子: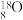 |
B. 的价层电子对互斥(VSEPR)模型: 的价层电子对互斥(VSEPR)模型: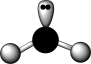 |
C.用电子式表示 的形成过程: 的形成过程: |
D.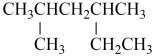 的名称: 的名称: 甲基 甲基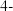 乙基戊烷 乙基戊烷 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】关于CH3OH、N2H4和(CH3)2NNH2的结构与性质,下列说法错误的是
| A.CH3OH为极性分子 | B.N2H4空间结构为平面形 |
| C.N2H4的沸点高于(CH3)2NNH2 | D.CH3OH和(CH3)2NNH2中C、O、N杂化方式均相同 |
您最近一年使用:0次
【推荐2】周期表中IIIA族元素及其化合物应用广泛。硼熔点很高,其硬度仅次于金刚石,单质硼可以溶于热的浓硝酸生成硼酸(H3BO3),硼酸是有重要用途的一元弱酸,能溶于水,可用作防腐剂;硼烷(B2H6,常温下为气态)是一种潜在的高能燃料,在O2中完全燃烧生成B2O3固体和液态水,燃烧热为2165kJ•mol-1;氨硼烷(H3NBH3)是最具潜力的储氢材料之一,与硼烷的相对分子质量相近,但沸点却比硼烷高得多;BF3是石油化工的重要催化剂;Al2O3熔点很高,是两性氧化物,可溶于强酸、强碱;砷化镓(GaAs)是一种新型化合物半导体材料。下列说法正确的是
| A.H3NBH3分子间存在氢键 |
| B.BF3是由极性键构成的极性分子 |
| C.镓原子(31Ga)基态原子核外电子排布式为4s24p1 |
| D.IIIA族元素单质的晶体类型相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列选项中各物质的化学键类型相同、晶体类型也相同的是
A. 、 、 、 、 | B.金刚石、 、 、 |
C. 、 、 、 、 | D. 、 、 、 、 、单质硅 、单质硅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15, X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
| A.原子半径:W>Z>Y>X>M |
| B.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
| C.XZ2, X2M2, W2Z2均为直线型的共价化合物 |
| D.由X元素形成的单质不一定是原子晶体 |
您最近一年使用:0次

 形的极性分子
形的极性分子 、
、 和
和 杂化
杂化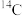 原子中,核外存在2对自旋相反的电子,其核外电子有4种运动状态
原子中,核外存在2对自旋相反的电子,其核外电子有4种运动状态 键,可能有
键,可能有 键
键 、
、
 、
、

 、
、
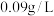 ,Y的同位素可用于测定文物年代,Z元素的某种单质可用作自来水消毒剂,下列说法正确的是
,Y的同位素可用于测定文物年代,Z元素的某种单质可用作自来水消毒剂,下列说法正确的是
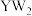 、
、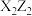 均为非极性分子
均为非极性分子 、
、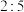 的两种分子
的两种分子

