某实验小组以H2O2 分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响,在常温下按照如下方案完成实验。
(1)催化剂能加快化学反应速率的原因是________________ 。
(2)实验①和②的目的是___________________ ;实验时由于较长时间没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2不易分解,为了达到实验目的,你对原实验方案的改进是_________________________________________ 。
(3)若实验③中,反应 5 分钟内,测得产生氧气体积为22.4mL (标准状况下),假设反应前后溶液总体积不变,则该时间段以H2O2 表示的反应速率为________ 。
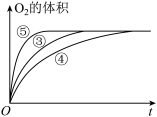
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图,分析下图能够得出的实验结论是________________________________________ 。
| 实验编号 | 反应物 | 催化剂 |
| ① | 9mL2%H2O2溶液 | 无 |
| ② | 9mL5%H2O2溶液 | 无 |
| ③ | 9mL5%H2O2溶液 | 1mL0.1·mol.L-1FeCl3溶液 |
| ④ | 9mL5%H2O2溶液+少量稀盐酸 | 1mL0.1mol.L-1FeCl3溶液 |
| ⑤ | 9mL5%H2O2溶液+少量NaOH溶液 | 1mL0.1mol.L-1FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是
(2)实验①和②的目的是
(3)若实验③中,反应 5 分钟内,测得产生氧气体积为22.4mL (标准状况下),假设反应前后溶液总体积不变,则该时间段以H2O2 表示的反应速率为
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图,分析下图能够得出的实验结论是

更新时间:2024-03-24 14:22:25
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖。工业合成氨生产示意图如图所示。

(1)下列有关合成氨工业的说法正确的是_________
(2)循环利用的Y是氮气和氢气,目的是__________________ 。
(3)在合成氨工业中,要使氨的产率增大,同时又能提高反应速率,可采取的措施有_________ (填编号)。
①使用催化剂 ②恒温恒容,增大原料气 和
和 充入量 ③及时分离产生的
充入量 ③及时分离产生的
④升高温度 ⑤恒温恒容,充入惰性气体 使压强增大
使压强增大
(4)氮的固定和氮的循环是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分 值。
值。
分析数据可知:
①在 下模拟工业固氮,某时刻
下模拟工业固氮,某时刻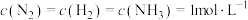 ,此时
,此时
_________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②人类不适合大规模模拟大气固氮的原因是__________________ 。
(5)为获得合成氨的原料气氢气,某科研小组以太阳能为热源分解 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如下。
的过程如下。
已知: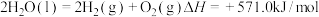 。
。
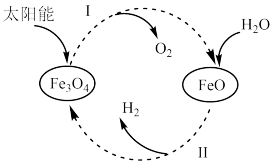
过程Ⅰ: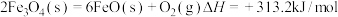
过程Ⅱ:……
过程Ⅱ的热化学方程式为_________ 。

(1)下列有关合成氨工业的说法正确的是_________
| A.工业合成氨的反应是熵减小的放热反应,在低温或常温时可自发进行 |
| B.合成氨反应中,反应物的总键能小于产物的总键能 |
C.合成氨厂一般采用的压强为 ,因为该压强下铁触媒的活性最高 ,因为该压强下铁触媒的活性最高 |
D. 的量越多, 的量越多, 的转化率越大,因此,充入的 的转化率越大,因此,充入的 越多越有利于 越多越有利于 的合成 的合成 |
(3)在合成氨工业中,要使氨的产率增大,同时又能提高反应速率,可采取的措施有
①使用催化剂 ②恒温恒容,增大原料气
 和
和 充入量 ③及时分离产生的
充入量 ③及时分离产生的
④升高温度 ⑤恒温恒容,充入惰性气体
 使压强增大
使压强增大(4)氮的固定和氮的循环是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分
 值。
值。| 反应 | 大气固氮 | 工业固氮 | |||
温度 | 27 | 2000 | 25 | 400 | 450 |
 |  | 0.1 | 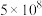 | 0.507 | 0.152 |
①在
 下模拟工业固氮,某时刻
下模拟工业固氮,某时刻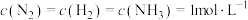 ,此时
,此时
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②人类不适合大规模模拟大气固氮的原因是
(5)为获得合成氨的原料气氢气,某科研小组以太阳能为热源分解
 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如下。
的过程如下。已知:
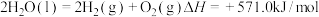 。
。
过程Ⅰ:
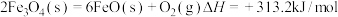
过程Ⅱ:……
过程Ⅱ的热化学方程式为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】工业利用 、
、 催化合成氨实现了人类“向空气中要面包”的梦想。
催化合成氨实现了人类“向空气中要面包”的梦想。
(1)原料气(含 、
、 、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
 。
。
①为提高CO吸收率,应选择的条件为___________ 。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
② 中的配体为
中的配体为___________
(2)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的物种用*标注。
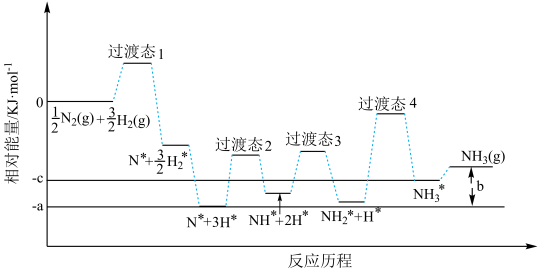
①该反应历程中最大活化能对应步骤的化学方程式为___________ 。合成氨反应: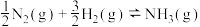 的
的
___________  (用图中字母表示)。
(用图中字母表示)。
②铁催化合成氨时 与
与 需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程
需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程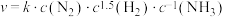 (k为速率常数)可知,
(k为速率常数)可知, 越大,反应速率越小。原因是
越大,反应速率越小。原因是___________ 。
(3)反应 的标准平衡常数可表达为:
的标准平衡常数可表达为: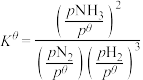 ,其中
,其中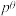 为标准压强(0.1MPa),
为标准压强(0.1MPa),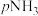 、
、 和
和 分别为各组分的平衡分压(分压=总压×物质的量分数)。若
分别为各组分的平衡分压(分压=总压×物质的量分数)。若 和
和 起始物质的量之比为1:3,反应在恒温、恒压(10MPa)下进行,平衡时
起始物质的量之比为1:3,反应在恒温、恒压(10MPa)下进行,平衡时 转化率为50%,则
转化率为50%,则
___________ (结果保留两位有效数字)。
 、
、 催化合成氨实现了人类“向空气中要面包”的梦想。
催化合成氨实现了人类“向空气中要面包”的梦想。(1)原料气(含
 、
、 、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
、CO)中的CO能被催化剂吸附,需经过铜氨液处理除去,反应为:
 。
。①为提高CO吸收率,应选择的条件为
A.高温高压 B.高温低压 C.低温高压 D.低温低压
②
 中的配体为
中的配体为(2)研究发现铁催化剂表面上合成氨的反应历程如图所示,其中吸附在铁催化剂表面上的物种用*标注。

①该反应历程中最大活化能对应步骤的化学方程式为
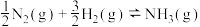 的
的
 (用图中字母表示)。
(用图中字母表示)。②铁催化合成氨时
 与
与 需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程
需吸附在催化剂表面活性位点进行反应,由合成氨反应的速率方程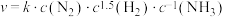 (k为速率常数)可知,
(k为速率常数)可知, 越大,反应速率越小。原因是
越大,反应速率越小。原因是(3)反应
 的标准平衡常数可表达为:
的标准平衡常数可表达为: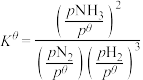 ,其中
,其中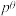 为标准压强(0.1MPa),
为标准压强(0.1MPa),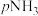 、
、 和
和 分别为各组分的平衡分压(分压=总压×物质的量分数)。若
分别为各组分的平衡分压(分压=总压×物质的量分数)。若 和
和 起始物质的量之比为1:3,反应在恒温、恒压(10MPa)下进行,平衡时
起始物质的量之比为1:3,反应在恒温、恒压(10MPa)下进行,平衡时 转化率为50%,则
转化率为50%,则
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】影响化学反应速率的因素有很多,某课外兴趣小组用实验的方法对其进行探究。
(1)实验一:取 的
的 溶液各
溶液各 分别进行下列实验,实验报告如表所示。
分别进行下列实验,实验报告如表所示。
①实验 、
、 研究的是
研究的是 _______ 对 分解速率的影响。
分解速率的影响。
②表中数据 的值应该为
的值应该为 _______ ;实验 、
、 研究的是
研究的是 _______ 对 分解速率的影响。
分解速率的影响。
(2)实验二:查文献可知, 对
对 分解也有催化作用,为比较
分解也有催化作用,为比较 、
、 对
对 分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
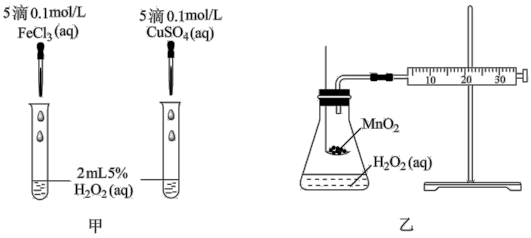
①定性分析:如图甲可通过观察_______ ,定性比较得出结论。有同学提出将 溶液改为
溶液改为 溶液更合理,其理由是
溶液更合理,其理由是 _______ 。
②定量分析:如图乙所示,实验时以收集到 气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是
气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是 _______ 。
(1)实验一:取
 的
的 溶液各
溶液各 分别进行下列实验,实验报告如表所示。
分别进行下列实验,实验报告如表所示。| 序号 | 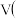 过氧化氢溶液 过氧化氢溶液 | 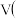 氯化铁溶液 氯化铁溶液 | 二氧化锰质量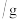 | 反应温度/℃ | 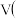 水 水 | 结论 |
 | 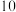 |  |  |  |  | |
 | 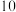 |  |  |  |  | |
 | 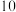 |  |  |  |  |
 、
、 研究的是
研究的是  分解速率的影响。
分解速率的影响。②表中数据
 的值应该为
的值应该为  、
、 研究的是
研究的是  分解速率的影响。
分解速率的影响。(2)实验二:查文献可知,
 对
对 分解也有催化作用,为比较
分解也有催化作用,为比较 、
、 对
对 分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:
①定性分析:如图甲可通过观察
 溶液改为
溶液改为 溶液更合理,其理由是
溶液更合理,其理由是 ②定量分析:如图乙所示,实验时以收集到
 气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是
气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】硼位于ⅢA族,三卤化硼是物质结构化学的研究热点,也是重要的化工原料。三氯化硼(BCl3)可用于制取乙硼烷(B2H6),也可作有机合成的催化剂。
查阅资料:①BCl3的沸点为12.5℃,熔点为‒107.3℃;
②2B+6HCl 2BCl3+3H2;
2BCl3+3H2;
③硼与铝的性质相似,也能与氢氧化钠溶液反应。
设计实验:某同学设计如图所示装置利用氯气和单质硼反应制备三氯化硼:
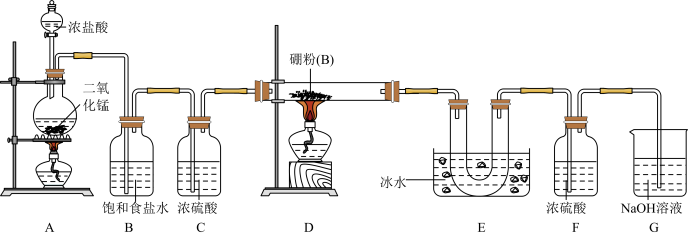
请回答下列问题:
(1)写出A中反应的化学方程式:___________ 。
(2)E装置的作用是___________ 。如果拆去B装置,可能的后果是___________ 。
(3)为了顺利完成实验,正确的操作是___________ (填序号)。
①先点燃A处酒精灯,后点燃D处酒精灯
②先点燃D处酒精灯,后点燃A处酒精灯
③同时点燃A、D处酒精灯
(4)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式:___________ 。
(5)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓___________ (填化学式)溶液,若有气泡产生,则样品中含有硼粉;若无气泡产生,则样品中无硼粉。
查阅资料:①BCl3的沸点为12.5℃,熔点为‒107.3℃;
②2B+6HCl
 2BCl3+3H2;
2BCl3+3H2;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
设计实验:某同学设计如图所示装置利用氯气和单质硼反应制备三氯化硼:

请回答下列问题:
(1)写出A中反应的化学方程式:
(2)E装置的作用是
(3)为了顺利完成实验,正确的操作是
①先点燃A处酒精灯,后点燃D处酒精灯
②先点燃D处酒精灯,后点燃A处酒精灯
③同时点燃A、D处酒精灯
(4)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式:
(5)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】常用调味剂花椒油是一种从花椒籽中提取的水蒸气挥发性香精油,溶于乙醇、乙醚等有机溶剂。利用如图所示装置处理花椒籽粉,经分离提纯得到花椒油。
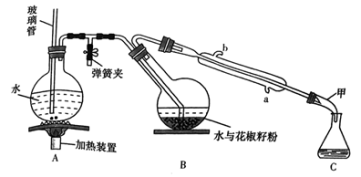
实验步骤:
ⅰ.在A装置的圆底烧瓶中装入2/3容积的水,加1~2粒沸石。在B的圆底烧瓶中加入20 g花椒籽粉和50 mL。
ⅱ.加热A装置中的圆底烧瓶,当有大量蒸气产生时关闭弹簧夹,进行蒸馏。
ⅲ.向馏出液中加入食盐至饱和,再用15 mL乙醚萃取2次,将两次萃取的醚层合并,加入少量无水 ;将液体倾倒入蒸馏烧瓶中,蒸馏得花椒油。
;将液体倾倒入蒸馏烧瓶中,蒸馏得花椒油。
回答下列问题:
(1)装置A中玻璃管的作用是___________ 。
(2)步骤ⅱ中,当观察到___________ 现象时,可停止蒸馏。蒸馏结束时,下列操作的顺序为___________ (序号)。
①停止加热 ②打开弹簧夹 ③关闭冷凝水
(3)在馏出液中加入食盐的作用是___________ ;加入无水 的作用是
的作用是___________ 。
(4)实验结束后,冷凝管中残留物以 表示,清洗冷凝管的最佳试剂是___________(填标号)。
表示,清洗冷凝管的最佳试剂是___________(填标号)。
(5)为测定在花椒油中油脂的含量,取20.00 mL花椒油溶于乙醇中,加80.00 mL 0.5  NaOH的乙醇溶液,搅拌,充分反应,加水配成200 mL溶液。移取25.00 mL于锥形瓶中,滴加酚酞溶液,用0.1
NaOH的乙醇溶液,搅拌,充分反应,加水配成200 mL溶液。移取25.00 mL于锥形瓶中,滴加酚酞溶液,用0.1  盐酸进行滴定,滴定终点消耗盐酸20.00 mL。则该花椒油中含有油脂
盐酸进行滴定,滴定终点消耗盐酸20.00 mL。则该花椒油中含有油脂___________  (花椒油中油脂以
(花椒油中油脂以 计,相对分子质量:884)。
计,相对分子质量:884)。

实验步骤:
ⅰ.在A装置的圆底烧瓶中装入2/3容积的水,加1~2粒沸石。在B的圆底烧瓶中加入20 g花椒籽粉和50 mL。
ⅱ.加热A装置中的圆底烧瓶,当有大量蒸气产生时关闭弹簧夹,进行蒸馏。
ⅲ.向馏出液中加入食盐至饱和,再用15 mL乙醚萃取2次,将两次萃取的醚层合并,加入少量无水
 ;将液体倾倒入蒸馏烧瓶中,蒸馏得花椒油。
;将液体倾倒入蒸馏烧瓶中,蒸馏得花椒油。回答下列问题:
(1)装置A中玻璃管的作用是
(2)步骤ⅱ中,当观察到
①停止加热 ②打开弹簧夹 ③关闭冷凝水
(3)在馏出液中加入食盐的作用是
 的作用是
的作用是(4)实验结束后,冷凝管中残留物以
 表示,清洗冷凝管的最佳试剂是___________(填标号)。
表示,清洗冷凝管的最佳试剂是___________(填标号)。| A.蒸馏水 | B.稀盐酸 | C.苯 | D.NaOH溶液 |
 NaOH的乙醇溶液,搅拌,充分反应,加水配成200 mL溶液。移取25.00 mL于锥形瓶中,滴加酚酞溶液,用0.1
NaOH的乙醇溶液,搅拌,充分反应,加水配成200 mL溶液。移取25.00 mL于锥形瓶中,滴加酚酞溶液,用0.1  盐酸进行滴定,滴定终点消耗盐酸20.00 mL。则该花椒油中含有油脂
盐酸进行滴定,滴定终点消耗盐酸20.00 mL。则该花椒油中含有油脂 (花椒油中油脂以
(花椒油中油脂以 计,相对分子质量:884)。
计,相对分子质量:884)。
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】实验室用环己醇脱水的方法合成环己烯,该实验的装置如下图所示:
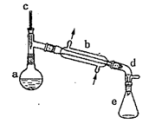
可能用到的有关数据如下:
按下列实验步骤回答问题:
Ⅰ.产物合成
在a中加入10.0g环己醇和2片碎瓷片,冷却搅拌下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度接近90℃。
(l)碎瓷片的作用是_______________________ ;b的名称是____________________ ;
(2)a中发生主要反应的化学方程式为_____________________________________ ;本实验最容易产生的有机副产物的结构简式为___________________ 。
Ⅱ.分离提纯
将反应粗产物倒入分液漏斗中,依次用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过操作X得到纯净的环己烯,称量,其质量为4.1g。
(3)用碳酸钠溶液洗涤的作用是________________ ,操作X的名称为_________________ 。
Ⅲ.产物分析及产率计算
(4)① 核磁共振氢谱可以帮助鉴定产物是否为环己烯,环己烯分子中有_______ 种不同化学环境的氢原子。
② 本实验所得环己烯的产率是______________ 。

可能用到的有关数据如下:
| 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
按下列实验步骤回答问题:
Ⅰ.产物合成
在a中加入10.0g环己醇和2片碎瓷片,冷却搅拌下慢慢加入1mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度接近90℃。
(l)碎瓷片的作用是
(2)a中发生主要反应的化学方程式为
Ⅱ.分离提纯
将反应粗产物倒入分液漏斗中,依次用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过操作X得到纯净的环己烯,称量,其质量为4.1g。
(3)用碳酸钠溶液洗涤的作用是
Ⅲ.产物分析及产率计算
(4)① 核磁共振氢谱可以帮助鉴定产物是否为环己烯,环己烯分子中有
② 本实验所得环己烯的产率是
您最近半年使用:0次



