乙二酸,又称草酸,通常在空气中易被氧化而变质。其两分子结晶水(H2C2O4·2H2O)却能在空气中稳定存在。在分析化学中常用H2C2O4•2H2O做KMnO4的滴定剂,下列关于H2C2O4的说法正确的是
| A.草酸是二元弱酸,其电离方程式为H2C2O4═2H++C2O42− |
| B.草酸滴定KMnO4属于中和滴定,可用石蕊做指示剂 |
| C.乙二酸可通过乙烯经过加成、水解、氧化再氧化制得 |
| D.将浓H2SO4滴加到乙二酸上使之脱水分解,分解产物是CO2和H2O |
13-14高二下·江西·期中 查看更多[11]
四川省宜宾市叙州区第一中学校2019-2020学年高二下学期期中考试化学试题贵州省铜仁市沿河县第二高级中学2019-2020学年高二上学期期末考试化学试题云南省剑川县第一中学2019-2020学年高二上学期期末考试化学试题云南省鲁甸县一中2019-2020学年高二10月月考化学试题云南省丘北二中2018-2019学年高二下学期期末考试化学试题重庆市凤鸣山中学2018-2019学年高二下学期期中考试化学试题贵州省六盘水盘县四中2017-2018学年高二下学期期末考试化学试题2015-2016学年广东省汕头金山中学高二下期中化学试卷(已下线)2014届江西省白鹭洲中学高二下学期期中考试化学试卷2016-2017学年江西省崇义中学高二下学期第二次月考化学试卷2016-2017学年湖北省襄阳市第五中学高二3月月考化学试卷
更新时间:2016-12-09 06:14:29
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】有甲、乙、丙三瓶等体积、等物质的量浓度的NaOH溶液,若甲不变,将乙蒸发掉一半水(溶质不析出),丙中通入一定量的CO2 。然后以甲基橙作指示剂,用相同浓度的盐酸滴定,分别达到终点消耗盐酸的体积是
| A.V甲=V乙>V丙 | B.V丙>V乙>V甲 | C.V乙>V丙>V甲 | D.V甲=V乙=V丙 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】图像表征是化学研究问题的重要方法,由下列图像得出的结论中不正确的是


A.图甲所对应的可逆反应平衡时升高温度,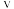 (正)增大的程度小于 (正)增大的程度小于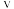 (逆)增大的程度 (逆)增大的程度 |
B.图乙是室温下 催化分解过程中 催化分解过程中 随反应时间变化的曲线,20s时的速率为 随反应时间变化的曲线,20s时的速率为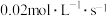 |
C.图丙是室温下用 NaOH溶液滴定20.00mL NaOH溶液滴定20.00mL HX酸溶液的滴定曲线,滴定终点时溶液呈碱性 HX酸溶液的滴定曲线,滴定终点时溶液呈碱性 |
D.图丁是室温下用 除去溶液中的 除去溶液中的 达到沉淀溶解平衡时的曲线,揭示了溶液中 达到沉淀溶解平衡时的曲线,揭示了溶液中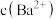 与 与 之间的关系 之间的关系 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,向20.00 mL0.1000 mol/LCH3COOH溶液中逐滴滴加0.1000 mol/L的NaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示。下列说法错误的是


| A.常温下,CH3COOH的Ka约为10-5 |
| B.水的电离程度:b>c |
| C.c点所示溶液中:c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| D.b点时该溶液中存在的微粒关系:2c(H+)+c(CH3COOH) = c(CH3COO-)+2c(OH-) |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】298K时,甲酸(HCOOH)和甲酸钠的混合溶液中HCOOH、 的浓度存在关系式
的浓度存在关系式 ,而含碳元素的粒子的浓度与pH的关系如图所示。
,而含碳元素的粒子的浓度与pH的关系如图所示。
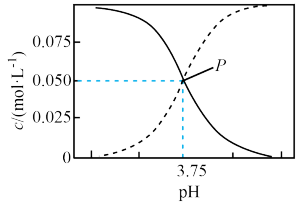
下列说法错误的是
 的浓度存在关系式
的浓度存在关系式 ,而含碳元素的粒子的浓度与pH的关系如图所示。
,而含碳元素的粒子的浓度与pH的关系如图所示。
下列说法错误的是
A.298K时,加蒸馏水稀释P点溶液,溶液中 增大 增大 |
B. 溶液中有 溶液中有 |
C.298K时,HCOOH的电离常数 |
D. 溶液和 溶液和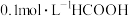 溶液等体积混合后沘合液的pH=3.75 溶液等体积混合后沘合液的pH=3.75 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
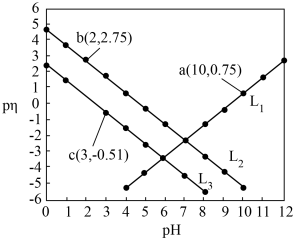
【推荐2】已知HX、HY为一元弱酸且 ,MOH为一元弱碱。常温下,在含HX、HY、MNO3的混合溶液中滴加NaOH溶液,溶液中
,MOH为一元弱碱。常温下,在含HX、HY、MNO3的混合溶液中滴加NaOH溶液,溶液中 与pH的关系如图所示。下列叙述正确的是
与pH的关系如图所示。下列叙述正确的是
 ,MOH为一元弱碱。常温下,在含HX、HY、MNO3的混合溶液中滴加NaOH溶液,溶液中
,MOH为一元弱碱。常温下,在含HX、HY、MNO3的混合溶液中滴加NaOH溶液,溶液中 与pH的关系如图所示。下列叙述正确的是
与pH的关系如图所示。下列叙述正确的是
| A.L1代表HX |
B.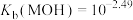 |
C. 的平衡常数K=10﹣2.26 的平衡常数K=10﹣2.26 |
D.MY溶液中, |
您最近半年使用:0次

 的
的 标准溶液滴定浓度均为
标准溶液滴定浓度均为 和
和 混合待测溶液,滴定过程中溶液的
混合待测溶液,滴定过程中溶液的 随
随 (
( )的变化曲线如图所示。下列说法正确的是
)的变化曲线如图所示。下列说法正确的是