几种主族元素在周期表中的位置如下:
(1)①⑨形成的化合物属于___________ (填“离子化合物”或“共价化合物”),用电子式表示其形成过程___________ 。
(2)以上元素的最高价氧化物对应的水化物的酸性最强的分子式为___________ 。
(3)比较⑦、⑧简单氢化物的还原性:___________ (填化学式);比较①、⑥、⑦三种简单离子的半径大小,其由大到小的顺序___________ (填离子符号)。
(4)下列可以判断①和③金属性强弱的是___________(填字母)。
(5)金属镓 常用作光学玻璃、真空管、半导体的原料。
常用作光学玻璃、真空管、半导体的原料。
预测 的化学性质并填写表格:
的化学性质并填写表格:
以上预测都是依据___________ 。
 | 0 | |||||||
| 1 | ④ |  |  |  | 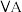 | 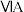 | 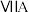 | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑨ | ⑦ | ||||
| 4 | ② |  | ⑧ | |||||
(2)以上元素的最高价氧化物对应的水化物的酸性最强的分子式为
(3)比较⑦、⑧简单氢化物的还原性:
(4)下列可以判断①和③金属性强弱的是___________(填字母)。
A.单质的熔点: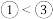 | B.化合价: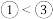 |
| C.单质与水反应的剧烈程度:①>③ | D.最高价氧化物对应水化物的碱性:①>③ |
 常用作光学玻璃、真空管、半导体的原料。
常用作光学玻璃、真空管、半导体的原料。预测
 的化学性质并填写表格:
的化学性质并填写表格:| 预测性质(所填物质类别不同) | 反应后可能的生成物(填化学式) |
 能与 能与 | 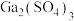 、 、 |
 能与 能与 | 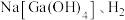 |
更新时间:2024-04-04 05:44:36
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】下表列出了a~z15种元素在周期表中的位置:
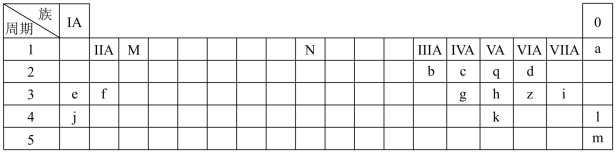
(1)元素b为___________ (填名称);画出g的原子结构示意图_____________ 。
(2)写出M、N分别表示的族序数为_________ 、___________ 。元素f、i、j的原子分别形成简单离子后,离子半径从大到小的顺序是_______________ (用离子符号表示)。元素l、m原子序数之差为_____ 。
(3)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为_____________ ,该化合物中化学键有__________ ,该化合物可与z的一种氧化物发生化合反应,写出该反应的化学方程式为______________________________________________ 。
(4)根据元素周期表推测k元素及其化合物的性质正确的是_________
A.气态氢化物的稳定性:k>h>q B.k所在的主族元素通常用于制造农药和半导体材料
C.k的最高正价为+6 D.氢化物的沸点:q>k
(5)f与q形成的离子化合物可以与d的氢化物发生反应,写出该反应的化学方程式为_______________ 。

(1)元素b为
(2)写出M、N分别表示的族序数为
(3)元素d和e形成的一种化合物为淡黄色固体,该化合物的电子式为
(4)根据元素周期表推测k元素及其化合物的性质正确的是
A.气态氢化物的稳定性:k>h>q B.k所在的主族元素通常用于制造农药和半导体材料
C.k的最高正价为+6 D.氢化物的沸点:q>k
(5)f与q形成的离子化合物可以与d的氢化物发生反应,写出该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知五种元素原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成的离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子。试回答下列问题:
(1) 写出C元素的名称是___________________
(2) 用电子式表示离子化合物A2B的形成过程_____________________________ ;
(3) 写出下列物质的电子式:E与B形成的化合物_______________ ;A、B、E形成的化合物
____________ ;D、E形成的化合物_____________ 。
(4) A、B两元素组成的化合物A2B2属于___________ (离子或共价)化合物,存在的化学键____________________________________ 。
(1) 写出C元素的名称是
(2) 用电子式表示离子化合物A2B的形成过程
(3) 写出下列物质的电子式:E与B形成的化合物
(4) A、B两元素组成的化合物A2B2属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素周期表是学习化学的重要工具,它隐含着许多信息和规律.下表所列是五种短周期的原子半径及主要化合价(已知铍的原子半径为0.089nm).
(1)C元素在元素周期表中的位置是______ ;
(2)B的原子结构示意图为______ ;
(3)D、E气态氢化物的稳定性强弱顺序为______ (填化学式);
(4)上述七种元素的最高价氧化物对应水化物中酸性最强的是______ (填化学式);
(5)以C为材料制成的容器不能贮存强碱溶液,用离子方程式表示其原因为:______ ;
(6)碲(52Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理的性能改变而记录、储存信号.推测碲元素在周期表中的位置,则碲元素及其化合物可能具有的性质为:______ ;
A.单质碲在常温下是固体 B.Cl2通入H2Te溶液中不发生反应
C.H2Te不如HI稳定 D.H2TeO4的酸性比H2SO4的弱
| 元素代号 | A | B | C | D | E | F | G |
| 原子半径/nm | 0.037 | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 | 0.075 |
| 主要化合价 | +1 | +2 | +3 | +6、-2 | -1 | -2 | +5、-3 |
(1)C元素在元素周期表中的位置是
(2)B的原子结构示意图为
(3)D、E气态氢化物的稳定性强弱顺序为
(4)上述七种元素的最高价氧化物对应水化物中酸性最强的是
(5)以C为材料制成的容器不能贮存强碱溶液,用离子方程式表示其原因为:
(6)碲(52Te)的某化合物是常用的VCR光盘记录材料之一,可在激光照射下发生化学或物理的性能改变而记录、储存信号.推测碲元素在周期表中的位置,则碲元素及其化合物可能具有的性质为:
A.单质碲在常温下是固体 B.Cl2通入H2Te溶液中不发生反应
C.H2Te不如HI稳定 D.H2TeO4的酸性比H2SO4的弱
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,下图是元素周期表的一部分,回答下列问题:
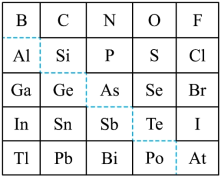
(1)元素Ga在元素周期表中的位置为:______ ;
(2)Sn的最高正价为______ ,C1的最高价氧化物对应水化物的化学式为______ ;
(3)根据元素周期律,推断
①表中元素形成的氢化物中热稳定性最高的是______ (写化学式),其电子式为______ 。
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4______ H2SeO4(填“>”、<”、“=”或“无法比较”);
③氢化物的还原性:H2O______ H2S(填“>”、“<”、“=”或“无法比较”)。
④原子半径比较:N______ Si(填“>”、“<”、“=”或“无法比较”)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断
①表中元素形成的氢化物中热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4
③氢化物的还原性:H2O
④原子半径比较:N
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】右表为元素周期表的一部分。回答下列问题:
(1)Z的元素符号为_________________ 。
(2)X位于元素周期表第_______ 周期_______ 族。
(3)W与Y形成的化合物WY中,W的化合价是________ 。
(4)硫的最简单氢化物与硫的低价氧化物通入水中时,发生反应的化学方程式为_________________________ 。
| W | 氮 | Y | |
| X | 硫 | Z |
(1)Z的元素符号为
(2)X位于元素周期表第
(3)W与Y形成的化合物WY中,W的化合价是
(4)硫的最简单氢化物与硫的低价氧化物通入水中时,发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】科学家们在探索生命奥秘的过程中,认识到生命细胞的组成和元素周期律有着密切的联系,约占人体总质量99.97%的11种大量元素全部位于元素周期表前20号元素,其余0.03%是由10多种人体不可缺少的微量元素组成。现有a~g 7种短周期元素,是除氧、硫、钾、钙外的其他大量元素,它们在元素周期表中的位置如下,请据此回答下列问题:
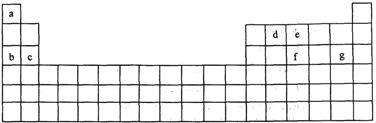
(1)元素的原子间反应最容易形成离子键的是下列中的( ) ,元素的原子间反应容易形成共价键的是下列中的( )
A.c和f B.b和g C.d和g D.d和e
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是( ) 。
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为__________________ 。
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式_______ ,化学键类型为____ ,与稀盐酸反应的方程式为_____________________ .

(1)元素的原子间反应最容易形成离子键的是下列中的
A.c和f B.b和g C.d和g D.d和e
(2)下列由a~g形成的各分子中,所有原子都满足最外层为8电子结构的是
A.ea3 B.ag C.fg3 D.dg4
(3)由11种元素的几种非金属元素构成的离子化合物的电子式为
(4)c与e可形成一种化合物,试根据原子结构写出该化合物的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硫及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)S在元素周期表中位于第______ 族,属于______ 区。
(2)基态S原子的价层电子轨道表示式为______ ,其原子核外电子共有______ 种空间运动状态。
(3)完成下列比较(填“>”、“<”或“=”)。
第一电离能:S______ P;电负性:S______ O;半径:
______ Na+。
(4)已知:25℃时 的电离常数:
的电离常数:
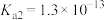 ,则NaHS的水解常数
,则NaHS的水解常数
______ ,NaHS溶液的pH______ 7(填“>”“<”或“=”)。
(5)锅炉水垢既会降低燃料的利用率,又会影响锅炉的使用寿命。为了除去水垢中的 可先用
可先用 溶液处理,写出该反应的离子方程式:
溶液处理,写出该反应的离子方程式:__________________ 。
(6)0.1 mol/L 溶液中各种离子浓度由大到小的顺序是
溶液中各种离子浓度由大到小的顺序是______ 。
(1)S在元素周期表中位于第
(2)基态S原子的价层电子轨道表示式为
(3)完成下列比较(填“>”、“<”或“=”)。
第一电离能:S

(4)已知:25℃时
 的电离常数:
的电离常数:
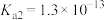 ,则NaHS的水解常数
,则NaHS的水解常数
(5)锅炉水垢既会降低燃料的利用率,又会影响锅炉的使用寿命。为了除去水垢中的
 可先用
可先用 溶液处理,写出该反应的离子方程式:
溶液处理,写出该反应的离子方程式:(6)0.1 mol/L
 溶液中各种离子浓度由大到小的顺序是
溶液中各种离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下图是短周期元素①~⑤在元素周期表中的位置。

(1)②在周期表中的位置是第___________ 周期第___________ 族,其与 反应的化学方程式是
反应的化学方程式是___________ 。
(2)③的一种核素的中子数是10,表示该核素的符号是___________ 。
(3)非金属性:④___________ ⑤(填“>”或“<”),从原子结构角度解释其原因:___________ 。
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程___________ 。
(5)下列关于①的说法正确的是___________ 。
a、原子结构示意图为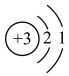
b、在同周期中,①最高价氧化物的水化物的碱性最强
c、在同主族的元素中,①的金属性最强

(1)②在周期表中的位置是第
 反应的化学方程式是
反应的化学方程式是(2)③的一种核素的中子数是10,表示该核素的符号是
(3)非金属性:④
(4)②、⑤两种元素形成的化合物有重要的用途,用电子式表示它的形成过程
(5)下列关于①的说法正确的是
a、原子结构示意图为

b、在同周期中,①最高价氧化物的水化物的碱性最强
c、在同主族的元素中,①的金属性最强
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】氧族元素的单质及其化合物对人类的生活、生产有着举足轻重的影响。如氧气、水、臭氧、二氧化硫等。
(1)在氧、硫、硒、碲元素原子形成的简单阴离子中,其离子半径由大到小的顺序为_________ (用离子符号表示)。与硫元素同周期且在本周期中非金属性最强的元素在周期表中的位置_______ 。
(2)氧族元素的单质及其化合物的性质存在着相似性和递变性。下列有关说法正确的是________
A.氧族元素气态氢化物的稳定性按H2O、H2S、H2Se、H2Te的顺序依次减弱
B.其氢化物中的键长按O—H、S—H、Se—H、Te—H的顺序依次减小
C.其阴离子的还原性按O2–、S2–、Se2–、Te2–的顺序依次增强
D.其最高价氧化物的水化物酸性按H2SO4、H2SeO4、H2TeO4顺序依次增强
(3)火山喷发时会释放出许多H2S气体,请写出H2S分子的电子式____________ 。在H2S分子中, 两个H—S键之间的夹角_____________ (填“大于”、“小于”或“等于”)180°,H2S分子属_____ (填“极性”或“非极性”)分子。
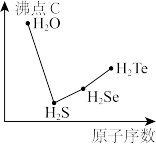
(4)从图可知氧族元素氢化物的沸点变化规律是____________________ 。
(1)在氧、硫、硒、碲元素原子形成的简单阴离子中,其离子半径由大到小的顺序为
(2)氧族元素的单质及其化合物的性质存在着相似性和递变性。下列有关说法正确的是
A.氧族元素气态氢化物的稳定性按H2O、H2S、H2Se、H2Te的顺序依次减弱
B.其氢化物中的键长按O—H、S—H、Se—H、Te—H的顺序依次减小
C.其阴离子的还原性按O2–、S2–、Se2–、Te2–的顺序依次增强
D.其最高价氧化物的水化物酸性按H2SO4、H2SeO4、H2TeO4顺序依次增强
(3)火山喷发时会释放出许多H2S气体,请写出H2S分子的电子式

(4)从图可知氧族元素氢化物的沸点变化规律是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】离子键
(1)离子键的形成过程(以氯化钠的形成过程为例)
钠原子和氯原子最外层电子数分别为1和7,均不稳定。
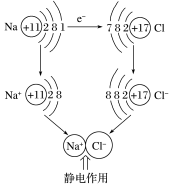
即它们通过得失电子后最外层达到____ 稳定结构,分别形成Na+和Cl-,两种带相反电荷的离子通过_____ 结合在一起,形成新物质氯化钠。
(2)离子键
①概念:____ 之间存在的_____ 的相互作用。
②构成微粒:_____ 。
③实质:____ 。
(1)离子键的形成过程(以氯化钠的形成过程为例)
钠原子和氯原子最外层电子数分别为1和7,均不稳定。

即它们通过得失电子后最外层达到
(2)离子键
①概念:
②构成微粒:
③实质:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氨气是一种重要的化工产品,是生产尿素的原料。工业合成氨的反应如下:
N2(g) +3H2(g) 2NH3(g) △H= - 92. 2 KJ·mol-1
2NH3(g) △H= - 92. 2 KJ·mol-1
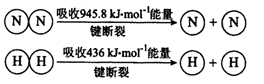
(1)1mol N-H键断裂吸收的能量为_______ kJ。
(2)对于N2(g) +3H2(g) 2NH3(g) △H= - 92. 2 KJ·mol-1反应
2NH3(g) △H= - 92. 2 KJ·mol-1反应
①只改变某一条件,一定可以提高平衡体系中H2的转化率,又能加快反应速率的措施是( ) 。
A.升高温度 B.移走NH3 C.加入催化剂 D.再充入N2
②向1L密闭容器中加入1mol N2、3molH2,下列叙述能说明此反应达到平衡状态的是( ) 。
A.混合气体的平均相对分子质量保持不变 B.N2和H2的转化率相等
C. H2的体积分数保持不变 D.混合气体的密度保持不变
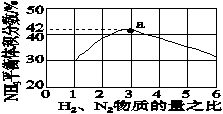
(3)下图表示500 ℃、60.0 MPa条件下,原料气H2、 N2投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:_______ 。(保留3位有效数字)
(4)合成尿素的反应:2NH3(g)+CO (g) CO(NH2)2(g)+H2(g) △H = - 81.0kJ/mol;T℃时,在体积为2L的恒容密闭容器中,将2 mol的NH3和1mol CO混合反应,5 min时,NH3的转化率为80%。已知:
CO(NH2)2(g)+H2(g) △H = - 81.0kJ/mol;T℃时,在体积为2L的恒容密闭容器中,将2 mol的NH3和1mol CO混合反应,5 min时,NH3的转化率为80%。已知:

则:K1_________ 126.5(填“>”或“< ”);其判断理由是________ 。
N2(g) +3H2(g)
 2NH3(g) △H= - 92. 2 KJ·mol-1
2NH3(g) △H= - 92. 2 KJ·mol-1
(1)1mol N-H键断裂吸收的能量为
(2)对于N2(g) +3H2(g)
 2NH3(g) △H= - 92. 2 KJ·mol-1反应
2NH3(g) △H= - 92. 2 KJ·mol-1反应①只改变某一条件,一定可以提高平衡体系中H2的转化率,又能加快反应速率的措施是
A.升高温度 B.移走NH3 C.加入催化剂 D.再充入N2
②向1L密闭容器中加入1mol N2、3molH2,下列叙述能说明此反应达到平衡状态的是
A.混合气体的平均相对分子质量保持不变 B.N2和H2的转化率相等
C. H2的体积分数保持不变 D.混合气体的密度保持不变
(3)下图表示500 ℃、60.0 MPa条件下,原料气H2、 N2投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:

(4)合成尿素的反应:2NH3(g)+CO (g)
 CO(NH2)2(g)+H2(g) △H = - 81.0kJ/mol;T℃时,在体积为2L的恒容密闭容器中,将2 mol的NH3和1mol CO混合反应,5 min时,NH3的转化率为80%。已知:
CO(NH2)2(g)+H2(g) △H = - 81.0kJ/mol;T℃时,在体积为2L的恒容密闭容器中,将2 mol的NH3和1mol CO混合反应,5 min时,NH3的转化率为80%。已知:
则:K1
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题:
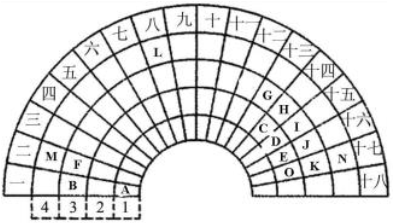
(1)L元素在常见周期表中所处的位置是________ ,其单质与A2E反应的化学方程式为____________ 。
(2)元素F、G、J、K、M对应简单离子的离子半径由大到小的顺序是(用离子符号表示)___________ 。
(3)用电子式表示MO2的形成过程:_______________ 。
(4)B、F、G三种元素最高价氧化物对应的水化物碱性最强的是__________ (填化学式)。比较元素C和J的非金属性强弱:C______ J(填“强于”或“弱于”)。
(5)向元素B和N形成的化合物的水溶液中,加入元素K的单质,所发生的反应的离子方程式为_____ ;反应后,向溶液中加入C、K形成的化合物,现象为___________ 。
(6)均由A、B、E、J四种元素组成的两种化合物可相互反应,写出反应的化学方程式______________ 。

(1)L元素在常见周期表中所处的位置是
(2)元素F、G、J、K、M对应简单离子的离子半径由大到小的顺序是(用离子符号表示)
(3)用电子式表示MO2的形成过程:
(4)B、F、G三种元素最高价氧化物对应的水化物碱性最强的是
(5)向元素B和N形成的化合物的水溶液中,加入元素K的单质,所发生的反应的离子方程式为
(6)均由A、B、E、J四种元素组成的两种化合物可相互反应,写出反应的化学方程式
您最近一年使用:0次



