汽车尾气(含 、
、 、CO、
、CO、 、
、 等)是城市空气的污染源之一、
等)是城市空气的污染源之一、
(1)汽车尾气对环境的危害主要有温室效应、雾霾、_______ 等。
(2)在三元催化装置的作用下,汽车尾气可转化为无污染的物质。写出CO与 在此条件下反应的化学方程式:
在此条件下反应的化学方程式:_______ ,消耗14gCO时,转移电子的物质的量是_______ mol。
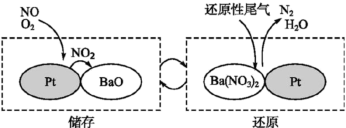
(3) 储存还原技术可有效降低柴油发动机在空气过量条件下
储存还原技术可有效降低柴油发动机在空气过量条件下 的排放。如图所示,
的排放。如图所示, 的储存和还原在不同时段交替进行,通过BaO和
的储存和还原在不同时段交替进行,通过BaO和 的相互转化实现
的相互转化实现 的储存和还原。储存
的储存和还原。储存 的物质是
的物质是_______ 。
(4) 也可以用于催化转化NOx,减少空气污染。请写出实验室用铵盐制备
也可以用于催化转化NOx,减少空气污染。请写出实验室用铵盐制备 的反应方程式
的反应方程式_______ 。
(5)若将 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有_______ (填离子符号)。
 、
、 、CO、
、CO、 、
、 等)是城市空气的污染源之一、
等)是城市空气的污染源之一、(1)汽车尾气对环境的危害主要有温室效应、雾霾、
(2)在三元催化装置的作用下,汽车尾气可转化为无污染的物质。写出CO与
 在此条件下反应的化学方程式:
在此条件下反应的化学方程式:(3)
 储存还原技术可有效降低柴油发动机在空气过量条件下
储存还原技术可有效降低柴油发动机在空气过量条件下 的排放。如图所示,
的排放。如图所示, 的储存和还原在不同时段交替进行,通过BaO和
的储存和还原在不同时段交替进行,通过BaO和 的相互转化实现
的相互转化实现 的储存和还原。储存
的储存和还原。储存 的物质是
的物质是
(4)
 也可以用于催化转化NOx,减少空气污染。请写出实验室用铵盐制备
也可以用于催化转化NOx,减少空气污染。请写出实验室用铵盐制备 的反应方程式
的反应方程式(5)若将
 固体投入到含有下列离子的溶液中:
固体投入到含有下列离子的溶液中: 、
、 、
、 、
、 ,反应完毕后,溶液中上述离子数目几乎不变的有
,反应完毕后,溶液中上述离子数目几乎不变的有
更新时间:2024-04-09 21:19:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】 是一种重要的杀菌消毒剂,也常用来漂白织物等。其一种生产工艺如图:
是一种重要的杀菌消毒剂,也常用来漂白织物等。其一种生产工艺如图:

(1)写出“反应”步骤中生成 的化学方程式:
的化学方程式:_______ 。
(2)“尾气吸收”是吸收“电解”过程排出的少量 。写出“尾气吸收”的化学方程式:
。写出“尾气吸收”的化学方程式:_______ 。此吸收反应中,氧化剂与还原剂的物质的量之比为_______ 。
 是一种重要的杀菌消毒剂,也常用来漂白织物等。其一种生产工艺如图:
是一种重要的杀菌消毒剂,也常用来漂白织物等。其一种生产工艺如图:
(1)写出“反应”步骤中生成
 的化学方程式:
的化学方程式:(2)“尾气吸收”是吸收“电解”过程排出的少量
 。写出“尾气吸收”的化学方程式:
。写出“尾气吸收”的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】
(1)+6价铬的化合物毒性较大,常用NaHSO3将废液中的 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为__________________________________________________________ 。
(2)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为____________________________________ 。
(3)“酸浸”时V2O5转化为 ,反应的离子方程式为
,反应的离子方程式为________________________________________ 。
(4)在H2SO4的酸性环境中ClO2与碘化钾反应的离子方程式___________________________ 。
(5)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为__________________________ 。
(1)+6价铬的化合物毒性较大,常用NaHSO3将废液中的
 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为(2)向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程式为
(3)“酸浸”时V2O5转化为
 ,反应的离子方程式为
,反应的离子方程式为(4)在H2SO4的酸性环境中ClO2与碘化钾反应的离子方程式
(5)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)写出除去或分离括号内物质所用方法(填序号):
a.加热法b.过滤c.渗析d.水洗法e.升华法f.萃取和分液g.沉淀法
①碳酸钠(碳酸氢钠)_____ ;
②一氧化氮(二氧化氮)_____ ;
③氯化钠(I2)_____ ;
④氢氧化铁胶体中的离子_____ ;
⑤碘水中碘单质_____ ;
⑥氯化钠(硫酸钠)_____ 。
(2)①写出实验室中由固体物质制取氨气的化学方程式_____ 。
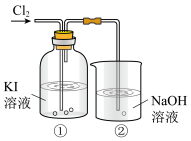
②欲用上述方法制取并收集一瓶干燥的氨气,从图中选择合适的装置,其连接顺序为_____ 。(按气流方向,用小写字母表示,如x→y→z)。

a.加热法b.过滤c.渗析d.水洗法e.升华法f.萃取和分液g.沉淀法
①碳酸钠(碳酸氢钠)
②一氧化氮(二氧化氮)
③氯化钠(I2)
④氢氧化铁胶体中的离子
⑤碘水中碘单质
⑥氯化钠(硫酸钠)
(2)①写出实验室中由固体物质制取氨气的化学方程式
②欲用上述方法制取并收集一瓶干燥的氨气,从图中选择合适的装置,其连接顺序为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】“价—类”二维图反映的是元素化合价与物质类别之间的关系,构建“价—类”二维图是元素化合物学习的重要方法。下图是氮元素的“价—类”二维图。

回答下列问题:
(1)B的电子式为___________ 。
(2)实验室制备A可选用下图的___________ (填“①”或“②”),写出该装置发生反应的化学方程式:___________ 。

(3)I电离可使溶液显碱性,写出I的电离方程式:___________ 。
(4)C、D均为大气污染物,工业上可用氢氧化钠溶液吸收C和D,同时生成H,写出该反应的离子方程式:___________
(5)将一定质量的铜与一定量的浓硝酸混合,恰好完全反应,刚开始反应的现象为___________ ,反应得到硝酸铜溶液和C、D的混合气体,若使混合气体完全溶于水生成F需要标准状况下 1.68L,则参加反应的铜的质量为
1.68L,则参加反应的铜的质量为___________ g。
(6)实验室检验J的水溶液中阳离子的操作方法为___________ 。

回答下列问题:
(1)B的电子式为
(2)实验室制备A可选用下图的

(3)I电离可使溶液显碱性,写出I的电离方程式:
(4)C、D均为大气污染物,工业上可用氢氧化钠溶液吸收C和D,同时生成H,写出该反应的离子方程式:
(5)将一定质量的铜与一定量的浓硝酸混合,恰好完全反应,刚开始反应的现象为
 1.68L,则参加反应的铜的质量为
1.68L,则参加反应的铜的质量为(6)实验室检验J的水溶液中阳离子的操作方法为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】人类农业生产离不开氮肥,科学合理使用氰肥,不仅能提高化肥的使用率,而且能够更好地保护环境,请回答下列问题:
(1)工业合成氨是制取氮肥的基础。写出工业合成氨的化学反应方程式___________ 。
(2)某小组在实验室模拟以 为原料,制备少量硝态氮肥
为原料,制备少量硝态氮肥 ,转化途径如下(转化所需试剂及条件已略去)。
,转化途径如下(转化所需试剂及条件已略去)。

①写出实验室用 和消石灰共热制备氨气的化学反应方程式
和消石灰共热制备氨气的化学反应方程式___________ 。
②写出 发生催化氧化反应生成
发生催化氧化反应生成 的化学方程式
的化学方程式___________ 。
③将 转化为
转化为 ,列举两种不同类别的化合物M
,列举两种不同类别的化合物M___________ (写化学式)。
(3) 是一种铵态氮肥,需阴凉处保存,原因是
是一种铵态氮肥,需阴凉处保存,原因是___________ (写化学方程式)。
(4)过渡施用氮肥将导致大气中 含量增高,加剧雾霾的形成。
含量增高,加剧雾霾的形成。 是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去)
是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去)
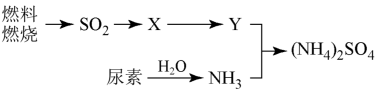
①X可能是 或
或___________ 。
②尿素 是一种常用有机氮肥,缓慢与
是一种常用有机氮肥,缓慢与 发生非氧化还原反应释放出
发生非氧化还原反应释放出 和另外一种气体,该反应的化学方程式为
和另外一种气体,该反应的化学方程式为___________ 。
(1)工业合成氨是制取氮肥的基础。写出工业合成氨的化学反应方程式
(2)某小组在实验室模拟以
 为原料,制备少量硝态氮肥
为原料,制备少量硝态氮肥 ,转化途径如下(转化所需试剂及条件已略去)。
,转化途径如下(转化所需试剂及条件已略去)。
①写出实验室用
 和消石灰共热制备氨气的化学反应方程式
和消石灰共热制备氨气的化学反应方程式②写出
 发生催化氧化反应生成
发生催化氧化反应生成 的化学方程式
的化学方程式③将
 转化为
转化为 ,列举两种不同类别的化合物M
,列举两种不同类别的化合物M(3)
 是一种铵态氮肥,需阴凉处保存,原因是
是一种铵态氮肥,需阴凉处保存,原因是(4)过渡施用氮肥将导致大气中
 含量增高,加剧雾霾的形成。
含量增高,加剧雾霾的形成。 是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去)
是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去)
①X可能是
 或
或②尿素
 是一种常用有机氮肥,缓慢与
是一种常用有机氮肥,缓慢与 发生非氧化还原反应释放出
发生非氧化还原反应释放出 和另外一种气体,该反应的化学方程式为
和另外一种气体,该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】化学与人类生活密切相关。请按要求,回答下列问题:
(1)漂白粉有效成分的化学式为_____ ,其能消毒杀菌是因有强_____ 性。
(2)KAl(SO4)2•12H2O的俗名为_____ ,因其溶于水生成_____ 而具有净水作用。
(3)酸雨的pH小于_____ ,含亚硫酸的酸雨久置后pH_____ (增大、减小或不变)。
(4)小苏打可用于治疗胃酸过多,其反应的离子方程式为_____ 。
(1)漂白粉有效成分的化学式为
(2)KAl(SO4)2•12H2O的俗名为
(3)酸雨的pH小于
(4)小苏打可用于治疗胃酸过多,其反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列小题
(1)为什么化学变化中总是伴随着能量的变化_____ ?
(2)如何除去NO气体中混有的少量的NO2气体杂质_____ ?
(3)酸雨的产生那些物质有关?酸雨造成的危害有哪些_____ ?
(1)为什么化学变化中总是伴随着能量的变化
(2)如何除去NO气体中混有的少量的NO2气体杂质
(3)酸雨的产生那些物质有关?酸雨造成的危害有哪些
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】近年来,我国秋冬季雾霾天气呈现常态化趋势,造成严重空气污染,对人类身心健康造成极大威胁。硫酸盐气溶胶作为PM2.5的主要构成成分,是雾霾产生的一个重要元凶。科学家最近发现了一种利用水催化促进硫酸盐形成的化学新机制。如图所示:

(1)NO2和SO2作为大气初期污染物的主要成分,主要来自___________ 。
(2)电子传递可以促进HSO 中O—H键的解离,进而形成中间体SO
中O—H键的解离,进而形成中间体SO ,反应的离子方程式为
,反应的离子方程式为___________ 。
(3)通过“水分子桥”,处于纳米液滴中的SO 或HSO
或HSO 可以将电子快速转移到周围的气相NO2分子。写出HSO
可以将电子快速转移到周围的气相NO2分子。写出HSO 与NO2间发生的总反应的离子方程式:
与NO2间发生的总反应的离子方程式:___________ 。
(4)亚硝酸(HNO2)是一种弱酸,酸性比醋酸稍强,极不稳定,只能存在于稀的水溶液中,加热时发生歧化反应,生成一种强酸和一种遇空气变为红棕色的气体,写出该反应的化学方程式:___________ 。
(5)结合题中信息,请写出一种鉴别NaNO2和NaCl的方法:___________ 。

(1)NO2和SO2作为大气初期污染物的主要成分,主要来自
(2)电子传递可以促进HSO
 中O—H键的解离,进而形成中间体SO
中O—H键的解离,进而形成中间体SO ,反应的离子方程式为
,反应的离子方程式为(3)通过“水分子桥”,处于纳米液滴中的SO
 或HSO
或HSO 可以将电子快速转移到周围的气相NO2分子。写出HSO
可以将电子快速转移到周围的气相NO2分子。写出HSO 与NO2间发生的总反应的离子方程式:
与NO2间发生的总反应的离子方程式:(4)亚硝酸(HNO2)是一种弱酸,酸性比醋酸稍强,极不稳定,只能存在于稀的水溶液中,加热时发生歧化反应,生成一种强酸和一种遇空气变为红棕色的气体,写出该反应的化学方程式:
(5)结合题中信息,请写出一种鉴别NaNO2和NaCl的方法:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】某银白色金属单质A在空气中加热燃烧时发出黄色火焰,得到淡黄色固体B,A露置在空气中足够长时间变为C,B和酸性气体D能生成C,A和B都能与水生成E,E和D也能生成C。回答下列问题。
(1)写出下列物质的化学式:C______ ,D______ ,E______ 。
(2)写出下列反应的化学方程式:
①A和水生成E:______ 。
②B和D生成C:______ 。
③Cl2与E的水溶液:______ 。
(1)写出下列物质的化学式:C
(2)写出下列反应的化学方程式:
①A和水生成E:
②B和D生成C:
③Cl2与E的水溶液:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】卫生部发出公告,禁止在面粉生产中添加过氧化钙(CaO2)等食品添加剂。过氧化钙(CaO2)是一种安全无毒物质,带有结晶水,通常还含有CaO,过氧化钙(CaO2)与过氧化钠(Na2O2)性质相似,都会与H2O和酸反应。

(1)下列对于过氧化钙(CaO2)的叙述错误的是______
A.CaO2具有氧化性,对面粉可能具有增白作用
B.CaO2中阴阳离子的个数比为1∶1
C.CaO2和水反应时,每产生1 mol O2转移电子4 mol
D.CaO2和CO2反应的化学方程式为:2CaO2+2CO2=2CaCO3+O2
(2)写出过氧化钙(CaO2)与盐酸反应的离子方程式______ 。
(3)某化学学习小组为测定过氧化钙样品(含有CaO杂质)中过氧化钙的结晶水的数目,做如下实验:
实验一: 称取5.42 g过氧化钙样品,灼热时发生如下反应:2[CaO2·xH2O]=2CaO+O2↑+2xH2O,得到O2在标准状况下体积为672 mL。
实验二:另取同一样品5.42 g,溶于适量稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 7.0 g。
①5.42 g过氧化钙样品中CaO2的物质的量为______ 。
②该样品中CaO2·xH2O的x值为______ 。

(1)下列对于过氧化钙(CaO2)的叙述错误的是
A.CaO2具有氧化性,对面粉可能具有增白作用
B.CaO2中阴阳离子的个数比为1∶1
C.CaO2和水反应时,每产生1 mol O2转移电子4 mol
D.CaO2和CO2反应的化学方程式为:2CaO2+2CO2=2CaCO3+O2
(2)写出过氧化钙(CaO2)与盐酸反应的离子方程式
(3)某化学学习小组为测定过氧化钙样品(含有CaO杂质)中过氧化钙的结晶水的数目,做如下实验:
实验一: 称取5.42 g过氧化钙样品,灼热时发生如下反应:2[CaO2·xH2O]=2CaO+O2↑+2xH2O,得到O2在标准状况下体积为672 mL。
实验二:另取同一样品5.42 g,溶于适量稀盐酸中,然后加入足量的Na2CO3溶液,将溶液中Ca2+全部转化为CaCO3沉淀,得到干燥的CaCO3 7.0 g。
①5.42 g过氧化钙样品中CaO2的物质的量为
②该样品中CaO2·xH2O的x值为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图转化关系中已知A是Na2O2,甲是气体,B、F两种气体都能使澄清石灰水变浑浊。F气体使品红溶液褪色,加热又恢复原色, H是一种强酸;丙是一种金属单质。(部分反应物或产物略去)

(1)写出下列物质的化学式:甲_______ D_______ G________
(2)写出下列反应的化学方程式:
A与B__________________________________
H→F___________________________________
(3)丙投入浓H溶液中,无明显变化,原因是______________ 。

(1)写出下列物质的化学式:甲
(2)写出下列反应的化学方程式:
A与B
H→F
(3)丙投入浓H溶液中,无明显变化,原因是
您最近一年使用:0次