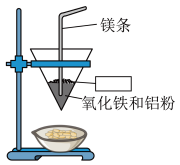
将铝与氧化铁混合制备单质铁的反应称为铝热反应,反应装置如图所示:_____ 。
(2)该铝热反应的化学方程式为_____ ,引发铝热反应的实验操作是_____ 。
(3)取少量反应所得的固体混合物,将其溶于足量稀 ,滴加KSCN溶液无明显现象,能否说明固体混合物中已无
,滴加KSCN溶液无明显现象,能否说明固体混合物中已无 ,请判断并说明理由
,请判断并说明理由_____ 。
(4)写出一种铝热反应的实际应用_____ 。
(2)该铝热反应的化学方程式为
(3)取少量反应所得的固体混合物,将其溶于足量稀
 ,滴加KSCN溶液无明显现象,能否说明固体混合物中已无
,滴加KSCN溶液无明显现象,能否说明固体混合物中已无 ,请判断并说明理由
,请判断并说明理由(4)写出一种铝热反应的实际应用
23-24高一下·上海奉贤·阶段练习 查看更多[2]
更新时间:2024-04-17 22:20:12
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、X均为中学化学常见的物质。它们之间存在如下图所示转化关系(图中反应条件略去)填写下列空白:

(1)若A为金属铝,B为氧化铁,写出反应A+B→C+D的一种用途______
(2)若A为两性氢氧化物, B为NaOH溶液,写出反应A+B→C+D的离子方程式________________ 。
(3)若A为金属单质,B、C、D都是化合物,A与B发生的反应常用于刻制印刷电路板,该反应的离子方程式________________________________________ 。
(4)若A、B、C为化合物,D、X为单质,A、B、C中肯定含有X元素的是________

(1)若A为金属铝,B为氧化铁,写出反应A+B→C+D的一种用途
(2)若A为两性氢氧化物, B为NaOH溶液,写出反应A+B→C+D的离子方程式
(3)若A为金属单质,B、C、D都是化合物,A与B发生的反应常用于刻制印刷电路板,该反应的离子方程式
(4)若A、B、C为化合物,D、X为单质,A、B、C中肯定含有X元素的是
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】X、Y、Z为三种常见的单质,Z为绿色植物光合作用后的产物之一,A、B为常见化合物.它们在一定条件下可以发生如图反应(均不是在溶液中进行的反应)(以下每个空中只需填入一种物质)
(1)X、Y均为金属时,此反应在工业上称为___ 反应,其反应方程式为 ________
(2)X为金属,Y为非金属时,A为__ B__
(3)X为非金属Y为金属时,A为__ B为_______
(4)X为非金属,Y为非金属时,A为_____ B为______

(1)X、Y均为金属时,此反应在工业上称为
(2)X为金属,Y为非金属时,A为
(3)X为非金属Y为金属时,A为
(4)X为非金属,Y为非金属时,A为

您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】常温下D、E、F、I、J为气体,H、I、J都为氧化物;C的焰色反应为黄色;M为红褐色的固体,由G分解得到的H、I、J三者的物质的量相等.下图表示各物质之间的转化关系.
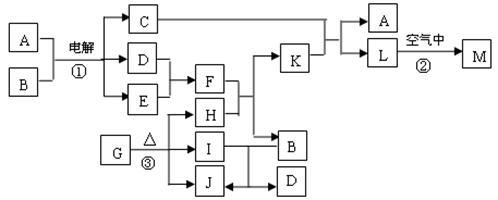
试回答下列问题:
(1)写出L的化学式____________ .
(2)基于反应①原理的化学工业称为______________ .
写出该反应①的离子方程式__________________________________________ .
(3)反应②的现象是__________________________________________ .
(4)写出H与Al在高温下反应的化学方程式___________________________________ .
(5)写出反应③的化学方程式___________________________________ .

试回答下列问题:
(1)写出L的化学式
(2)基于反应①原理的化学工业称为
写出该反应①的离子方程式
(3)反应②的现象是
(4)写出H与Al在高温下反应的化学方程式
(5)写出反应③的化学方程式
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】柠檬酸亚铁(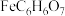 )是一种易吸收的高效铁制剂,工业上以硫铁矿(主要成分为
)是一种易吸收的高效铁制剂,工业上以硫铁矿(主要成分为 )为原料,制备柠檬酸亚铁,其流程如下:
)为原料,制备柠檬酸亚铁,其流程如下:

回答下列问题:
(1)在空气中焙烧时产生对环境有危害的气体是_______ (填化学式);培烧后得到的固体主要成分为 ,焙烧时反应的化学方程式是
,焙烧时反应的化学方程式是_______ 。
(2)滤渣1的成分为_______ (填化学式)。
(3)“还原”过程中与 有关的离子方程式为
有关的离子方程式为_______ ;加入Fe粉还原后,可用_______ (填试剂)检验还原反应是否已经完全反应。
(4)“沉铁”时,反应温度不宜太高的可能原因是_______ 。
(5)生成的 固体需充分洗涤,检验洗涤是否完全的方法是
固体需充分洗涤,检验洗涤是否完全的方法是_______ 。
(6)将制得的 加入到足量柠檬酸溶液中,充分反应后再加入少量铁粉。铁粉的作用是
加入到足量柠檬酸溶液中,充分反应后再加入少量铁粉。铁粉的作用是_______ 。
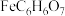 )是一种易吸收的高效铁制剂,工业上以硫铁矿(主要成分为
)是一种易吸收的高效铁制剂,工业上以硫铁矿(主要成分为 )为原料,制备柠檬酸亚铁,其流程如下:
)为原料,制备柠檬酸亚铁,其流程如下:
回答下列问题:
(1)在空气中焙烧时产生对环境有危害的气体是
 ,焙烧时反应的化学方程式是
,焙烧时反应的化学方程式是(2)滤渣1的成分为
(3)“还原”过程中与
 有关的离子方程式为
有关的离子方程式为(4)“沉铁”时,反应温度不宜太高的可能原因是
(5)生成的
 固体需充分洗涤,检验洗涤是否完全的方法是
固体需充分洗涤,检验洗涤是否完全的方法是(6)将制得的
 加入到足量柠檬酸溶液中,充分反应后再加入少量铁粉。铁粉的作用是
加入到足量柠檬酸溶液中,充分反应后再加入少量铁粉。铁粉的作用是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】铁是植物必须的一种微量营养元素,铁肥可以提高植物叶片的光合作用,让叶片更加翠绿。某研究小组同学欲探究某袋敞口放置一段时间的“硫酸亚铁家庭园艺精品肥料”的成分。同学们首先对这袋肥料可能出现的变化进行了如下预测:
a. 未被氧化 b.
未被氧化 b. 部分被氧化 c.
部分被氧化 c. 全部被氧化
全部被氧化
然后,取适量肥料固体粉末溶于水中并加入少量硫酸得到溶液(记为X),进行如下实验:
(1)对实验i的预期现象是开始产生白色沉淀,迅速变为灰绿色,最后出现红褐色沉淀。预期产生该现象的依据是(用化学方程式或离子方程式表达)___________ 、___________ 。
(2)通过以上实验,可得出的结论是预测___________ (填“a”“b”或“c”)不成立。
(3)为进一步探究,小组同学进行了以下实验:
实验ⅳ中溶液红色变深,是因为 与溶液X中某种离子发生了反应。反应的离子方程式是
与溶液X中某种离子发生了反应。反应的离子方程式是___________ 。
(4)通过以上实验,可得出的结论是预测___________ (填“a”“b”或“c”)成立。
(5)实验ⅳ中红色褪去的同时有气体生成,经检验为氧气。该小组同学对红色褪去的原因进行探究。
①取褪色后的溶液两份,第一份滴加氯化铁溶液无明显变化;第二份滴加KSCN溶液出现红色。
②另取同浓度的氯化铁溶液滴加2滴KSCN溶液,溶液变红,再通入氧气,无明显变化。
③在实验②后的溶液中加入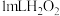 溶液,一段时间后溶液褪色,再滴加稀盐酸和氯化钡溶液,产生白色沉淀。
溶液,一段时间后溶液褪色,再滴加稀盐酸和氯化钡溶液,产生白色沉淀。
实验①说明___________ ;实验②的目的是___________ ;通过实验①②③,可以得出溶液褪色的原因是___________ 。
a.
 未被氧化 b.
未被氧化 b. 部分被氧化 c.
部分被氧化 c. 全部被氧化
全部被氧化然后,取适量肥料固体粉末溶于水中并加入少量硫酸得到溶液(记为X),进行如下实验:
| 序号 | 操作 | 现象 |
| i | 取2mL溶液X,加入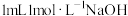 溶液 溶液 | 产生红褐色沉淀 |
| ii | 取2mL溶液X,加入少量KSCN溶液 | 溶液显红色 |
(2)通过以上实验,可得出的结论是预测
(3)为进一步探究,小组同学进行了以下实验:
| 序号 | 操作 | 现象 |
| ⅲ | 取2mL溶液X,加入少量KSCN溶液,再加入1mL水 | 溶液显红色,加水后红色变浅 |
| ⅳ | 取2mL溶液X,加入少量KSCN溶液,再加入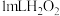 溶液 溶液 | 溶液显红色,加 溶液后颜色变深,静置一段时间后,溶液褪色 溶液后颜色变深,静置一段时间后,溶液褪色 |
 与溶液X中某种离子发生了反应。反应的离子方程式是
与溶液X中某种离子发生了反应。反应的离子方程式是(4)通过以上实验,可得出的结论是预测
(5)实验ⅳ中红色褪去的同时有气体生成,经检验为氧气。该小组同学对红色褪去的原因进行探究。
①取褪色后的溶液两份,第一份滴加氯化铁溶液无明显变化;第二份滴加KSCN溶液出现红色。
②另取同浓度的氯化铁溶液滴加2滴KSCN溶液,溶液变红,再通入氧气,无明显变化。
③在实验②后的溶液中加入
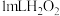 溶液,一段时间后溶液褪色,再滴加稀盐酸和氯化钡溶液,产生白色沉淀。
溶液,一段时间后溶液褪色,再滴加稀盐酸和氯化钡溶液,产生白色沉淀。实验①说明
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】一定量的铁粉在氯气中充分燃烧后,将所得固体完全溶于稀盐酸,制得溶液A。
(1)铁在氯气中燃烧的化学方程式是____________________________ 。
(2)推测A中可能含有的金属阳离子:①Fe3+;②只有Fe2+;③______ 。
甲同学为探究溶液的组成,实验如下:
(3)乙同学继续探究溶液A的组成。
查阅资料:16HCl+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O
实验过程:另取少量溶液A于试管中,逐滴加入酸性KMnO4溶液,充分振荡,KMnO4紫色褪去。
实验结论:__________ (填写字母序号)。
a.可能有Fe2+ b.可能无Fe2+ c.一定有Fe2+
(4)结论:A中含有的阳离子是_________ ,简述理由:________________ 。
(1)铁在氯气中燃烧的化学方程式是
(2)推测A中可能含有的金属阳离子:①Fe3+;②只有Fe2+;③
甲同学为探究溶液的组成,实验如下:
| 实验步骤 | 实验现象 | 实验结论及反应离子方程式 |
| 取少量溶液A于试管中,加入KSCN溶液。 | 假设②不成立,假设①或③成立;反应的离子方程式是 |
查阅资料:16HCl+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O
实验过程:另取少量溶液A于试管中,逐滴加入酸性KMnO4溶液,充分振荡,KMnO4紫色褪去。
实验结论:
a.可能有Fe2+ b.可能无Fe2+ c.一定有Fe2+
(4)结论:A中含有的阳离子是
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】向盛有10mL饱和氯化铁溶液的试管里投入足量铝片,观察到如下现象:
①黄色溶液很快变成红褐色,过一会儿溶液中有红褐色沉淀生成。
②铝片表面立刻有少量黑色物质析出,黑色物质能被磁铁吸起。
③混合液温度升高甚至发烫,产生无色气泡,且产生气泡速率明显加快,铝片上下翻滚。
(1)产生的红褐色沉淀是____________________ ,无色气泡的成分是____________________ 。
(2)产生无色气泡的原因是(用离子方程式表示)____________________ 。
(3)写出生成气泡速率明显加快的两个原因____________________ 、____________________ 。
①黄色溶液很快变成红褐色,过一会儿溶液中有红褐色沉淀生成。
②铝片表面立刻有少量黑色物质析出,黑色物质能被磁铁吸起。
③混合液温度升高甚至发烫,产生无色气泡,且产生气泡速率明显加快,铝片上下翻滚。
(1)产生的红褐色沉淀是
(2)产生无色气泡的原因是(用离子方程式表示)
(3)写出生成气泡速率明显加快的两个原因
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:______ 与盐酸反应最剧烈,____ 与盐酸反应的速度最慢;____ 与盐酸反应产生的气体最多.
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为______________________________ ;
(3)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:_________ ,________________ ;
Ⅱ.利用图装置可验证同主族元素非金属性的变化规律
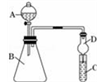
(4)干燥管D的作用为_______________ ;
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液________________________ 的现象,即可证明.但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有______________ 溶液的洗气瓶.
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
(3)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?并说明理由:
Ⅱ.利用图装置可验证同主族元素非金属性的变化规律

(4)干燥管D的作用为
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某校实验小组的同学利用下图所示实验装置探究氨与氧化铜的反应(图中夹持、固定装置均略去)。
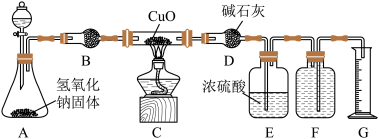
(1)按图设计组装好仪器,先__________________ ,再装入药品。
(2)A中分液漏斗内应装_________________ ,B中固体试剂为__________________ 。
(3)打开分液漏斗活塞,加入试剂,点燃C处的酒精灯,一段时间后,观察到C中氧化铜全部转化成光亮的红色固体,F中集气瓶内收集到一种无色气态单质。写出装置C中反应的化学方程式:______ 。
(4)E中浓硫酸的作用是__________________ 。
(5)用平衡移动原理解释A中产生气体的原因__________________________ 。(用相关的离子方程式和必要的文字描述)
(6)已知Cu2O也是红色的。下表为实验前后C装置的质量,通过计算可知反应后的产物中______ (填“有”、“无”或“无法确定”)Cu2O。

(1)按图设计组装好仪器,先
(2)A中分液漏斗内应装
(3)打开分液漏斗活塞,加入试剂,点燃C处的酒精灯,一段时间后,观察到C中氧化铜全部转化成光亮的红色固体,F中集气瓶内收集到一种无色气态单质。写出装置C中反应的化学方程式:
(4)E中浓硫酸的作用是
(5)用平衡移动原理解释A中产生气体的原因
(6)已知Cu2O也是红色的。下表为实验前后C装置的质量,通过计算可知反应后的产物中
| 空玻璃管 | 实验前(样品+玻璃管) | 实验后(样品+玻璃管) |
| 59.60 g | 65.60g | 64.64g |
您最近半年使用:0次



