柠檬酸亚铁(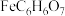 )是一种易吸收的高效铁制剂,工业上以硫铁矿(主要成分为
)是一种易吸收的高效铁制剂,工业上以硫铁矿(主要成分为 )为原料,制备柠檬酸亚铁,其流程如下:
)为原料,制备柠檬酸亚铁,其流程如下:

回答下列问题:
(1)在空气中焙烧时产生对环境有危害的气体是_______ (填化学式);培烧后得到的固体主要成分为 ,焙烧时反应的化学方程式是
,焙烧时反应的化学方程式是_______ 。
(2)滤渣1的成分为_______ (填化学式)。
(3)“还原”过程中与 有关的离子方程式为
有关的离子方程式为_______ ;加入Fe粉还原后,可用_______ (填试剂)检验还原反应是否已经完全反应。
(4)“沉铁”时,反应温度不宜太高的可能原因是_______ 。
(5)生成的 固体需充分洗涤,检验洗涤是否完全的方法是
固体需充分洗涤,检验洗涤是否完全的方法是_______ 。
(6)将制得的 加入到足量柠檬酸溶液中,充分反应后再加入少量铁粉。铁粉的作用是
加入到足量柠檬酸溶液中,充分反应后再加入少量铁粉。铁粉的作用是_______ 。
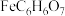 )是一种易吸收的高效铁制剂,工业上以硫铁矿(主要成分为
)是一种易吸收的高效铁制剂,工业上以硫铁矿(主要成分为 )为原料,制备柠檬酸亚铁,其流程如下:
)为原料,制备柠檬酸亚铁,其流程如下:
回答下列问题:
(1)在空气中焙烧时产生对环境有危害的气体是
 ,焙烧时反应的化学方程式是
,焙烧时反应的化学方程式是(2)滤渣1的成分为
(3)“还原”过程中与
 有关的离子方程式为
有关的离子方程式为(4)“沉铁”时,反应温度不宜太高的可能原因是
(5)生成的
 固体需充分洗涤,检验洗涤是否完全的方法是
固体需充分洗涤,检验洗涤是否完全的方法是(6)将制得的
 加入到足量柠檬酸溶液中,充分反应后再加入少量铁粉。铁粉的作用是
加入到足量柠檬酸溶液中,充分反应后再加入少量铁粉。铁粉的作用是
更新时间:2022-10-14 17:14:02
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】碱式硫酸铁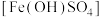 是一种用于污水处理的新型高效絮凝剂。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
是一种用于污水处理的新型高效絮凝剂。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
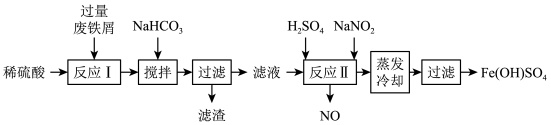
完成下列填空:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表。
(1)反应Ⅰ后的溶液中存在的主要阳离子有_______ 。
(2)加入少量 的目的是将溶液的pH调节在
的目的是将溶液的pH调节在_______ 范围内。
(3)在实验室,“过滤”操作中用到的硅酸盐仪器是_______ 。
(4)反应Ⅱ加入 的目的是
的目的是_______ ,反应的离子方程式为_______ 。
(5)该流程中“蒸发”要采用减压蒸发,相对于常压蒸发,减压蒸发的优点是_______ ,溶液的pH也不能过大或过小,原因是_______ 。
(6)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有 及
及 。为检验所得产品中是否含有
。为检验所得产品中是否含有 ,应使用的试剂为_______(选填序号)。
,应使用的试剂为_______(选填序号)。
 是一种用于污水处理的新型高效絮凝剂。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
是一种用于污水处理的新型高效絮凝剂。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下:
完成下列填空:
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表。
| 沉淀物 |  |  |  |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
(2)加入少量
 的目的是将溶液的pH调节在
的目的是将溶液的pH调节在(3)在实验室,“过滤”操作中用到的硅酸盐仪器是
(4)反应Ⅱ加入
 的目的是
的目的是(5)该流程中“蒸发”要采用减压蒸发,相对于常压蒸发,减压蒸发的优点是
(6)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有
 及
及 。为检验所得产品中是否含有
。为检验所得产品中是否含有 ,应使用的试剂为_______(选填序号)。
,应使用的试剂为_______(选填序号)。| A.氯水 | B.KSCN溶液 | C.NaOH溶液 | D.酸性 溶液 溶液 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体( ):
):
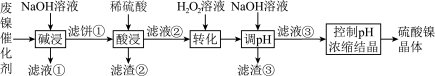
某温度下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“碱浸”中 的作用除了去除催化剂表面的油脂外,还具有作用是
的作用除了去除催化剂表面的油脂外,还具有作用是___________ (写一个化学方程式就可以)。为回收金属,通常用稀硫酸将“滤液①”调为中性,生成沉淀,该沉淀的化学式为___________ 。
(2)“滤液②”中含有的金属离子除了“ ”,还有
”,还有___________ 。
(3)“转化”中加入 的主要作用是
的主要作用是___________ (用离子方程式表示)。
(4)利用上述表格数据,计算 的
的
___________ (列出计算式即可,不用化简)。如果“转化”后的溶液中 浓度为
浓度为 ,则“调pH”应控制pH范围:
,则“调pH”应控制pH范围:___________ (填数值)。
 ):
):
某温度下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
| 金属离子 |  |  |  |  |
开始沉淀时( )的pH )的pH | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时( )的pH )的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中
 的作用除了去除催化剂表面的油脂外,还具有作用是
的作用除了去除催化剂表面的油脂外,还具有作用是(2)“滤液②”中含有的金属离子除了“
 ”,还有
”,还有(3)“转化”中加入
 的主要作用是
的主要作用是(4)利用上述表格数据,计算
 的
的
 浓度为
浓度为 ,则“调pH”应控制pH范围:
,则“调pH”应控制pH范围:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】某研究小组利用某酸性腐蚀废液(含Fe3+、Cu2+、NH4-、SO42-),制取铵明矾[NH4Al(SO4)2·12H2O]的流程如下:
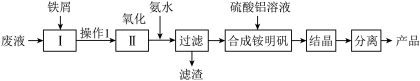
回答下列问题:
(1)加入铁屑的目的是______________________ 。
(2)第II步中用双氧水作为氧化剂。请写出步骤II氧化反应离子方程式__________________ 。
(3)检验溶液中含有NH4+的方法是______________________ 。
(4)工业上将流程中产生的滤渣用NaClO碱性溶液氧化可生成一种高效净水剂(Na2FeO4),写出对应的离子方程式:_________________________________ 。
(5)固体铵明矾加热过程中,固体质量随温度的变化如图所示。
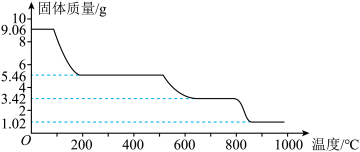
若将铵明矾加热灼烧,400℃时剩余固体成分的化学式为___________ 。在温度从800℃到950℃的过程中得到的两种氧化物,一种为固体,一种为氧化性气体,该气体的名称是___________ 。

回答下列问题:
(1)加入铁屑的目的是
(2)第II步中用双氧水作为氧化剂。请写出步骤II氧化反应离子方程式
(3)检验溶液中含有NH4+的方法是
(4)工业上将流程中产生的滤渣用NaClO碱性溶液氧化可生成一种高效净水剂(Na2FeO4),写出对应的离子方程式:
(5)固体铵明矾加热过程中,固体质量随温度的变化如图所示。

若将铵明矾加热灼烧,400℃时剩余固体成分的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】如图,有以下物质相互转化,其中B溶液为浅绿色,I溶液为棕黄色,J为AgCl,请回答:
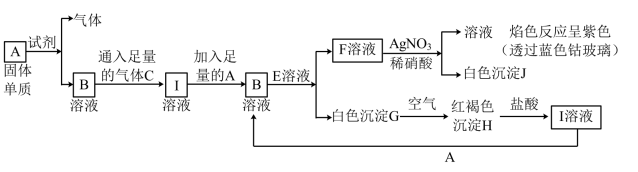
(1)C是(填化学式)_____ ,F的化学式_____ .
(2)写出B的化学式______ ,检验B中阳离子的操作方法是__________________ .(只填一种方法,用文字表述)
(3)写出由G转变成H的化学方程式_______________________ .
(4)写出检验I溶液中阳离子的离子方程式________________ ;向I溶液中加入单质Cu的有关离子反应方程式是______________ .

(1)C是(填化学式)
(2)写出B的化学式
(3)写出由G转变成H的化学方程式
(4)写出检验I溶液中阳离子的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】在化学研究中,往往可以通过观察现象认识物质变化的情况。请分析以下一组有现象变化的化学反应。
(1)用离子方程式解释现象I中出现胶状沉淀的原因: ______ 。
(2)II中加碱时出现的现象是____________________ ,此现象说明溶液中发生反应的离子方程式是__________________________ 。
(3)III中加碱时出现的现象是_____ 。
(4)IV中加酸时出现的现象是_____________ ,用离子方程式解释产生此现象的原因:___________________ 。
(5)滴加试剂顺序的变化会影响溶液中的现象和发生的反应。请继续分析以下实验。
①探究加酸时Fe(NO3)2溶液中是否发生了反应:向1.0 mL 0.1 mol·L-1 Fe(NO3)2溶液中_______ ,如果溶液变红色,说明溶液中含Fe3+,证明加酸时溶液中发生了反应。(请将上述操作补充完整)
②推测溶液中产生Fe3+的可能原因有两种:a._________ ;b._________ 。
| 实验 | 试剂及操作 | 现象 | |
| 试管 | 滴管 | ||
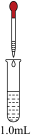 | 饱和Na2SiO3溶液(含2滴酚酞) | 先滴加1.0 mL0.5 mol·L-1NaOH溶液;再滴加1.5 mL 1.0 mol·L-1H2SO4溶液 | Ⅰ.红色溶液中出现胶状沉淀 |
| 0.1 mol·L-1AlCl3溶液 | Ⅱ.加碱时____;加酸时产生白色沉淀,又逐渐溶解至消失 | ||
| 0.1 mol·L-1Fe(NO3)2溶液 | Ⅲ.加碱时____;加酸后得棕黄色溶液 | ||
| 新制饱和氯水 | Ⅳ.加碱时溶液变为无色;加酸后____ | ||
(2)II中加碱时出现的现象是
(3)III中加碱时出现的现象是
(4)IV中加酸时出现的现象是
(5)滴加试剂顺序的变化会影响溶液中的现象和发生的反应。请继续分析以下实验。
| 实验 | 试剂及操作 | 现象 | |
| 试管 | 滴管 | ||
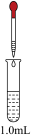 | 0.1 mol·L-1 Fe(NO3)2溶液 | 先滴加1.5 mL 1.0 mol·L-1 H2SO4溶液;再滴加1.0 mL 0.5 mol·L-1NaOH溶液 | Ⅴ.加酸时溶液无明显现象;加碱后溶液依然没有明显变化 |
②推测溶液中产生Fe3+的可能原因有两种:a.
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】由硫铁矿烧渣(主要成分为 、
、 、
、 和
和 )得到绿矾
)得到绿矾 ,然后制取透明氧化铁颜料的流程如下:
,然后制取透明氧化铁颜料的流程如下: ),难溶于水;②“还原”时,
),难溶于水;②“还原”时, 能将
能将 中的硫元素氧化为+6价。
中的硫元素氧化为+6价。
回答下列问题:
(1)“滤渣”中的主要成分有过量的 和
和___________ (填化学式)。
(2)“还原”过程中涉及的离子方程式为___________ 。
(3)流程中“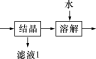 ”环节的目的是
”环节的目的是___________ 。
(4)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正的氢氧化铁,而且还可以___________ 。
(5)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁1.2红的含量。已知 的吸光度
的吸光度 (对特定波长光的吸收程度)与
(对特定波长光的吸收程度)与 标准溶液浓度的关系如图所示:
标准溶液浓度的关系如图所示: 的质量分数为
的质量分数为___________ %(保留小数点后一位)。
(6)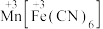 可用作钾离子电池的正极材料,其晶胞结构如下图所示:
可用作钾离子电池的正极材料,其晶胞结构如下图所示: 最近的
最近的 有
有___________ %个。
②第三电离能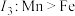 ,结合原子结构解释原因:
,结合原子结构解释原因:___________ %。
③ 放电后转化为
放电后转化为 ,充电时物质的变化如下:
,充电时物质的变化如下:
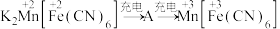
写出充电时生成A的电极反应式:___________ (请标注A中Fe和Mn的化合价)。
 、
、 、
、 和
和 )得到绿矾
)得到绿矾 ,然后制取透明氧化铁颜料的流程如下:
,然后制取透明氧化铁颜料的流程如下: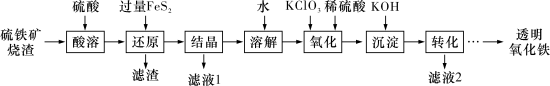
 ),难溶于水;②“还原”时,
),难溶于水;②“还原”时, 能将
能将 中的硫元素氧化为+6价。
中的硫元素氧化为+6价。回答下列问题:
(1)“滤渣”中的主要成分有过量的
 和
和(2)“还原”过程中涉及的离子方程式为
(3)流程中“
 ”环节的目的是
”环节的目的是(4)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正的氢氧化铁,而且还可以
(5)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁1.2红的含量。已知
 的吸光度
的吸光度 (对特定波长光的吸收程度)与
(对特定波长光的吸收程度)与 标准溶液浓度的关系如图所示:
标准溶液浓度的关系如图所示: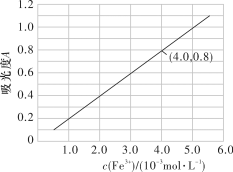
 的质量分数为
的质量分数为(6)
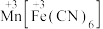 可用作钾离子电池的正极材料,其晶胞结构如下图所示:
可用作钾离子电池的正极材料,其晶胞结构如下图所示: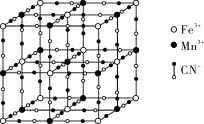
 最近的
最近的 有
有②第三电离能
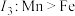 ,结合原子结构解释原因:
,结合原子结构解释原因:③
 放电后转化为
放电后转化为 ,充电时物质的变化如下:
,充电时物质的变化如下: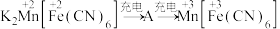
写出充电时生成A的电极反应式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】含钒化合物广泛用于冶金、化工行业。由富钒废渣(含V2O3、V2O4和Na2O•Al2O3•4SiO2、FeO)制备V2O5的一种流程如下:

查阅资料:①部分含钒物质在水溶液中的主要存在形式如下:
②本工艺中,生成氢氧化物沉淀的pH如下:
回答下列问题:
(1)写出基态V原子的价电子排布式_________________________ 。
(2)“焙烧”中,将“研磨”所得粉末与O2逆流混合的目的为___________________ ;所生成的气体A可在___________ 工序中再利用。
(3)“酸浸”中V元素发生的离子反应方程式__________________________ 。
(4)滤渣2含有的物质为__________________ 。
(5)“转化Ⅱ”需要调整pH范围为__________ ,“转化Ⅲ”中含钒物质反应的离子方程式为_________________________________________________ 。
(6)“沉钒”中加入过量NH4Cl有利于晶体析出,其原因为_________________ 。

查阅资料:①部分含钒物质在水溶液中的主要存在形式如下:
pH | <1 | 1~4 | 4~6 | 6~8.5 | 8.5~13 | >13 |
主要形式 | VO | V2O5 | 多矾酸根 | VO | 多矾酸根 | VO |
备注 | 多矾酸盐在水中溶解度较小 | |||||
物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
开始沉淀pH | 7.0 | 1.9 | 3.2 |
沉淀完全pH | 9.0 | 3.2 | 4.7 |
(1)写出基态V原子的价电子排布式
(2)“焙烧”中,将“研磨”所得粉末与O2逆流混合的目的为
(3)“酸浸”中V元素发生的离子反应方程式
(4)滤渣2含有的物质为
(5)“转化Ⅱ”需要调整pH范围为
(6)“沉钒”中加入过量NH4Cl有利于晶体析出,其原因为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】利用油脂厂废弃的镍(Ni)催化剂(主要含有Ni、Al、Fe及少量 、
、 、
、 )制备
)制备 的工艺流程如下:
的工艺流程如下:
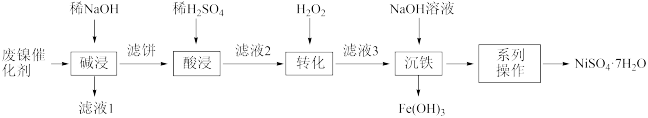
回答下列问题:
(1)为加快“碱浸”的速率可采取的措施是___________ (任写一条);
(2)“碱浸”中 的作用有:去除油脂、
的作用有:去除油脂、___________ ;
(3)“滤液2”中含金属阳离子,主要有:___________ ;
(4)①“转化”中反应的离子方程式是___________ , 也能转化
也能转化 ,工业生产中不选用
,工业生产中不选用 的原因是
的原因是___________ ;
②“转化”中可替代 的最佳物质是
的最佳物质是___________ (填标号);
a. b.
b. c.Fe
c.Fe
(5)“转化”时,应控制的pH范围为___________ ;
(6)某温度下, 分解得到铁、氧质量比为
分解得到铁、氧质量比为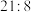 的氧化物,其化学式为
的氧化物,其化学式为___________ 。
 、
、 、
、 )制备
)制备 的工艺流程如下:
的工艺流程如下:
回答下列问题:
(1)为加快“碱浸”的速率可采取的措施是
(2)“碱浸”中
 的作用有:去除油脂、
的作用有:去除油脂、(3)“滤液2”中含金属阳离子,主要有:
(4)①“转化”中反应的离子方程式是
 也能转化
也能转化 ,工业生产中不选用
,工业生产中不选用 的原因是
的原因是②“转化”中可替代
 的最佳物质是
的最佳物质是a.
 b.
b. c.Fe
c.Fe(5)“转化”时,应控制的pH范围为
| 氢氧化物 |  |  |  |  |
| 开始沉淀的pH | 7.5 | 2.2 | 4.1 | 6.4 |
| 沉淀完全的pH | 9.5 | 3.5 | 5.4 | 8.4 |
 分解得到铁、氧质量比为
分解得到铁、氧质量比为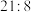 的氧化物,其化学式为
的氧化物,其化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】以盐湖锂精矿(主要成分为Li2CO3,还含有少量的CaCO3)和盐湖卤水(含一定浓度LiCl和MgCl2)为原料均能制备高纯Li2CO3。
(1) 以锂精矿为原料制取碳酸锂的流程如下,其中“碳化溶解”的装置如图所示。
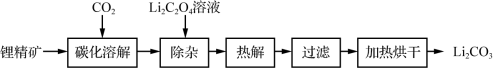
已知:Ⅰ.20 ℃时LiOH的溶解度为12.8 g。
Ⅱ.Li2CO3在不同温度下的溶解度:0 ℃ 1.54 g,20 ℃ 1.33 g,80 ℃ 0.85 g。
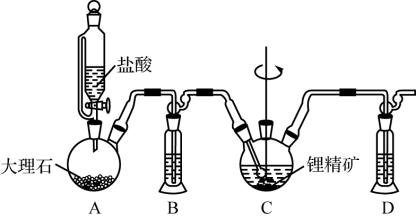
①装置C中主要反应的化学方程式为______ 。
②装置C中的反应需在常温下进行,温度越高锂精矿转化速率越小的原因可能是______ 。保持温度、反应时间、反应物和溶剂的量不变,实验中提高锂精矿转化率的操作有______ 。
③热解、过滤获得Li2CO3的表面有少量Li2C2O4,未经洗涤也不会影响最终Li2CO3产品的纯度,其原因是______ 。
(2)设计由盐湖卤水制取Li2CO3的实验方案:向浓缩后的盐湖卤水______ 。[已知:pH=10时Mg(OH)2完全沉淀,实验中必须用的试剂:NaOH溶液、Na2CO3溶液]。
(1) 以锂精矿为原料制取碳酸锂的流程如下,其中“碳化溶解”的装置如图所示。

已知:Ⅰ.20 ℃时LiOH的溶解度为12.8 g。
Ⅱ.Li2CO3在不同温度下的溶解度:0 ℃ 1.54 g,20 ℃ 1.33 g,80 ℃ 0.85 g。

①装置C中主要反应的化学方程式为
②装置C中的反应需在常温下进行,温度越高锂精矿转化速率越小的原因可能是
③热解、过滤获得Li2CO3的表面有少量Li2C2O4,未经洗涤也不会影响最终Li2CO3产品的纯度,其原因是
(2)设计由盐湖卤水制取Li2CO3的实验方案:向浓缩后的盐湖卤水
您最近一年使用:0次






