含钒化合物广泛用于冶金、化工行业。由富钒废渣(含V2O3、V2O4和Na2O•Al2O3•4SiO2、FeO)制备V2O5的一种流程如下:

查阅资料:①部分含钒物质在水溶液中的主要存在形式如下:
②本工艺中,生成氢氧化物沉淀的pH如下:
回答下列问题:
(1)写出基态V原子的价电子排布式_________________________ 。
(2)“焙烧”中,将“研磨”所得粉末与O2逆流混合的目的为___________________ ;所生成的气体A可在___________ 工序中再利用。
(3)“酸浸”中V元素发生的离子反应方程式__________________________ 。
(4)滤渣2含有的物质为__________________ 。
(5)“转化Ⅱ”需要调整pH范围为__________ ,“转化Ⅲ”中含钒物质反应的离子方程式为_________________________________________________ 。
(6)“沉钒”中加入过量NH4Cl有利于晶体析出,其原因为_________________ 。

查阅资料:①部分含钒物质在水溶液中的主要存在形式如下:
pH | <1 | 1~4 | 4~6 | 6~8.5 | 8.5~13 | >13 |
主要形式 | VO | V2O5 | 多矾酸根 | VO | 多矾酸根 | VO |
备注 | 多矾酸盐在水中溶解度较小 | |||||
物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 |
开始沉淀pH | 7.0 | 1.9 | 3.2 |
沉淀完全pH | 9.0 | 3.2 | 4.7 |
(1)写出基态V原子的价电子排布式
(2)“焙烧”中,将“研磨”所得粉末与O2逆流混合的目的为
(3)“酸浸”中V元素发生的离子反应方程式
(4)滤渣2含有的物质为
(5)“转化Ⅱ”需要调整pH范围为
(6)“沉钒”中加入过量NH4Cl有利于晶体析出,其原因为
更新时间:2023-01-17 10:51:53
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室用下面装置测定FeO和Fe2O3固体混合物中Fe2O3的质量,D装置的硬质双通玻璃管中的固体物质是FeO和Fe2O3的混合物。

(1)如何检查装置A的气密性?_____ 。
(2)为了安全,在点燃D处的酒精灯之前,必须进行的操作是_____ 。
(3)装置B的作用是_____ 。装置C中装的液体是_____ ,所起的作用是_____ 。
(4)点燃D处的酒精灯,写出在硬质双通玻璃管中发生反应的化学方程式_____ 。
(5)若FeO和Fe2O3固体混合物的质量为23.2g,反应完全后U形管的质量增加7.2g,则混合物中Fe2O3的质量为_____ 。

(1)如何检查装置A的气密性?
(2)为了安全,在点燃D处的酒精灯之前,必须进行的操作是
(3)装置B的作用是
(4)点燃D处的酒精灯,写出在硬质双通玻璃管中发生反应的化学方程式
(5)若FeO和Fe2O3固体混合物的质量为23.2g,反应完全后U形管的质量增加7.2g,则混合物中Fe2O3的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料。以钛铁矿(主要成分为钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如图所示。

请回答下列问题:
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C=2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为_______ ;钛酸亚铁和浓H2SO4反应的产物之一是TiOSO4,反应中无气体生成,该反应的化学方程式为_______ 。
(2)上述生产流程中加入铁屑的目的是_______ 。此时溶液Ⅰ中含有Fe2+、TiO2+和少量Mg2+等阳离子,常温下,其对应氢氧化物的Ksp如表所示。
常温下,若所得溶液中Mg2+的物质的量浓度为0.001 8 mol·L-1,当溶液的pH等于_______ 时,Mg(OH)2开始沉淀。
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl4的化学方程式为_______ 。Mg还原TiCl4过程必须在1 070 K的温度下进行,你认为还应该控制的反应条件是_______ ,除去所得金属钛中少量的金属镁可用的试剂是_______ 。

请回答下列问题:
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C=2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为
(2)上述生产流程中加入铁屑的目的是
| 氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl4的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)可用于制备FeCO3,其流程如下:
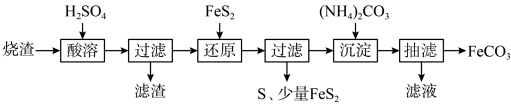
已知:“还原”时,FeS2与H2SO4不反应;Fe3+通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ为FeS2+14Fe3++8H2O=15Fe2++ 2SO +16H+。
+16H+。
(1)滤渣的成分为_____ ;“还原”后为检验Fe3+是否反应完全,可以用什么试剂_____ 。
(2)“还原”时反应Ⅱ的离子方程式_____ 。
(3)下列操作或描述不正确的是_____ 。
A “沉淀”时,可以先将溶液调节成强碱性,再加入(NH4)2CO3以使沉淀完全
B 抽滤时,应选择比布氏漏斗内径略小又能将全部小孔盖住的滤纸
C 抽滤不宜用于过滤胶状沉淀,因为其易在滤纸上形成一层密实的沉淀,溶液不易透过
D 制得的FeCO3还需洗涤、烘干
(4)如图安装抽滤装置,经过一系列操作完成抽滤。请选择合适的编号,按正确的操作顺序补充 完整:
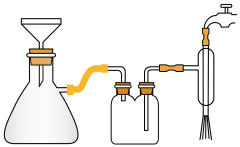
在布氏漏斗中加入滤纸→__ →__ →__ →__ →确认抽干。
①转移固液混合物;②开大水龙头;③关闭水龙头;④微开水龙头;⑤加入少量蒸馏水润湿滤纸。
(5)抽滤后得到的FeCO3需要充分洗涤,如何检验FeCO3已洗涤干净?_____ 。

已知:“还原”时,FeS2与H2SO4不反应;Fe3+通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ为FeS2+14Fe3++8H2O=15Fe2++ 2SO
 +16H+。
+16H+。(1)滤渣的成分为
(2)“还原”时反应Ⅱ的离子方程式
(3)下列操作或描述不正确的是
A “沉淀”时,可以先将溶液调节成强碱性,再加入(NH4)2CO3以使沉淀完全
B 抽滤时,应选择比布氏漏斗内径略小又能将全部小孔盖住的滤纸
C 抽滤不宜用于过滤胶状沉淀,因为其易在滤纸上形成一层密实的沉淀,溶液不易透过
D 制得的FeCO3还需洗涤、烘干
(4)如图安装抽滤装置,经过一系列操作完成抽滤。请选择合适的编号,按正确的操作顺序补充 完整:

在布氏漏斗中加入滤纸→
①转移固液混合物;②开大水龙头;③关闭水龙头;④微开水龙头;⑤加入少量蒸馏水润湿滤纸。
(5)抽滤后得到的FeCO3需要充分洗涤,如何检验FeCO3已洗涤干净?
您最近一年使用:0次
【推荐1】无机净水剂主要有铁系和铝系两类,但铝对人体有慢性毒害作用,所以研制各种铁系净水剂成为热门。聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m是一种常用的净水剂,其生产工艺如下:
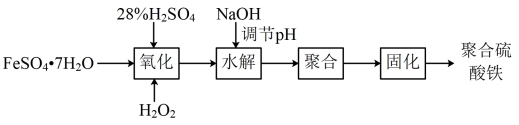
回答下列问题:
(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒、玻璃棒外,还有______ 。
(2)FeSO4·7H2O在空气中会被氧化变质,检验其已变质的操作:__________ 。
(3)“氧化”时发生反应的离子方程式为___________ 。
(4)Fe3+水解会使溶液的pH减小,加入NaOH调节pH的目的是_________ 。
(5)聚合硫酸铁中n(Fe3+):n(OH-):n(SO )比值的确定方法:取一定量的聚合硫酸铁,先加入足量的稀盐酸酸化后,然后加入BaCl2溶液,经操作Ⅰ后得到沉淀A和滤液B,洗涤、干燥沉淀A后称得质量为3.495g,向滤液B中加入足量的NaOH充分反应,将经操作Ⅰ后得到的滤渣洗涤、灼烧至恒重,得2.40g固体C。
)比值的确定方法:取一定量的聚合硫酸铁,先加入足量的稀盐酸酸化后,然后加入BaCl2溶液,经操作Ⅰ后得到沉淀A和滤液B,洗涤、干燥沉淀A后称得质量为3.495g,向滤液B中加入足量的NaOH充分反应,将经操作Ⅰ后得到的滤渣洗涤、灼烧至恒重,得2.40g固体C。
①生成沉淀A的离子方程式为___________ 。
②操作Ⅰ的名称为__________ ,固体C的化学式为__________ 。
③聚合硫酸铁中n(Fe3+):n(OH-):n(SO )
)_________ 。

回答下列问题:
(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒、玻璃棒外,还有
(2)FeSO4·7H2O在空气中会被氧化变质,检验其已变质的操作:
(3)“氧化”时发生反应的离子方程式为
(4)Fe3+水解会使溶液的pH减小,加入NaOH调节pH的目的是
(5)聚合硫酸铁中n(Fe3+):n(OH-):n(SO
 )比值的确定方法:取一定量的聚合硫酸铁,先加入足量的稀盐酸酸化后,然后加入BaCl2溶液,经操作Ⅰ后得到沉淀A和滤液B,洗涤、干燥沉淀A后称得质量为3.495g,向滤液B中加入足量的NaOH充分反应,将经操作Ⅰ后得到的滤渣洗涤、灼烧至恒重,得2.40g固体C。
)比值的确定方法:取一定量的聚合硫酸铁,先加入足量的稀盐酸酸化后,然后加入BaCl2溶液,经操作Ⅰ后得到沉淀A和滤液B,洗涤、干燥沉淀A后称得质量为3.495g,向滤液B中加入足量的NaOH充分反应,将经操作Ⅰ后得到的滤渣洗涤、灼烧至恒重,得2.40g固体C。①生成沉淀A的离子方程式为
②操作Ⅰ的名称为
③聚合硫酸铁中n(Fe3+):n(OH-):n(SO
 )
)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】弱电解质的电离平衡、盐类的水解平衡均属于化学平衡。根据要求回答问题:
(1)铝盐的水解原理在生活中应用广泛,如明矾常作净水剂,其净水的原理是___________ (用离子方程式表示);如硫酸铝常作泡沫灭火器原料之一,其原理是___________ (用离子方程式表示)
(2)在氯化铜晶体(CuCl2·2H2O)中含有FeCl2杂质,为制得纯净的氯化铜晶体,首先将其溶于水后加少量盐酸配制成水溶液,然后按下图所示的操作步骤进行提纯。
已知:在pH=4~5时,Cu2+、Fe2+不水解,而Fe3+几乎完全水解而沉淀
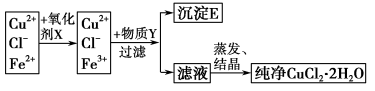
回答下列问题:
①下列物质都可以作为氧化剂,其中适合本实验的X是___________ (填字母)
A.H2O2 B.KMnO4 C.氯水 D.K2Cr2O7
②加入Y调节溶液的pH至4~5,物质Y可能是___________ (填字母)
A.氨水 B.Cu C.Cu(OH)2 D.CuO
③欲将CuCl2·2H2O加热制得无水CuCl2,可在HCl气氛下蒸发,否则得不到纯净CuCl2固体,试用简要的文字和相应化学方程式解释这样操作的原因:___
(3)常温下,浓度均为0.1mol·L-1的六种溶液的pH如下表:
①上述盐溶液中的阴离子,结合质子能力最强的是______
②根据表中数据,浓度均为0.01mol·L-1的下列五种物质的溶液中,酸性最强的是___________ (填字母);将各溶液分别稀释100倍,pH变化最小的是___________ (填字母)
A.HCN B.HClO C.H2SO4 D.CH3COOH E.H2CO3
③向NaClO溶液中通入少量二氧化碳气体,写出发生反应的离子方程式___________
(1)铝盐的水解原理在生活中应用广泛,如明矾常作净水剂,其净水的原理是
(2)在氯化铜晶体(CuCl2·2H2O)中含有FeCl2杂质,为制得纯净的氯化铜晶体,首先将其溶于水后加少量盐酸配制成水溶液,然后按下图所示的操作步骤进行提纯。
已知:在pH=4~5时,Cu2+、Fe2+不水解,而Fe3+几乎完全水解而沉淀

回答下列问题:
①下列物质都可以作为氧化剂,其中适合本实验的X是
A.H2O2 B.KMnO4 C.氯水 D.K2Cr2O7
②加入Y调节溶液的pH至4~5,物质Y可能是
A.氨水 B.Cu C.Cu(OH)2 D.CuO
③欲将CuCl2·2H2O加热制得无水CuCl2,可在HCl气氛下蒸发,否则得不到纯净CuCl2固体,试用简要的文字和相应化学方程式解释这样操作的原因:
(3)常温下,浓度均为0.1mol·L-1的六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | Na2SO4 |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 7.0 |
①上述盐溶液中的阴离子,结合质子能力最强的是
②根据表中数据,浓度均为0.01mol·L-1的下列五种物质的溶液中,酸性最强的是
A.HCN B.HClO C.H2SO4 D.CH3COOH E.H2CO3
③向NaClO溶液中通入少量二氧化碳气体,写出发生反应的离子方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】钡元素在自然界主要以重晶石(BaSO4,含有少量Fe2O3、Al2O3和SiO2杂质)的形式存在于地壳中,将矿石进行浮选、粉碎,酸浸处理后即可用于工业制备钡的常见化合物及其单质。
(1)已知钡元素的原子结构示意图为 ,则钡元素在周期表中的位置是
,则钡元素在周期表中的位置是___________ 。
(2)使用稀盐酸对矿石进行酸浸处理,然后过滤,能除去矿石中的杂质___________ (填化学式)。
(3)将处理过的矿石用饱和Na2CO3溶液进行多次浸泡,可使绝大部分BaSO4转化为BaCO3。已知反应温度下,Ksp(BaSO4)=1.0×10-10,Ksp (BaCO3)=2.5 ×10-9。则将BaSO4配制成悬浊液后,其中c(Ba2+ )=___________ ,反应BaSO4(s)+CO (aq)
(aq)  BaCO3(s) +SO
BaCO3(s) +SO (aq)的平衡常数K=
(aq)的平衡常数K=___________ 。
(4)向(3)中获得的固体混合物中加入过量___________ ,充分反应后过滤,可除去未转化的BaSO4和SiO2,然后通过 ___________ 等操作获得BaCl2·2H2O晶体。
(5)若由BaCl2·2H2O晶体加热分解获得无水BaCl2,是否需要在HCl气体氛围中进行操作?___________ (填“是”或“否”),理由是 ___________ 。
(1)已知钡元素的原子结构示意图为
 ,则钡元素在周期表中的位置是
,则钡元素在周期表中的位置是(2)使用稀盐酸对矿石进行酸浸处理,然后过滤,能除去矿石中的杂质
(3)将处理过的矿石用饱和Na2CO3溶液进行多次浸泡,可使绝大部分BaSO4转化为BaCO3。已知反应温度下,Ksp(BaSO4)=1.0×10-10,Ksp (BaCO3)=2.5 ×10-9。则将BaSO4配制成悬浊液后,其中c(Ba2+ )=
 (aq)
(aq)  BaCO3(s) +SO
BaCO3(s) +SO (aq)的平衡常数K=
(aq)的平衡常数K=(4)向(3)中获得的固体混合物中加入过量
(5)若由BaCl2·2H2O晶体加热分解获得无水BaCl2,是否需要在HCl气体氛围中进行操作?
您最近一年使用:0次
【推荐1】零排放、太阳能、绿色光源等高科技点亮2010上海世博。
(1)世博园区外围设置生态化停车场,有害尾气被纳米光触媒涂料分解为无毒物质,汽车尾气中的下列物质属于由极性键形成的非极性分子的是____ 。
a.CO b.NO c.NO2 d.CO2
(2)“一轴四馆”中安装了高亮度节能的陶瓷金卤灯,金卤灯中填充物通常包含NA,81Tl、49In、SC,I等元素的单质或化合物.有关说法正确的是_____ 。
a.第ⅢA元素铊和铟,第一电离能Tl小于In
b.元素Sc位于周期表s区
c.钠的熔点低,是因为金属键较弱
d.I2溶于KI溶液,可产生I3-,由价层互斥理论可推知I3-呈直线形
(3)世博锗广泛采用了冰蓄冷空调.冰蓄冷空调采用液态化合物乙二醇(HOCH2CH2OH)介质,乙二醇沸点高,是由于_____ 。
(4)上海城区大规模集中使用“21世纪绿色光源”LED半导体照明,LED晶片采厢砷化镓(GaAs)等材料组成。其中Ga原子在基态时,核外电子排布式为:_____ 。GaAs的晶胞结构如图,晶胞中含砷原子数为_____ 。_____ 。
(1)世博园区外围设置生态化停车场,有害尾气被纳米光触媒涂料分解为无毒物质,汽车尾气中的下列物质属于由极性键形成的非极性分子的是
a.CO b.NO c.NO2 d.CO2
(2)“一轴四馆”中安装了高亮度节能的陶瓷金卤灯,金卤灯中填充物通常包含NA,81Tl、49In、SC,I等元素的单质或化合物.有关说法正确的是
a.第ⅢA元素铊和铟,第一电离能Tl小于In
b.元素Sc位于周期表s区
c.钠的熔点低,是因为金属键较弱
d.I2溶于KI溶液,可产生I3-,由价层互斥理论可推知I3-呈直线形
(3)世博锗广泛采用了冰蓄冷空调.冰蓄冷空调采用液态化合物乙二醇(HOCH2CH2OH)介质,乙二醇沸点高,是由于
(4)上海城区大规模集中使用“21世纪绿色光源”LED半导体照明,LED晶片采厢砷化镓(GaAs)等材料组成。其中Ga原子在基态时,核外电子排布式为:

您最近一年使用:0次
【推荐2】N、P、Ga、Cu、Zn等常见元素,在电子、材料、生命科学等领域应用广泛,回答下列问题:
(1)GaN是制造5G芯片的材料,氮化镓和氮化铝LED可发出紫外光。回答下列问题:
①基态Ga原子的核外电子排布式为______________ 。
②根据元素周期律,元素的电负性Ga_____ (填“大于”或“小于”,下同)As。
(2)已知Cu、Zn的第二电离能分别为1957.9kJ·mol-1、1733.3kJ·mol-1,前者高于后者的原因是_____________ 。
(3)磷(P)是组成生命物质的重要元素,回答下列问题。
①基态P原子外围电子的轨道表示式为___ 。与氮(N)相比,第一电离能P_____ N(填“=”“>”或“<”)。每个白磷分子中有____ 个σ键。
②PH3的分子构型与NH3的分子构型相似。下列说法正确的是_____ 。
A. P—H键的极性大于N—H键的极性
B.PH3的键角大于NH3的键角,但小于BF3分子中的键角
C.PH3中P—H键的键长大于N—H键的键长
D. N、P的第一电离能均比同周期相邻元素的大
(1)GaN是制造5G芯片的材料,氮化镓和氮化铝LED可发出紫外光。回答下列问题:
①基态Ga原子的核外电子排布式为
②根据元素周期律,元素的电负性Ga
(2)已知Cu、Zn的第二电离能分别为1957.9kJ·mol-1、1733.3kJ·mol-1,前者高于后者的原因是
(3)磷(P)是组成生命物质的重要元素,回答下列问题。
①基态P原子外围电子的轨道表示式为
②PH3的分子构型与NH3的分子构型相似。下列说法正确的是
A. P—H键的极性大于N—H键的极性
B.PH3的键角大于NH3的键角,但小于BF3分子中的键角
C.PH3中P—H键的键长大于N—H键的键长
D. N、P的第一电离能均比同周期相邻元素的大
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物,单质铁、砷及它们的化合物广泛应用于超导体材料等领域,请回答下列问题:
(1)Fe的基态原子核外价层电子排布图为_______ 。
(2) 是一种很好的配体,
是一种很好的配体, 的沸点
的沸点_______ (填“>”“=”或“<”) 。
。
(3)N原子核外有_______ 种不同运动状态的电子。基态N原子中,能量最高的电子所占据的原子轨道的形状为_______ 。
(4)科学家通过X射线测得胆矾结构示意图可简单表示如图,图中虚线表示的作用力为_______ 。

(5)As的卤化物的熔点如下:
表中卤化物熔点差异的原因是_______ 。
(6)向 溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表
溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表 ,则
,则 与氮原子之间形成的化学键是
与氮原子之间形成的化学键是_______ , 的配位数为
的配位数为_______ 。

(7)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯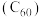 的结构如图,分子中碳原子轨道的杂化类型为
的结构如图,分子中碳原子轨道的杂化类型为_______ ; 分子中
分子中 键的数目为
键的数目为_______ 个。

(1)Fe的基态原子核外价层电子排布图为
(2)
 是一种很好的配体,
是一种很好的配体, 的沸点
的沸点 。
。(3)N原子核外有
(4)科学家通过X射线测得胆矾结构示意图可简单表示如图,图中虚线表示的作用力为

(5)As的卤化物的熔点如下:
 | 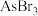 | 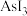 | |
| 熔点/K | 256.8 | 304 | 413 |
(6)向
 溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表
溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表 ,则
,则 与氮原子之间形成的化学键是
与氮原子之间形成的化学键是 的配位数为
的配位数为
(7)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯
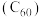 的结构如图,分子中碳原子轨道的杂化类型为
的结构如图,分子中碳原子轨道的杂化类型为 分子中
分子中 键的数目为
键的数目为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】处理并利用硫酸尾气NOx制备工业原料亚硝酸钠和硝酸钠的工艺如下:___________ ,过高和过低都不利于NOx的吸收,其原因是___________ 。
(3)在30℃时进行碱液吸收NOx的反应,此时NaOH的浓度控制在22%~25%最佳,NaOH浓度不宜过高的原因是___________ 。
(5)转化池中加入硝酸用于除杂,同时产生NO,其发生的离子反应方程式为___________ 。在转化池内通常需要一定量的空气,其作用是___________ 。
A.减少氮氧化物二次污染 B. 除去溶液中的杂质
C.有利于产品的分离 D. 节省HNO3的用量
(6)已知硝酸尾气中NOx的总含量为6.2×10-3mol/m3,气体流速为1268m3/h,经该吸收工艺后,排出气体中NOx的总含量降低为5.0×10-4mol/m3,则每小时至少需要质量分数为25%的NaOH溶液(密度为1.04g/cm3)___________ m3(保留2位有效数字)。


| A.顶部 | B.上部 | C.中部 | D.底部 |
(3)在30℃时进行碱液吸收NOx的反应,此时NaOH的浓度控制在22%~25%最佳,NaOH浓度不宜过高的原因是

| A.冷却结晶 | B.趁热过滤 | C.蒸发至干 | D.重结晶 |
(5)转化池中加入硝酸用于除杂,同时产生NO,其发生的离子反应方程式为
A.减少氮氧化物二次污染 B. 除去溶液中的杂质
C.有利于产品的分离 D. 节省HNO3的用量
(6)已知硝酸尾气中NOx的总含量为6.2×10-3mol/m3,气体流速为1268m3/h,经该吸收工艺后,排出气体中NOx的总含量降低为5.0×10-4mol/m3,则每小时至少需要质量分数为25%的NaOH溶液(密度为1.04g/cm3)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】亚氯酸钠(NaClO2)是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等。已知:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2•3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。纯ClO2易分解爆炸。一种制备亚氯酸钠粗产品的工艺流程如图:
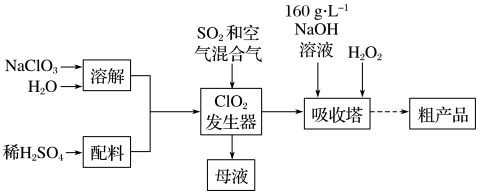
(1)ClO2发生器中反应的离子方程式为_____ ,发生器中鼓入空气的作用可能是____ (填字母)。
a.将SO2氧化成SO3,增强酸性 b.稀释ClO2以防止爆炸 c.将NaClO3还原为ClO2
(2)吸收塔内反应的化学方程式为_____ ,吸收塔内的温度不能超过20℃,其原因是____ 。
(3)从“母液”中可回收的主要物质是_____ 。
(4)从吸收塔中可获得NaClO2溶液,从NaClO2溶液到粗产品(NaClO2)经过的操作步骤依次为①减压,55℃蒸发结晶;②____ ;③____ ;④低于60℃干燥,得到成品。

(1)ClO2发生器中反应的离子方程式为
a.将SO2氧化成SO3,增强酸性 b.稀释ClO2以防止爆炸 c.将NaClO3还原为ClO2
(2)吸收塔内反应的化学方程式为
(3)从“母液”中可回收的主要物质是
(4)从吸收塔中可获得NaClO2溶液,从NaClO2溶液到粗产品(NaClO2)经过的操作步骤依次为①减压,55℃蒸发结晶;②
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上用铝土矿 主要成分为
主要成分为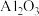 ,还有少量的
,还有少量的 ,
, 等杂质
等杂质 提取氧化铝作冶炼铝的原料,提取的操作过程如下:
提取氧化铝作冶炼铝的原料,提取的操作过程如下:
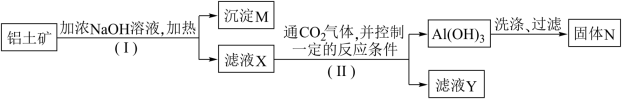
(1) 和II步骤中分离溶液和沉淀的操作是:
和II步骤中分离溶液和沉淀的操作是:__________________ ;
(2)沉淀M中除含有泥沙外,一定还含有____________ ,固体N是____________ ;
(3)滤液X中,含铝元素的溶质的化学式为________________ ,它属于_____  填“酸”、“碱”或“盐”
填“酸”、“碱”或“盐” 类物质;
类物质;
(4)实验室里常往 溶液中加入
溶液中加入________________  填“氨水”或“NaOH溶液”
填“氨水”或“NaOH溶液” 来制取
来制取 ,请写出该反应的方程式
,请写出该反应的方程式___________________________
 主要成分为
主要成分为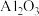 ,还有少量的
,还有少量的 ,
, 等杂质
等杂质 提取氧化铝作冶炼铝的原料,提取的操作过程如下:
提取氧化铝作冶炼铝的原料,提取的操作过程如下:
(1)
 和II步骤中分离溶液和沉淀的操作是:
和II步骤中分离溶液和沉淀的操作是:(2)沉淀M中除含有泥沙外,一定还含有
(3)滤液X中,含铝元素的溶质的化学式为
 填“酸”、“碱”或“盐”
填“酸”、“碱”或“盐” 类物质;
类物质;(4)实验室里常往
 溶液中加入
溶液中加入 填“氨水”或“NaOH溶液”
填“氨水”或“NaOH溶液” 来制取
来制取 ,请写出该反应的方程式
,请写出该反应的方程式
您最近一年使用:0次






